这一新发现的微生物揭示了一个由寄生于细胞的生命所构成的生物多样性世界。而这个世界,才刚刚通过基因组测序技术展露冰山一角。
生命的基本结构是细胞,因此细胞的主要功能被视为生命的标志,包括加工生物分子、生长、复制其遗传物质并产生新个体。但2025年早些时候,科学家发现了一种功能精简到极致的细胞,该细胞彻底挑战了生物学家对生命的定义。
它是一种单细胞生物,目前仅能通过其神秘的基因序列被认知。它的基因组小得惊人:在漫长的演化过程中,它似乎已经摒弃了绝大部分基因。研究团队2025年5月在预印本平台bioRxiv上发表的相关研究成果显示,缺失的基因中包括那些对细胞新陈代谢至关重要的基因,这意味着它既不能代谢营养物质,也无法自主生长。这一发现令这些研究人员震惊不已。
一般基因组高度精简的细胞,仍会编码蛋白质以合成氨基酸、分解碳水化合物供能或合成维生素。但这一切在这种细胞中都不存在,它似乎是一种完全依赖宿主或细胞群落来满足自身营养需求的寄生生物。此前,上述代谢通路一直被认为是所有细胞生存的基础。不过,该生物的“复制核心”(即自我增殖所需的遗传组件,占其基因组的一半以上)保留下来了。
日本筑波大学的演化微生物学家、研究团队负责人中山拓郎(Takuro Nakayama)说:“代谢是我们定义生命的一个关键部分。但关于该细胞的研究发现挑战了这一传统认知,揭示了细胞几乎可以在没有自身新陈代谢的情况下存在。这说明,细胞生命的多样性远超我们之前的认知,且生物的存在形式并非总能契合人类给出的定义。”
中山拓郎研究寄生于其他细胞表面或内部的微生物,以探寻微观世界中未被发现的生物多样性
尽管这种生命形式对科学界而言尚属新发现,但类似的生物可能很常见。法国国家科学研究中心的微生物生态学家普丽 · 洛佩斯-加西亚(Puri López-García,未参与该项研究)指出,在寄生微生物与宿主错综复杂的依存关系中,可能隐藏着相当大比例的微生物多样性。
她说:“归属于这类寄生生物大类的古菌与细菌,多样性极为丰富。其中,细菌可能就占该类群总数的25%至50%。”
这一发现拓展了人类的认知——细胞生命在演化的过程中竟然可以简化至如此微小、简单的程度,甚至能演化成勉强算得上生命的形态。
非凡的发现
中山在科研生涯中,始终秉持着比同行更细致的探索精神。面对一个已十分微小的细胞,他仍会思考:是否有更微小的细胞在此安家呢?
他说:“寄生细胞与宿主细胞的体型差异,有时堪比人与哥斯拉的体型差距。”他被这类依存关系中可能蕴藏的海量未知的生物多样性所吸引,其实验室也一直致力于从海洋中寻找此类关系。海洋属于营养匮乏的环境,这促使细胞之间形成“贸易伙伴关系”。有时,它们松散相连、结伴漂浮,交换着稀有的营养物质与能量;有时,它们则会形成更为有序的组织形式。
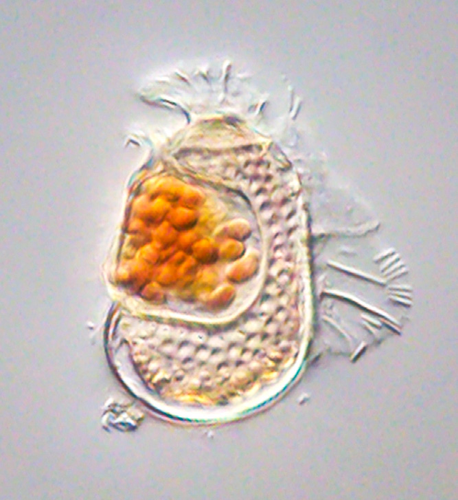
中山团队要探究的是广泛分布于全球的单细胞甲藻Citharistes regius(简称C. regius)。这种甲藻有一个带壁的囊状腔室,用于容纳共生蓝细菌。团队从太平洋采集海水样本以寻找这种藻类,常用的研究手段是对水样中可获取的DNA进行测序分析。这种方法被称为宏基因组学。
中山表示:“这种方法在高效获取宏观全貌方面极其强大。然而,靠这类数据往往难以建立基因序列与其来源细胞之间的关联,罕见生物也容易被遗漏。”因此,其团队采用了更具针对性的方法:在显微镜下从混合样本中识别并物理分离出单个目标细胞。
研究团队确认样本中存在C. regius后,对与该细胞有关的所有基因组进行了测序。不出所料,他们检测到了其共生蓝细菌的DNA,同时也有意外发现:一类古菌的基因序列。作为生命的一大分支,古菌被认为是包括人类在内的真核生物的起源。
海洋甲藻C. regius进化出一个囊状腔室,共生蓝细菌寄居于此
起初,中山团队以为是实验中出现了失误。该古菌的基因组极小,仅含有23.8万个碱基对。相比之下,人类拥有数十亿个碱基对,甚至连大肠杆菌也有数百万个碱基对,与C. regius共生的蓝细菌则有190万个碱基对。此前已知最小的古菌基因组是骑行纳古菌(Nanoarchaeum equitans)的基因组——包含49万个碱基对,是此次新发现的古菌基因组的两倍之多。他们最初认为这个微小的基因组是一个更大基因组的缩写片段,只是被他们的软件错误地汇编了而已。
“我们起初怀疑这是基因组组装过程中的假象。”中山回忆道。为了验证这一猜想,团队采用不同的技术对该基因组进行测序,并通过多个计算机程序运行数据,将DNA片段组装为完整的基因组。结果,所有方法都重建出完全相同的含23.8万个碱基对的环状基因组。“这种一致性让我们确信,这就是真实的完整基因组。”
这意味着中山团队发现了一种新生物。因其基因组极小,他们将其命名为待考证物种奇异少彦名古菌(Candidatus Sukunaarchaeum mirabile,简称少彦名古菌),灵感来自日本以身材矮小著称的神明——少彦名(Sukuna-biko-na)。
准生命谱系
研究团队通过查阅已知基因数据库来分析该古菌时发现,其基因组之所以这么小,是因为大量基因缺失。
少彦名古菌仅编码维持自身增殖所需的最基础蛋白,仅此而已。最奇特的是,除增殖所需的基因外,其基因组中完全找不到任何与生物分子加工和合成相关的基因。缺乏这些代谢途径,它必须将生长与生命维持所需的过程“外包”给其他细胞,即宿主。它完全依赖于宿主存活。
其他共生微生物也存在基因组大幅精简的现象,包括少彦名古菌的近亲。研究表明,这种新发现的微生物属于DPANN古菌门类(也可以称纳古菌或超小古菌),其特征是体型微小、基因组小。DPANN古菌通常被认为是附着在大型原核微生物细胞表面的共生体,其中许多物种的基因组都已大幅简化以匹配这种生存方式。但在此之前,尚无任何一种DPANN古菌的基因组会精简到如此程度。并且,少彦名古菌很早就从DPANN谱系中分化出来,这说明它走上了自己独特的演化之路。
普丽·洛佩斯-加西亚在智利安第斯山脉盐沼考察。她认为,约25%至50%的细菌细胞可能是其他细胞的寄生生物
古菌这一领域总体而言颇为神秘。美国得克萨斯大学奥斯汀分校的微生物生态学家布雷特 · 贝克(Brett Baker,未参与该项研究)表示:“DPANN古菌在代谢能力上存在明显局限。”
少彦名古菌或许能为宿主提供某种未知益处,但更可能是一种自私的寄生生物。悉尼科技大学的微生物学家蒂姆 · 威廉姆斯(Tim Williams,未参与该项研究)指出:“其基因组精简纯粹是出于自私的动机,这完全符合寄生生物的生存模式。”它无法提供任何代谢产物,因此与其他细胞之间的关系很可能是单向索取关系。
其他微生物也演化出类似的极端精简形式。例如,生活在以植物汁液为食的昆虫肠道内的共生菌卡松菌(Carsonella ruddii),其基因组更小,仅有约15.9万个碱基对。然而,此类超小细菌仍保留着代谢基因,能为宿主合成氨基酸、维生素等营养物质,但这是以舍弃相当大一部分独立增殖能力为代价的。威廉姆斯解释道:“这些微生物正朝着细胞器的方向演化,线粒体与叶绿体就是这样演化而来的。而少彦名古菌却走向了相反方向——保留自身增殖所需的基因,却丢失了绝大部分(甚至可能是全部)代谢基因。”
中山团队的成果在线发表后引发广泛关注。荷兰瓦赫宁根大学与研究中心的演化微生物学家、古菌基因组学专家蒂斯 · 埃特马(Thijs Ettema,未参与该项研究)表示:“看到预印本时,我们实验室的成员都很兴奋。此类基因组精简的生物以前也曾被发现,但从未这么夸张。”
一些新闻报道甚至称少彦名古菌或将演化成病毒。然而,尽管二者均依赖宿主完成基础生命活动,但病毒无法自主增殖。
中山强调:“少彦名古菌与病毒之间存在本质区别。少彦名古菌保留了基因表达的核心机制(包括核糖体),尽管是以一种简化的形式;而病毒缺乏核糖体,必须劫持宿主的细胞系统才能增殖。”
埃特马表示,这一发现进一步引发了关于如何定义生命的广泛讨论,因为自然界总能演化出难以简单分类的特例。“它大概率无法独立存活,细菌共生体也是如此。那线粒体、质体这类细胞器,我们又该如何定义?……究竟到何种程度,我们才能称之为生命?”
极简生存之道
关于少彦名古菌,仍有诸多未解之谜。例如,其基因组中很大一部分是由与任何已知序列都不匹配的基因构成。它们似乎编码大分子蛋白,这在极度精简的生物体中十分罕见。
中山团队认为,这些大分子蛋白分布于细胞膜上,并以某种方式维系着古菌与宿主之间的相互作用。对此,埃特马表示,这与其他已知的DPANN古菌的生存模式一致:它们通常被认为是外共生体,附着于体型相对较大的宿主细胞表面。
尽管目前来看少彦名古菌的发现与C. regius甲藻有关,但其真正的宿主身份尚未可知。C. regius甲藻是一种真核生物,而DPANN古菌通常与其他古菌共生。此外,有待讨论的是:少彦名古菌是像其他DPANN古菌一样附着于宿主细胞表面,还是寄生于宿主体内?抑或二者兼具?要回答这些问题,需对该古菌进行直接观测和研究。但截至目前,我们仅能通过一串奇特的基因数据来了解它。
洛佩斯-加西亚说,还存在一种极小的可能性:这些神秘基因或许就是“丢失”的代谢基因,只是它们演化得与原始序列差异过大,以至于无法识别。她解释道:“该基因组进化的速度极快,或许这些基因的功能确实对应着代谢功能,但由于序列差异太大,我们无法在数据库中识别出相应的基因同源物。”
蒂斯·埃特马认为,极简细胞的发现挑战了我们对生命的定义
埃特马认为,自然界中或许存在生存模式更奇特或基因组更精简的物种,只是被研究者忽略了。传统的微生物样本基因组分析方法,可能会将这些物种极小的基因组判定为不完整或低质量,进而予以舍弃或直接忽略。“这些微生物的DNA或许本来就存在于样本中,但测序后被剔除了,因此被忽视掉了。”
中山团队检索了全球海洋环境序列数据库,想看看这种新微生物是否在其他地方出现过,结果是没有。但他们检测到大量高度相似的序列,大概率来自它的近亲。少彦名古菌或许只是多样的微生物世界的冰山一角:微小微生物依附在稍微大一点的微生物上,甚至可能存在于其他微生物体内。它们之间的古老依存关系,才刚刚被揭开。
资料来源 Quanta Magazine