《自然》杂志挑选出了七大很可能在2023年对科学产生重大影响的工具和技术,应用范围从蛋白质测序到电子显微镜,从考古学到天文学。
单分子蛋白质测序
蛋白质组是细胞或器官产生的全套蛋白质,可以深刻揭示有关健康和疾病的详细信息,但如何刻画其特征仍旧是一个相当艰巨的挑战。
构造蛋白质的基础是比核酸更大的一些分子,也就是氨基酸。天然氨基酸大约有20种,相比之下,构成DNA和信使RNA的核苷酸分子只有4种。这意味着,蛋白质的化学多样性要丰富得多。有些蛋白质在细胞中的数量很少,而且与核酸不同,蛋白质无法扩增,这意味着分析蛋白质的方法必须使用已有的材料和技术。
大多数对蛋白质组的分析使用的是质谱法,也即根据质量和电荷分析蛋白质组的组成。这种方法可以同时量化数千种蛋白质,但探测到的蛋白质分子并不能保证被准确识别。另外,这种方法常常忽视蛋白质组中丰度较低的蛋白质。现在,可以测序样本中诸多(甚至是全部)蛋白质的单分子蛋白质测序技术即将问世。这种技术中有很多都类似分析DNA时用到的技术。
得克萨斯大学奥斯汀分校分析生物化学家爱德华 · 马尔科特(Edward Marcotte)正在开发的单分子蛋白质测序方法叫作“荧光测序法”。根据2018年的报道,马尔科特这项技术的基础是一种循序渐进的化学过程:单个氨基酸分子用荧光标记出来,当照相机捕获荧光信号后,再将它们一个接一个地从表面偶联蛋白质的末端剪下来。“我们可以用不同颜色的荧光标记蛋白质,然后在剪下来时逐个观察。”马尔科特解释说。去年,位于康涅狄格州吉尔福德的一家生物技术公司“量子测序”(Quantum-Si)的研究人员提出了另一种荧光测序技术,使用经过荧光标记的“结合物”蛋白质识别蛋白质末端的特定氨基酸(或多肽)序列。
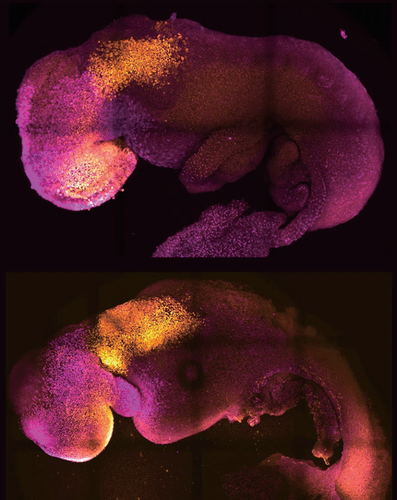
现在,研究人员可以在实验室中制造合成胚胎(下)以表征8天大的自然受孕胚胎(上)
其他研究人员开发的技术则是模拟基于纳米孔的DNA测序技术。这种技术根据多肽在通过微小通道时诱发的电流变化分析它们的性质。2021年,荷兰代尔夫特大学生物物理学家齐斯 · 德克尔(Cees Dekker)和他的同事展示了这种方法。他们在实验中使用了由蛋白质制成的纳米孔,并且成功区分了通过纳米孔的多肽含有的单个氨基酸。海法以色列理工学院生物医学工程师阿米特 · 梅勒(Amit Meller)的团队则在研究由硅基材料制成的固态纳米孔设备。这种设备可以同时对许多蛋白质分子个体进行高通量分析。“你可以同时看到数万甚至数百万个纳米孔。”梅勒说。
另一种单分子蛋白质测序技术目前还处于概念验证阶段,但商业化很快就可以到来。例如,Quantum-Si就计划在2023年推出这类工具的第一代。梅勒则特别提到,在2022年11月于代尔夫特召开的一次蛋白质测序大会上有一个专门讨论该领域初创企业的小组。“这让我想起了新一代DNA测序工具诞生之前的那段日子。”他说。
马尔科特——他也是得克萨斯奥斯汀一家叫作“埃利斯永”(Erisyon)的蛋白质测序公司的联合创始人——对这一领域信心满满。“现在的问题,并不是这些工具是否有用,” 他说,“而是它们还要多久能到人们的手上。”
詹姆斯 · 韦布空间望远镜
天文学家在2022年就已经正襟危坐了。在长达20余年的设计和建造之后,美国宇航局——以及合作的欧洲空间局与加拿大宇航局——终于在2021年12月25日成功将詹姆斯 · 韦布空间望远镜(JWST)发射升空。之后,全球人民又等待了接近7个月,这架望远镜才抵达预定位置、展开镜面(以及各种工具)、调整姿态,开始第一轮观测。
事实证明,詹姆斯 · 韦布空间望远镜配得上如此耐心的等待。马里兰巴尔的摩空间望远镜科学研究所天文学家、JWST项目科学家马特 · 芒顿(Matt Mountain)就表示,收到的第一批照片已经超越了他最大胆的期待。“这些照片告诉我们,原来天空中没有一处是空的——到处都是星系,”他说,“当然,我们之前就已经通过理论计算知晓了这点,但真正看到这样的画面,还是会大感震撼。”
JWST的设计目标之一就是填补哈勃空间望远镜留下的空白。当然,后者已经为人类拍摄了无数震撼照片,但并非没有盲点,那就是:具有诸多红外波段特征(可见光波段看不到)的古老恒星和星系。要弥补哈勃空间望远镜的这一缺憾,就必须借助极为灵敏的仪器,它得灵敏到能够探测到数十亿光年之外产生的极微弱红外信号。
JWST最后把主镜设计成了一个由18块极为平滑的子镜面构成的主镜。这些子镜面全部展开后,主镜口径能达到6.5米。芒顿表示,这些镜面建造得非常平滑,即便把它们等比例放大成全美国那么大,建造误差导致的厚度差也不会超过几厘米。此外,JWST还配备了最为先进的中红外和近红外探测器。
借助这些功能强大的设备,JWST得以填补哈勃空间望远镜留下的空白,比如捕捉拥有135亿年历史的古老星系的信号。正是这些星系产生了宇宙中第一批氧原子和氖原子。另外,JWST还有我们意想不到的惊喜,例如测量了特定系外行星的大气组成。
全世界的天文学家都排起长队等待JWST的观测时间。英国卡迪夫大学天体物理学家松浦美香子借助JWST开展了两项研究,目标是观察与行星和恒星形成相关的宇宙尘埃的创生与毁灭。美香子表示,相比自己过去使用过的望远镜,JWST的灵敏度和精准度高了不止一个量级。“同样是这些天体,用JWST观察到的画面与此前完全不同——这可太令人惊奇了。”
体积电子显微镜
电子显微镜以其卓越的分辨率而著称,但大多数只能检测样本的表面情况。要想深入研究样本的内部情况,就得把它们切割成极小的薄片,这对生物学家来说往往难以实现。伦敦弗朗西斯 · 克里克研究所电子显微镜学家露西 · 科林森(Lucy Collinson)解释说,用现有显微镜检视单个细胞,要想看到样本的全部情况,需要把它切成200个薄片。“你要是只有一份切片,那就只是在玩统计学游戏。”露西说。
现在,研究人员正努力让电子显微镜的高分辨率扩展到囊括数立方厘米空间的三维结构中。
在此之前,研究人员只能通过二维电子显微镜图像构建三维图像——例如,绘制大脑中的神经元网络——但这需要无比繁杂的样本准备、成像、计算工作,才能把那些二维图像转换成三维。现在,最新的“体积电子显微镜”技术可以极大地简化这个过程。
体积电子显微镜技术有很多优点,但也有很多限制。就拿连续块面成像来说,体积电子显微镜利用金刚石制成的刀刃,相对快速地切入样本,从而能一次处理体积约为1立方毫米的样本。然而,目前通过这项技术拍摄的样本内部照片分辨率不佳,所以构建得到的三维图像也比较模糊。聚焦粒子束扫描电子显微镜也可以把切片切得更薄——所以拍摄到的样本内部照片分辨率更高——因而更适合分析小体积样本。
科林森把体积电子显微镜技术的崛起描述为一场“静悄悄的革命”。研究人员原本更看重电子显微镜技术带来的结果,而非技术本身。然而,目前这种状况正在改变。例如,2021年,电子显微镜细胞器切割计划的研究人员就在《自然》杂志上发表了一系列论文,强调了在绘制细胞内部结构方面的重大进展。“那真是令人印象深刻。”科林森说。
电子显微镜细胞器切割计划使用了定制的高精度聚焦粒子束扫描电子显微镜,从而在保持良好空间分辨率的同时,将单次实验可以处理的样本大小扩大200倍左右。将这种先进设备同深度学习算法结合起来,研究人员就可以得到各种细胞器和其他亚细胞结构的全3D内部图像。
当然,样本的准备工作仍旧很繁琐,甚至有些难以掌握,得到的数据集也十分庞杂。但事实证明,这些努力都是值得的:科林森已经借助体积电子显微镜技术在传染病研究和癌症生物学领域收获了新成果。现在,她正与同事一道,探索构建高分辨率小鼠全脑三维图像的可行性。按照科林森的预测,这项工作耗时可能超过十年,需要数十亿美元的资金,并且产生海量数据。“这项工作的复杂程度很可能相当于绘制第一张人类基因组图谱。”科林森说。
CRISPR全面铺开
基因组编辑工具CRISPR-Cas9作为在基因组目标位点引进限定改变的关键方法,早已无可非议地获得名声,推动基因疗法、疾病建模和其他研究领域的种种突破。然而这项技术的用武之地还是有所限制。如今,科研人员在寻找方法来规避那些限制。
CRISPR编辑由一个短链向导RNA负责协调。短链向导RNA指引一个相关的Cas核酸酶到基因组序列目标处。但这种核酸酶还需要一个附近的原始间隔基相邻基序(PAM)。假如没有PAM,基因编辑很可能会失败。
在位于波士顿的麻省总医院,基因工程师本杰明 · 克莱因斯蒂弗(Benjamin Kleinstiver)使用蛋白质工程,改造常用的、源自化脓性链球菌的Cas9核酸酶,创造出近似无需PAM的Cas变异体。一个Cas变异体所需的PAM只要有三个连续的核苷酸基,并且中间位置的核苷酸为A或G就行。“现在这些核酸酶几乎能读出整个基因组,而常规的CRISPR酶对于基因组的任何位置,读出率都在1%到10%之间。”克莱因斯蒂弗说道。
这样放松后的PAM要求增加了脱靶编辑的概率,但进一步的基因工程改造能改善专一性。作为一个替代方案,克莱因斯蒂弗的团队正在用基因工程改造和测试大量的Cas9变异体,每一种变异体都展现出对于特定PAM序列的高专一性。
还有许多天然出现的Cas变异体有待发现。在自然界,CRISPR-Cas9系统是细菌对抗病毒感染的防御机制,不同的微生物演化出不同的核酸酶,这些核酸酶拥有独特的PAM偏好。意大利特伦托大学的病毒学家安娜 · 切雷塞特(Anna Cereset)和微生物组研究者尼古拉 · 塞加塔(Nicola Segata)梳理了一百多万种微生物基因组,识别了多种多样的Cas9变异体。他们估计,这些变异体加在一起,能瞄准超过人类中98%的已知会引起疾病的突变。
然而,这些变异体中只有少数会在哺乳动物细胞中发挥作用。“我们的想法是测试许多变异体,看一下让那些核酸酶恰当起作用的决定因素是什么。”切雷塞特说。克莱因斯蒂弗说,从这些天然核酸酶“池”中获得的洞见,再加上高通量蛋白质工程改造方面的努力,“我认为我们最终会得到十分完整的编辑器工具箱,使得我们能编辑任何一个我们想要编辑的核苷酸基。”
高精度的放射性碳定年法
对于加拿大纽芬兰的兰塞奥兹牧草地出土木材进行精确的放射性碳定年测量,揭示了维京人于1021年在这处遗址伐倒一棵树
去年,考古学家利用放射性碳定年法的进步,确定维京人探索者初次抵达美洲的准确年份——甚至准确到季节。荷兰格罗宁根大学的同位素分析专家迈克尔 · 迪伊(Michael Dee)与博士后玛戈 · 库伊特姆斯(Margot Kuitems)带领的一支团队用加拿大纽芬兰北岸一处聚落出土的伐倒木材碎片做分析,确定这些树很可能是在公元1021年被人伐倒的,并且大概是在春季。
从1940年代起,科学家一直在对有机人工制品使用放射性碳定年法来缩小历史事件的日期范围。他们通过测量碳-14同位素的痕量来定年。碳-14的形成是宇宙射线与地球大气层相互作用的结果,在千百年里缓慢衰变。但这项技术的精确度通常只够把年份推定到20年左右的范围内。
情况在2012年发生变化,由日本名古屋大学三宅芙沙(Fusa Miyake)带领的研究团队指出,他们可以将一棵日本柳杉年轮中碳-14水平的一个尖峰定年至公元774年至775年之间。随后的研究不仅证实这一尖峰出现在全球各地这个时期的木材样本中,另外还识别出至少五个其他尖峰,最早能追溯到公元前7176年。研究者已经将这些尖峰与太阳风暴活动关联起来,不过这种假说仍然处在探索中。
不管背后的原因是什么,这些“三宅事件”允许研究者能精确地确定木质人工制品的诞生年份,方法是先侦测一个特定的三宅事件,再清点自那之后形成的年轮数量。库伊特姆斯说,基于最外侧年轮的宽度,研究者甚至能确定某棵树是在哪个季节被砍伐的。
考古学家目前在将这个方法应用到新石器时代聚落和火山爆发遗址,而迪伊希望用它来研究中部美洲的玛雅帝国。迪伊乐观地认为,在接下来的十年左右,“我们会掌握许多古代文明的绝对记录,精确到年份,而且我们将能在精细的尺度上探讨它们的历史发展。”
至于三宅芙沙,她对历史“码尺”的搜寻仍在继续。“我们目前在过往一万年中搜寻其他可与774—775年事件相比的碳-14尖峰。”她说道。
单细胞代谢物组学
代谢物组学是对脂质、碳水化合物与其他驱动细胞的小分子的研究,最初是一套描绘一类细胞或组织中代谢产物特征的方法,但如今转变至单细胞层面。科学家能利用这样细胞层面的数据来解开大量貌似一模一样的细胞中存在的功能复杂性。然而,研究的转变提出令人畏缩的艰难挑战。
代谢物组包含大量具有不同化学性质的分子。欧洲分子生物学实验室海德堡总部的代谢物组学研究者西奥多 · 亚历山德罗夫(Theodore Alexandrov)说,一些分子的存在十分短暂,拥有亚秒级的替换率。而且它们很难探测到:尽管单细胞RNA定序能捕捉到细胞或有机体(转录组)所有RNA分子的将近一半,但大多数代谢分析只涵盖细胞代谢物中的极小一部分。丧失的信息可能包含关键的生物学见解。
“代谢物组实际上是细胞的活跃部分。”伊利诺伊大学厄巴纳-尚佩恩分校的分析化学家乔纳森 · 斯威德勒(Jonathan Sweedler)说道,“当你罹患疾病,假如你想要了解细胞状态,你会想要看一下代谢物。”
许多代谢物组实验室以分离的细胞做研究,他们将这些细胞困于毛细管中,用质谱法进行个别分析。相比之下,成像质谱法捕捉细胞代谢物生产在样本不同位点如何变化的空间信息。譬如说,研究者使用一种名叫基质辅助激光解吸/电离(MALDI)的技术,让激光光束扫过特别处理过的组织切片,随后对释放出的代谢物用质谱法进行分析。这种方法也能捕捉到样本产生代谢物的位点的空间坐标。
理论上,两种方法都能量化分析数千个细胞中的数百种化合物,但要达成该目标,一般需要顶尖的定制硬件设备,花费在100万美元范围内,斯威德勒说。
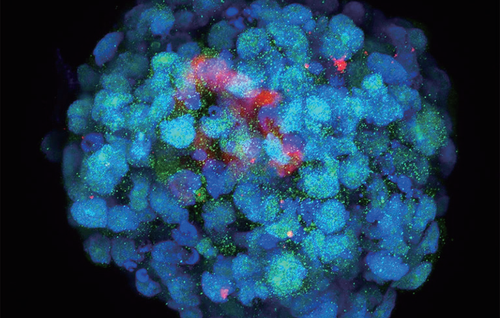
这个胚状体模型显示天然八细胞期胚胎中细胞的关键特征
现在,研究者在将这项技术以更低的成本推广普及。2021年,亚历山德罗夫的团队介绍了一个开源软件工具SpaceM,它使用光学显微镜成像数据,使得用标准商用质谱仪对培养的细胞之代谢物组作空间剖析成为可能。“我们有点像在数据分析的部分上做了吃力困难的工作。”他说。
亚历山德罗夫的团队已经使用SpaceM来剖析数万个人类细胞和小鼠细胞的数百种代谢物,利用标准单细胞转录方法来将那些细胞分为不同类别。亚历山德罗夫说,他对后一个方面特别感兴趣,考虑汇编“代谢物组图集”——类似于那些为转录组制定的图集——来加速这个领域的研究进展。他说:“这肯定是前沿领域,而且会是一个重要的使能者。”
体外胚胎模型
就小鼠和人类而言,从受精卵到完全成形的胚胎的历程在细胞层面上已经被详细地描绘出来。然而,我们对驱动这个过程早期阶段的分子机械依然了解甚少。如今,胚状体模型中的一系列活动正在帮助我们填补这些知识空缺,让研究者更清楚地观察那些能决定胎儿发育成功与否的早期关键事件。
一些最为复杂的模型来自加州理工学院和剑桥大学的发育生物学家玛格达莱娜 · 策尼卡-格茨(Magdalena Zernicka-Goetz)的实验室。2022年,她与团队示范了他们能够完全从胚胎干细胞生成着床期的小鼠胚胎。
和所有多能干细胞类似,胚胎干细胞能形成任何细胞或组织类型——但它们需要与两类胚外细胞的密切相互作用,才能完成正常的胚胎发育。策尼卡-格茨团队学习如何诱导胚胎干细胞来形成那些胚外细胞,表明这些细胞能与胚胎干细胞一起培养,产生的胚胎模型能成熟到此前以体外方式未曾达到的阶段。策尼卡-格茨说:“它和你想象中的胚胎模型一样。它发育出脑袋和心脏,而且心脏还会跳动。”她的团队能利用该模型来揭示,个体基因的变更能够如何让正常的胚胎发育偏离正轨。
在中国科学院广州生物医药与健康研究院,干细胞生物学家米格尔 · 埃斯特万(Miguel Esteban)与同事选择另一个研究方向:他们将人类干细胞重编程,建立胚胎发育最早期阶段的模型。
“我们从这样甚至也许能制造出受精卵的想法着手。”埃斯特万说。团队并未实际达成目标,但他们确定了一种推动干细胞回到某个类似人类胚胎八细胞期的阶段的培养策略。这是胚胎发育研究中的至关重要的里程碑,与基因表达的重大转变有关。正是有了基因表达的重大转变,才最终产生独特的胚胎与胚外细胞谱系。
尽管尚不完美,埃斯特万的模型显示天然八细胞期胚胎中细胞的关键特征,凸显人类胚胎和小鼠胚胎开始向八细胞期过渡时在方式上的重要差异。“我们看到一个在小鼠中甚至没有被表达的转录因子调节了整个转变过程。”埃斯特万说。
这些模型有助于研究人员弄清仅仅一些细胞是如何产生极其复杂的脊椎动物躯体的。
在许多国家,人类胚胎的研究受到限制,有着所谓的“14天准则”,即在体外培养人类胚胎的时间不得超过14天。但14天已经足够,研究人员能在上述限制条件下能进行研究。埃斯特万说,非人类的灵长类动物模型提供一种可能的替代选择。策尼卡-格茨说,她的小鼠胚胎研究策略也能生成发育最长达到第12天的人类胚胎。“我们仍然有许多对于那个发育阶段的问题要问。”她说道。
资料来源 Nature