导读
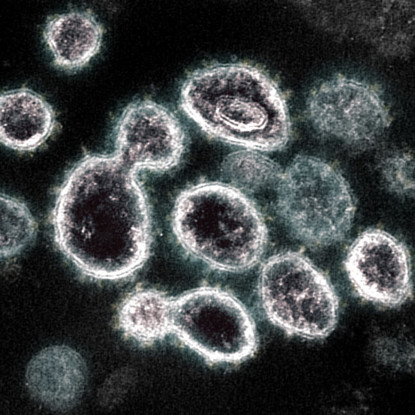
2025年诺贝尔化学奖已正式揭晓,三位科学家凭借在 “金属-有机框架(MOF)开发领域的奠基性工作”斩获该奖项。作为一类极具应用潜力的功能材料,MOF的核心特征是其内部存在大量规则空腔,可允许气体及其他化学物质的分子自由进出并实现吸附与释放。
这类材料的研发思路常以“乐高积木”作类比——金属离子作为核心“积木块”,通过配位键与有机配体这一“连接件”进行精准组装,形成多样的三维框架结构,这种可设计、可组合的特性也让“乐高积木”的玩法被上升为材料领域的“构建哲学”。
事实上,这一“构建哲学”已在多领域研究中得到延伸应用。西南科技大学李国强领衔的团队便将其融入微流控芯片研究,相关成果近期已刊载于《先进材料》(Advanced Materials)期刊。
自然界的许多生物演化了独特的结构以实现对微小液滴的操控。滨鸟鸟喙的往复开合运动可以将液滴反重力地运输至嘴部。一些蜥蜴则进化出了具有微小开放通道的皮肤,蜥蜴只需要将足支伸进水里,仅依靠皮肤上的毛细系统,就能汲取到所需要的水分,而不需要低头喝水,确保持续警惕周围的环境。
而人类对液滴的操控与利用同人类本身的历史一样悠久,早在17世纪,科学家们便开始探索毛细现象和微小通道中的流体行为,为微流控奠定了初步的理论基础。如今,微流控技术已发展成为一门高度交叉的前沿学科,它通过设计精密的微通道结构,能够在极小尺度上操控纳升至皮升级别的流体,实现对细胞、颗粒、液滴的精准输运、分离、混合与分析。这一特性使其在单细胞分析、器官芯片、即时检测等领域展现出巨大潜力。
然而,尽管在基础研究和技术开发方面已取得显著进展,但“精准移取微量试剂”、“多样化检测需求”、“一步错步步错”的微流控器件问题仍然是业界难题。正因如此,发展高集成度、可编程化和更好生物相容性的微流控平台已成为一个至关重要的研究方向。
开放通道微流控器件面临的挑战
无与伦比的易访问性与操作简便性是开放通道微流控设备最直接、最突出的优点。
研究者可以随时、直接使用移液枪、探针或显微操作仪接触到通道内的样品,进行添加、移除、混合或刺激等操作,而无需通过复杂的进口和阀门。无需复杂的泵送系统来驱替通道内的空气,只需用移液枪将液滴直接加在通道入口或特定位置即可,极大地简化了上样流程。
同时芯片易于清洗和重复使用,通道是开放的,没有永久性键合,因此清洗非常简单彻底,只需擦拭或冲洗,避免了封闭通道中常见的堵塞和残留问题,芯片可重复使用率更高。
开放通道微流控器件进行CO2的吸收
然而这一类器件通常是结构固定的,难以进行相互组装配合,其路径形状、运动行为受到严重制约。因此在实际应用的过程中仍然有着不同程度的局限性。
模块化微流控:从固定芯片到功能乐高的革命性演进
模块化微流控(Modular Microfluidics)是微流控技术领域一次深刻的范式转变。它摒弃了传统“一 chip 一用”的固定、封闭设计思路,转而借鉴“乐高积木”的构建哲学,将复杂的微流控系统分解为一系列具有独立功能、可自由拼接和组合的标准单元模块。
乐高拼图概念微流控芯片
这些功能模块通常包括:微泵、微阀、混合器、反应器、检测单元、细胞培养室等。研究者可以根据特定的实验需求,像搭积木一样,通过标准化接口(如物理卡扣、磁性连接或流体插头)将这些模块快速组装成一个完整、可定制的微流控系统。
其核心优势在于极高的灵活性与可重构性。一个模块化平台无需重新设计、加工整个芯片,即可轻松实现功能切换或流程优化,极大地加速了实验迭代和原型开发速度。同时,它显著降低了使用门槛和成本——某个单一模块的损坏只需更换该单元,而非抛弃整个昂贵芯片,这使得在资源有限的实验室或课堂教育中普及微流控技术成为可能。
此外,模块化微流控极大地促进了跨学科合作。生物学家、化学家或临床医生无需精通微加工技术,也能通过组合预制的功能模块,自主构建满足其专业需求的个性化实验平台。
目前,模块化微流控正成为即时诊断(POCT)、合成生物学、器官芯片(Organ-on-a-Chip)和空间组学等前沿领域的强大助推器。它不仅是技术上的创新,更代表了一种开放、协作、可扩展的新理念,正在重塑我们操控微观流体的方式,推动生命科学研究和医疗应用走向一个更高效、更灵活的未来。
1 方向性模块化微流控
方向性是微流控技术中一个专注于操控流体定向流动的重要分支,其核心目标是通过设计芯片自身的微观结构或表面特性,实现流体在特定方向上的自主、可控输运,从而减少对外部泵阀系统的依赖。这一领域的关键在于创造流动阻力的各向异性,使流体在不同方向上遇到不同的阻力。主要实现策略包括利用表面化学不对称性(如在通道内制造亲疏水性梯度,驱动流体从疏水区域流向亲水区域)、几何结构不对称性(如采用楔形通道、沟槽结构或特斯拉阀等设计,利用毛细力差引导定向流动)以及外场驱动不对称性(如通过表面声波或不对称电极产生定向驱动力)。这些方法往往结合使用,形成联合驱动策略,以增强定向输运效果。
方向性微流控在多个领域展现出重要应用价值。
· 在诊断检测中,它使自驱动试纸(如高级侧向层析试纸)能够依靠毛细作用实现样品的定向流动与检测;
· 在仿生系统中,它可模拟植物的水分输运机制,为长期细胞培养提供自驱动的营养供应;
· 在混合与分离过程中,不对称结构可驱动流体产生定向涡流,实现高效混合与分离;
· 在可穿戴设备中,定向微流道能够实现汗液的持续收集与输运,助力实时健康监测。
总体而言,方向性微流控不仅推动了微流控器件向更简化、可靠和节能的方向发展,也为智能仿生系统与即时诊断技术的创新提供了关键支持。
具有方向性的概念微流控
2 可编辑微流控
可编辑则是微流控技术领域一个前沿而富有前景的方向,它赋予了微流控芯片动态可重构的能力,使研究人员能够像在计算机上编辑文档一样,在同一个硬件平台上通过软件指令或简单操作,灵活、实时地修改流道功能、连接路径和实验流程,而无需更换芯片或其物理结构。它超越了模块化微流控的“硬件拼接”理念,致力于实现更高程度的软件定义流路和时空动态控制。
实现可编辑性的技术路径多样,比如数字微流控,通过在二维电极阵列上施加不同的电压序列,实现对离散液滴的精确操控(如移动、分裂、合并),其流路功能完全由软件定义的电极激活模式所决定,具有极高的灵活性。除此之外还有磁控微流控,将掺有磁性颗粒的智能材料(如磁流体、磁性水凝胶)作为“活动部件”,通过外部磁场的变化来动态调节阀门的开闭、泵的运作甚至流道的形状。
可编辑微流控的应用价值巨大。
在细胞研究中,它允许在一块芯片上先后运行截然不同的实验。例如先进行动态浓度梯度培养以筛选药物,随后立即重构流路,将特定响应细胞进行分离和收集,极大提升了研究效率和单芯片的利用率。
在合成化学领域,它像一个可编程的微型化工厂,研究人员可通过软件快速尝试不同的反应物混合顺序、反应停留时间等参数,加速反应条件的优化过程。
在器官芯片领域,可编辑性意味着能够动态模拟生理或病理条件下血流的变化,例如通过软件控制瞬间“阻塞”某一通道来模拟心肌梗塞,以研究缺血对心脏组织的影响。
可编辑的概念微流控
3 飞秒激光加工:为微流控器件制造注入“精准”与“自由”
在模块化微流控器件的制造过程中,飞秒激光加工技术正扮演着一位如同拥有“神之手”的工匠角色。其独特的“超快超强”特性,即以极高的峰值功率在百万亿分之一秒的极短时间内与材料相互作用,带来了“冷加工”效应,使得它能够以前所未有的精度、几乎无材料限制的方式,实现复杂的三维微纳结构制造,极大地推动了模块化微流控的发展。
飞秒激光焦点可以精确定位于透明材料(如玻璃、石英、PDMS)内部的任意一点,通过非线性吸收效应,只改变焦点区域的物质性质,从而实现在材料内部“直写”三维流道、空腔和连接孔,无需层层键合,避免了接口和死体积问题。从聚合物、玻璃到陶瓷甚至金属,飞秒激光几乎可以在任何材料上实现高质量微加工。这为制造具有不同功能需求(如生物相容性、光学性能、机械强度)的模块提供了极大的材料选择自由度。
同时飞秒激光的加工精度可达亚微米级别,并能获得异常光滑的通道内壁(粗糙度<100 nm),这显著减少了流体流动的阻力,并最大程度降低了生物分子吸附和细胞粘附的风险,对于细胞培养和敏感检测模块至关重要。
维也纳理工大学与庆应义塾大学的研究人员已经可以直接在生物相容性水凝胶(如GelMA)内部,用飞秒激光“雕刻”出高度仿真的3D毛细血管网络或肝小叶结构。然后将这个包含精细内部结构的凝胶模块作为一个整体,与其他流体控制、传感模块进行集成,构建出高度仿生的模块化器官芯片系统。
肝小叶结构示意图(左)与芯片上血管化肝小叶培养9天后的三维视图(右)
模块化微流控器件产业化与展望
模块化微流控器件的应用正以前所未有的灵活性重塑多个领域的研究范式。通过将复杂功能分解为标准化的可互换模块,研究人员能够像搭建乐高积木一样快速构建定制化实验平台。
在生物医学工程领域,模块化微流控展现出巨大潜力。
哈佛大学Wyss研究所开发的“器官芯片”系统,通过组合不同的器官模块(如肠、肝、肾模块),成功模拟了人体内药物代谢的完整过程。于2010年在《科学》(Science)杂志发表了世界上首个成功的人体器官芯片模型——一个模拟肺泡,也就是肺部气囊的器官芯片。
通过这个芯片,可实时模拟人类肺部的结构以及工作机制:吸气肺部舒张,血液从吸入的空气中提取身体所需的氧气;呼气肺部挤压,排出二氧化碳。这整个过程都可以在一块小小芯片中完整还原。
器官微流控芯片
唐纳德·英格伯(Donald E. Ingber)在华展示“器官芯片”
药物筛选与合成领域同样也受益匪浅。
诺华制药公司与麻省理工学院合作开发的模块化微流控平台,允许研究人员通过组合不同的反应器模块和混合器模块,快速构建多达数百个并行反应的微反应系统。每个模块包含独立的微阀和传感器,可实时监测反应条件,显著提高了先导化合物优化的效率。
然而现有的模块化研究仍然面临复杂如制备复杂、接口标准化以及液体输送方向性等工程挑战。
为了解决这些问题,西南科技大学团队结合自然界所获取的楔形接口灵感,结合飞秒激光的高精度、广材料加工特性,开创性的研发了一种灵活可编程的微流控器件(MFUs),技术核心是利用楔形接口的不对称拉普拉斯力使液体实现了单向流动效果,同时多种规范化的单元使得液体路径灵活多样,即插即用。
所开发的器件具备到单通道100 mm/s、组装路径30 mm/sd的液体传输速度,在传输过程中的损失率低于5%,远优于传统微流控芯片的10%~15%,尤其适合珍贵样品(如生物试剂、微量污染物样本)的操控;
宽温域:从室温到60℃的环境下均能稳定工作,覆盖了多数化学、生物实验的温度需求;
高容错:刚性的单元在组装后展现出了±5°的可变形性——即使路径轻微偏移,液桥仍能稳定形成,避免了传统刚性通道“一歪就漏”的问题。
这项技术的潜在应用场景正逐步清晰。在西南科技大学的实验室里,科研团队已演示了多项功能:
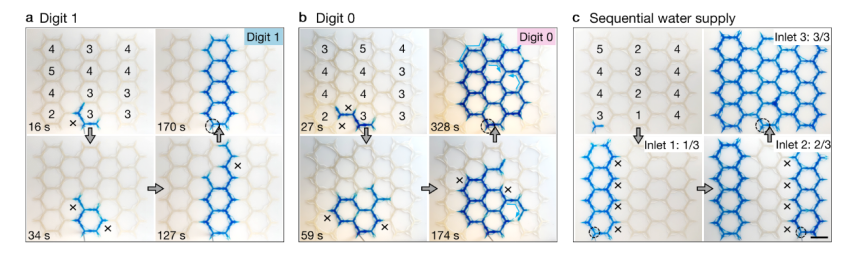
分步液体输送:组装成多边形路径的MFUs,能从3个不同入口依次向中心收集单元输送液体,精准控制加样顺序,可用于酶联免疫检测中的分步试剂添加;
可切换分流器:通过更换单元,160微升的液体可被均匀分成3-8等份,无需称重设备,适用于环境监测中的多平行样制备;
微型反应平台:在组装的MFUs阵列上,成功完成了盐酸电解制氯、亚硝酸钠与对氨基苯磺酸的显色反应,以及盐酸普鲁卡因的电位滴定——整个过程无需大型仪器,像“芯片上的微型实验室”,未来可集成到便携式检测设备中,用于野外医疗或食品安全快速检测。
“相比传统技术,MFUs无需外部动力、可灵活重构,还能实现液体的自发单向传输,这为‘绿色化学’和‘精准检测’提供了新工具”。团队研究成果已发表在国际期刊《先进材料》(Advanced Materials,是材料科学领域具有重要影响力的学术期刊,2023年影响因子27.4)上。
MFUs实现顺序液体流动路径
MFUs可编程性液体流动路径
结 语
展望未来,模块化微流控的发展将围绕以下几个关键方向:
首先是接口的标准化,制定全球统一的微流体接口标准是推动技术普及和生态发展的基石;
其次是更高层次的集成化,将驱动、控制、传感等功能更深度地集成到模块或底板中,提升系统性能和便携性;
再者是与先进制造技术(高精度3D打印、激光加工等)的结合,这将助力制造出更具复杂结构和多功能集成的三维模块;
最后是与人工智能的结合,通过AI辅助的系统设计和智能控制,实现模块化微流控系统的自我优化和自动化操作。
尽管面临接口密封性、死体积控制等工程挑战,模块化微流控所赋予的无限灵活性、可重构性以及降低的技术门槛,正在使其成为生命科学、临床诊断、合成化学等领域不可或缺的创新工具,未来有望在个性化医疗、太空生物实验、可穿戴设备等前沿领域开辟全新的应用范式。
END