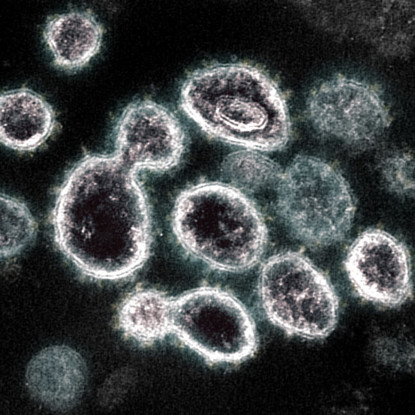
长久以来,医学界应对慢性肾脏问题的手段十分匮乏。等到病患发展至肾衰竭时,透析和器官移植成了唯二的无奈选择。
不过最近几年,诸多慢性肾脏病成功治疗案例让我们意识到,通过用药保护肾功能甚至逆转损伤是一条能走通的路径。以司美格鲁肽为代表的GLP-1类药物在临床试验中展现了令人惊叹的护肾效果。
有专家由此感慨,我们好像走进了治疗慢性肾脏病的黄金时代。
慢性肾脏病影响着全世界大约7亿人口,据估算,其中发展至第五期,即肾衰竭阶段的患者在全球30岁以上人群中占比0.21%,第四期的则占比0.51%。然而长久以来,慢性肾脏病的治疗手段极有限,目前仍以透析和肾脏移植这两项“大招”为主。
业内人士常引用“久病成医”代表人物朱莉 · 霍根(Jullie Hoggan)的案例。1998年确诊多囊肾病的她收到医生无奈回复:“等你二十年后肾脏衰竭了再回来治疗。”肾功能持续恶化二十多年后,已成为器官移植领域创业者的霍根在2020年完成了肾脏移植手术。
漫长等待和排异反应是老生常谈的器官移植难点。而且病人除了要终身忍受免疫抑制剂的副作用,其因心脏病或中风而死亡的风险也极高。此外,移植肾脏正常运转的周期只有12~20年。
至于透析,除了价格高昂,除了要求病人必须每周接受数次长达数小时的治疗,它还会给身体造成严重负担,导致疲劳、痉挛、恶心、睡眠障碍、思维混乱、电解质失衡以及感染风险等副作用。在接受透析的患者中,仅有35%的人能存活超过5年。
广大病患与全行业都期盼出现某种真正的慢性肾病疗法。不必换掉脏器,不必丧失生活质量,只需打针吃药,就能安全地阻止病症发展甚至逆转肾脏损伤,比如将第五期患者那衰竭的肾逆转至第三期的功能状态。
过去十年,许多科学家都积极开发针对各类慢性肾脏病的各种新疗法。如今回首与展望,我们发现,以司美格鲁肽为代表的2型糖尿病药物兼减肥药竟也能跨界保人肾,勾勒出一条通过吃药逆转功能衰退、治愈慢性肾病的路线。
减肥药效果太好
所以提前终止试验
在今年11月的美国肾脏病学会年会上,来自华盛顿大学的肾病专家凯瑟琳 · 塔特尔(Katherine Tuttle)展示临床数据,介绍了通过GLP-1受体激动剂有效治疗慢性肾脏病的新进展。
GLP-1全名“胰高血糖素样肽-1”,是一种由肠道L细胞分泌的血糖调节激素,能通过调动胰岛素分泌来降低血糖,此外也具有延缓胃排空、抑制食欲的作用。GLP-1受体激动剂则是模拟GLP-1的人工合成药物,主要用于治疗2型糖尿病和肥胖症。
司美格鲁肽(商品名Ozempic)无疑是GLP-1药物的杰出代表。而在治疗肾脏损伤方面,它同样展现奇效,不仅显著稳定病情,甚至还逆转了部分病例的肾脏损伤。这些改善包括肾脏内部炎症和瘢痕的减轻,以及整体功能的提升。
2024年发表的一项3期临床试验结果显示,司美格鲁肽能高效延阻糖尿病性慢性肾脏病患者发展至终末期肾衰竭,并降低其因心血管疾病死亡的风险。鉴于司美格鲁肽治疗组遭遇肾衰竭或死亡的风险远低于对照组,塔特尔团队认为继续让对照组病人服用安慰剂不合乎伦理,故提前终止了试验。
糖尿病性慢性肾脏病是慢性肾脏病中最常见的类型,影响着59%的肾衰竭患者。
目前塔特尔与同事正开展随机双盲安慰剂对照试验REMODEL,力求从分子层面揭示司美格鲁肽改善肾功能的具体机制。团队根据已有分析结果判断,司美格鲁肽能以直接与间接的多种途径带来肾脏健康收益。
一方面,它可显著改善多重代谢因素,包括降低糖化血红蛋白水平、减轻体重、控制血压和调节血脂谱等,从而为肾脏减负,间接地延缓肾病进展。
另一方面,司美格鲁肽对肾脏的直接保护效果似乎更突出,保护机制包括抗炎抗纤维化、降低肾脏脂肪、促进尿钠排出、抑制肾素-血管紧张素-醛固酮系统、改善血流动力学等。
从距离肾衰竭一步之遥
到四十年不曾出现的疗效
Ozempic已获批用于治疗糖尿病性慢性肾脏病。关于它能否改善非糖尿病性慢性肾脏病,有相关试验正在进行中。初步证据显示前景可期:与司美格鲁肽争雄的另一款GLP-1受体激动剂替尔泊肽(商品名Mounjaro),已为非糖尿病性慢性肾脏病带来显著疗效。
现年33岁的尼古拉斯 · 帕拉西奥斯(Nicolas Palacios)在2020年确诊非糖尿病性肾病第四期,距离肾衰竭一步之遥。他选择加入试验,服用替尔泊肽。结果这些药物遏制了肾病快速恶化的趋势,将肾功能从衰竭边缘挽回。
如今的他被归入第三期肾脏病。这意味着,只要病情不再恶化,他可以过上长寿且健康的生活,远离透析和移植。
塔特尔感叹道:“在我四十年职业生涯里,还从未见有病人出现像帕拉西奥斯那样的好转。更关键的是,帕拉西奥斯并非孤例。”
在9月份欧洲糖尿病研究协会年会上,SURPASS-CVOT研究公布的最新数据显示:替尔泊肽相较活性对照药物(度拉糖肽),显著延缓了肾小球滤过率的下降,拉低了尿白蛋白/肌酐比值,减小了复合肾脏结局事件的发生风险。
肾小球滤过率是衡量肾脏过滤功能的核心指标,其下降速度延缓表明肾功能受到保护;
尿白蛋白/肌酐比值是评估肾脏血管损伤的关键指标,反映肾小球滤过膜对蛋白质的通透性,其降低提示肾脏结构损伤减轻;
复合肾脏结局事件包括肾衰竭、肾病相关死亡等。
护肾新药浪潮方兴未艾
联合用药可以最大化疗效
研究慢性肾病新疗法的浪潮始于2019年,当时有试验表明,一类名为SGLT2抑制剂的糖尿病药物帮助糖尿病性慢性肾脏病患者缓解了病症。
SGLT2抑制剂能阻止肾脏重新吸收葡萄糖,从而降低血糖。至于它为何对肾脏健康如此有益,目前仍不确定其中机制。德国亚琛工业大学研究员拉斐尔 · 克拉曼(Rafael Kramann)推测:
原因很可能是肾近端小管上皮细胞需要消耗巨大能量用以重吸收葡萄糖,而SGLT2抑制剂阻止肾脏将能量用于葡萄糖重吸收,因此肾脏有更多能量来应对损伤,从而更好地适应不利局面。
由于SGLT2抑制剂护肾功效强大,能显著预防肾衰竭以及因心脏病发作或中风死亡的风险,许多相关试验都选择提前终止。后续研究表明,SGLT2抑制剂对非糖尿病性慢性肾脏病患者同样有益。
除SGLT2抑制剂和GLP-1受体激动剂外,还有另外两类药物获批用于治疗糖尿病性慢性肾脏病。这些药物各有各的作用机制,联合用药可令疗效加倍。
临床实证告诉我们,联合使用全部四类获批用于糖尿病性慢性肾脏病的药物,足以令患者肾衰竭风险降低58%。其中挑战则在于如何为个体患者制定联合用药方案。
未来创新源源不断
相比糖尿病性慢性肾脏病,目前非糖尿病性肾病的治疗选项更受限,但局面正迅速改变。
原发性肾小球肾炎是导致肾衰竭的最常见病因,IgA肾病则是原发性肾小球肾炎中最常见的类型。近年来有三种相关新疗法获批,它们能选择性靶向导致损伤的特定细胞类型,从而有效阻断疾病进展,帮助患者缓解病情。
当前有数百项针对不同类型肾脏疾病的临床试验正在推进中,其中仅针对IgA肾病的临床试验就有70项。
创新之所以如此活跃,原因在于学界此前设计出了更快速而精确的新策略用以测量IgA肾病造成的肾功能衰退程度,使得临床试验能更高效地在数年内完成,要知道传统试验可能持续数十年,耗资数亿美元。
我们或许已进入了研究和治疗慢性肾脏病的黄金时代。
资料来源:
Scientists found a way to reverse kidney damage—is a cure next?
Effects of Semaglutide on Chronic Kidney Disease in Patients with Type 2 Diabetes
REMODELing mechanistic trials for kidney disease: a multimodal, tissue-centered approach to understand the renal mechanism of action of semaglutide
知其所以然!REMODEL研究重磅公布,司美格鲁肽肾脏获益机制揭秘
The Evolution of Renal Status in Participants on Tirzepatide Versus Dulaglutide of the SURPASS-CVOT
EASD 2025|替尔泊肽 SURPASS-CVOT 研究重磅揭晓:头对头确证心血管获益,全方位改善糖尿病结局
END