内容提要
1. 从非人灵长类研究同性性行为 | 灵长类动物普遍存在同性性行为,这似乎利于其在环境压力下巩固社会联系。有趣的是,物种内的社会系统和等级制度越复杂,同性性行为往往越普遍。
2. 直立行走第一古人类 | 非洲大陆的沙赫人似乎人猿难辨。关于其股骨等骨骼化石的最新分析表明它具备显著的直立行走特征。
3. CAR-T疗法新用途 | 科学家发现CAR-T疗法可使老年小鼠的肠道内膜恢复年轻状态,这为人类肠道修复带来了新希望,也开拓了CAR-T疗法的新功效。
生存环境越是恶劣,灵长类动物越容易喜欢同性
以生物演化视角看,同性性行为的意义是否在于缓和群体内的紧张关系或促进社会联结?过往的一些研究给出了肯定答案。
而在《自然-生态与进化》(Nature Ecology & Evolution)的1月最新文章中,科学家提供了更加违反直觉的洞见——
面对更干燥的栖息环境、更稀缺的资源以及更高捕食风险的物种,更有可能出现同性性行为。
除此之外,在寿命较长的以及雌雄体型差异较大的物种中,同性性行为更为常见;两性体型差异显著的物种往往存在竞争激烈的大型社会群体。
另一方面,当社会系统和等级制度趋于复杂,同性性行为也将越发普遍。
论文作者通过分析非人灵长类动物同性性行为的记录,证实该现象普遍存在于以黑猩猩、巴巴利猕猴和山地大猩猩为代表的共计59个灵长类物种。如此广泛分布意味着——
该行为模式可能源于灵长类家族树中某处极为远古的进化源头;或者,它是多次独立演化的结果。
主导该项工作的克洛伊 · 考克肖尔(Chloe Coxshall)表示:“过往研究表明同性性行为在很大程度上由遗传因素决定,其实常被忽视的环境作用也施加着影响。”
另一位作者文森特 · 萨沃莱宁(Vincent Savolainen)指出:同性性行为看起来是种亲和性的行为,可增强个体间的社会联系,缓解紧张与对抗,帮助物种应对环境挑战。“不同影响因素似乎相互关联。环境条件塑造物种的生命史特征,进而影响其社会体系。”
作者团队还认为,对现代人而言,驱动同性性行为模式的动力可能并非食物匮乏或严格的社会等级制度,而是社会生活压力。当前年轻一代展现出更开放、流动的性取向,同时也面临心理健康方面的挑战。
资料来源:Primates’ same-sex sexual behaviour ‘may reinforce bonds amid environmental stress’
最早实现直立行走的祖先真是700万年前的乍得沙赫人吗?
在人类起源故事的开篇阶段,有位暂不知名的祖先完成了从四肢触地向前行到双腿直立阔步走的重大转变,就此走向人的定义。
发现这位祖先的遗骸几乎是不可能完成的任务,但科学家认为,我们已经明确了一种最接近它的“四驱转两驱”人士,那就是生活于700万年前的乍得沙赫人(Sahelanthropus tchadensis)。
2001年,古生物学家米歇尔 · 布鲁内(Michel Brunet)等人从非洲乍得的朱拉卜沙漠发现了少量乍得沙赫人化石,包括头骨、牙齿和下颌骨。化石呈现不同于大型猿类的形态特征;布鲁内认为其头骨与脊柱的连接方式表明乍得沙赫人很可能具备直立行走能力,并宣称这是最古老人族成员,是“全人类的祖先”。
对此学界不乏反对之声,毕竟在缺少更多化石证据,尤其是下半身骨骼的情况下,我们难以确定其移动方式。虽然后来又发掘出乍得沙赫人的部分股骨和前臂骨,但围绕其是否直立行走的争议犹在。
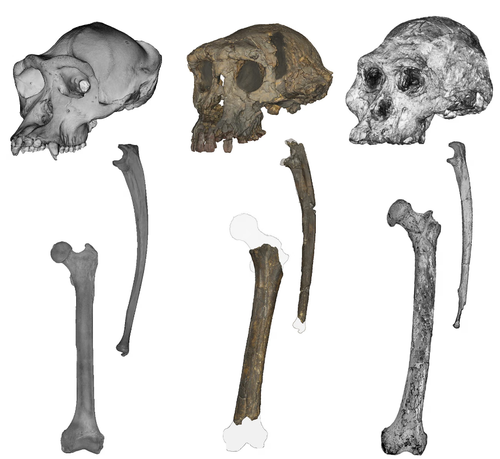
2026年1月,纽约大学学者斯科特 · 威廉姆斯(Scott Williams)与同事于《科学进展》(Science Advance)发表最新分析成果,确证了沙赫人的直立行走能力。团队采用新技术重新审视股骨和前臂骨化石,就尺寸、比例和三维轮廓等特征将其与已知其他人族及猿类骨骼作比对,最终发现了一处特殊结构:沙赫人大腿骨上有个名为“股骨结节”(femoral tubercle)的凸起。
从左至右分别为黑猩猩、沙赫人与南方古猿的颅骨、尺骨及股骨标本
威廉姆斯解释称:股骨结节是人体内最强大韧带的关键附着点。坐下时,此韧带处于松弛状态;站立时,它会绷紧。它能防止行走过程中躯干向后倒或左右摇晃,是适应双足行走的重要特征。“据我所知,学界此前仅在直立行走的古人类化石上发现这种结构。”
此外,这项分析还揭示了其他科研团队过往报道的一些直立行走特征,例如“股骨的自然扭转有助于腿部前伸”,又如“臀肌能保持髋部稳定以辅助站立、行走和奔跑”。
威廉姆斯认为,在人与猿的分化关键阶段,有过一种既具备猿类特征又能在地上直立行走(即便并非始终如此)的物种。“最早的人族动物逐渐适应着地面双足行走,不过仍通过树上作业实现觅食与避险。”
资料来源:Fresh bone analysis makes case for earliest ‘ancestor of humankind’, but doubts remain
CAR-T细胞疗法逆转肠道衰老
随着年龄增长,人体肠道内膜细胞的自我更新能力会逐渐衰退。这种再生能力对于维持高水平的免疫功能有着重要意义。
衰老细胞会随机体的年龄增长而不断累积数量;其分裂能力虽已丧失,但仍保持代谢活性,能释放促进炎症、加速衰老的化学物质。
美国冷泉港实验室学者塞米尔 · 贝亚兹(Semir Beyaz)与同事观察发现,年轻有活力的肠道内壁理应每三到五天完成一次更新,而在衰老后,其干细胞变得活力不足、更新放缓,这就导致肠道功能衰退。
于是贝亚兹设想:倘若针对一只老年动物的肠道内壁,清除其中“失去活力”的衰老细胞,那肠道整体的干细胞再生能力与健康状态,是不是就显著改善了?
为验证假设,冷泉港团队尝试用经过基因改造的T细胞,即所谓的CAR-T疗法,来逆转肠道内膜细胞的衰老过程、修复肠道功能。
他们为老年小鼠构建了独特的CAR-T细胞——它们能识别衰老细胞表面富集的uPAR蛋白并清除细胞。
当改造细胞被输回小鼠体内后,后者肠道内壁中负责维持组织功能的干细胞的活性与数量,均恢复至堪比年轻小鼠的水平。
另一组实验动物接受了非特异性靶向uPAR蛋白的CAR-T疗法,其肠道屏障完整性和炎症指标改善程度不及靶向uPAR组。
贝亚兹的同事科琳娜 · 阿莫尔(Corina Amor)表示:“经过工程化改造的CAR-T细胞清除了衰老细胞,从而阻止肠道衰老进程,甚至使组织功能逆转时光——表现出近似年轻小鼠的特征。”
上述成果已在2025年底刊载于《自然-衰老》(Nature Aging)杂志。有专家这样评价该项工作:“我们有望借此实现针对人体衰老相关的肠道功能退化的改善,进而降低肠道感染、肠道结构完整性受损乃至癌症风险。”
当然,开展人体试验前必须确定最佳“治疗剂量”。虽然uPAR蛋白高度富集于活力不足的衰老细胞表面,但正常组织也可能在某些条件下低水平地表达uPAR。
资料来源:CAR T-cell therapy makes ageing guts heal themselves
END