你有没有遇到过这样的情况:考试前特别紧张时,突然感觉肚子不舒服,甚至想跑厕所……当大脑感受到压力时,它会通过神经通路(如迷走神经)向肠道发送信号,导致肠道蠕动加快甚至痉挛,让你产生“紧张到想拉肚子”的感觉。反过来,肠胃如果不适,也会通过炎症因子、神经递质等免疫和化学信号传递给大脑,让你情绪低落,注意力涣散。
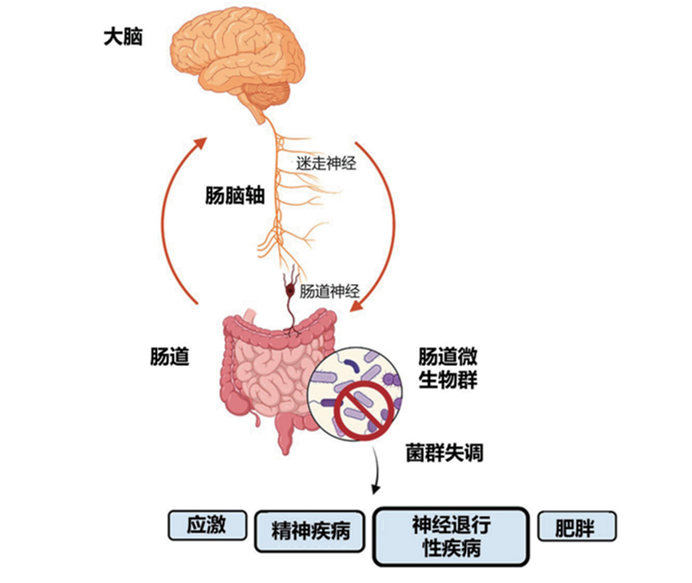
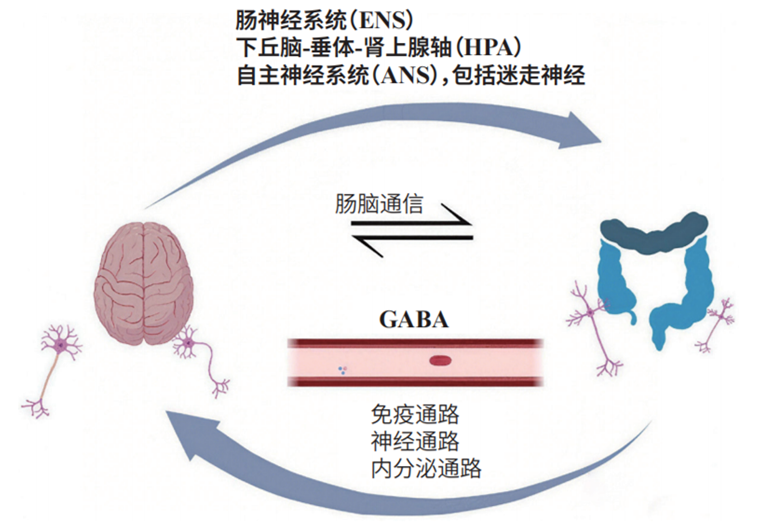
不难看出,肠胃与大脑有着紧密的联系。实际上,你的肠胃和大脑之间有一条24小时不间断的“专属热线”,科学家将这一精密复杂的双向通信系统称为肠脑轴(图1)。该系统通过神经、化学、免疫三条通路实现信息交互,悄然影响着你的认知。
图1 肠脑轴示意图(引自Singh et al.,2024)
肠脑“对话”的通道——肠神经系统和迷走神经
胃肠道拥有一个由2亿~6亿神经元构成的密集神经网络——肠神经系统(ENS),堪称人体的“第二大脑”。它贯穿整个消化道,是连接肠道微生物与神经系统的重要纽带。ENS由黏膜下神经丛和肌间神经丛组成。这两个神经丛包含多种类型的神经元,在肠壁内形成复杂的网络,不仅能够独立调节肠道蠕动、节律性收缩和肠黏膜免疫功能,还能通过迷走神经与大脑建立双向通信,参与感觉运动反射回路,进一步协调肠道蠕动、节律性收缩和肠黏膜免疫功能。
迷走神经则是肠道与大脑间最直接的神经通道,是连接大脑与胃肠道的“信息高速公路”。作为副交感神经系统的主要组成部分,它参与调节多项重要的生理功能,包括情绪调节、免疫应答、消化活动和心率控制。
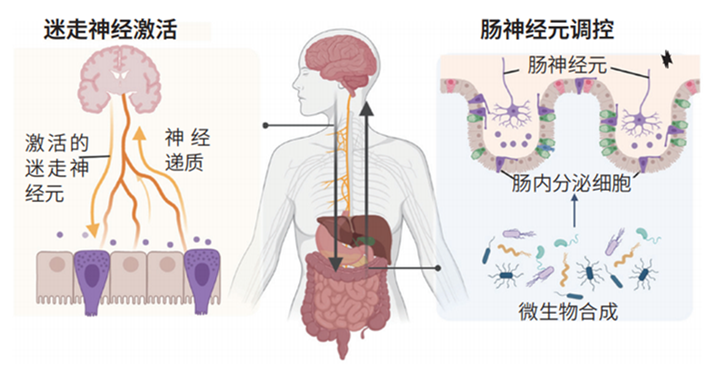
迷走神经80%的纤维为感觉传入神经,负责将肠道状态实时传递至大脑:肠道信号激活迷走神经的传入纤维,经脑干孤束核到达海马等与学习和记忆相关的脑区,调控神经元突触可塑性,影响认知功能。2018年,美国南加州大学斯科特 ?·? 卡诺斯基(Scott Kanoski)团队在《自然-通讯》(Nature Communications)杂志发文指出迷走神经与海马功能有关系。他们发现,选择性切断大鼠的胃肠道迷走神经传入神经后,其海马相关的情景记忆和空间记忆明显受损。2022年,韩国大田大学南宫郁(Uk Namgung)与同事发表在《神经炎症杂志》(Journal of Neuroinflammation)上的研究表明,刺激迷走神经不仅可以改善动物和人类的认知功能,还可以减轻炎症反应对海马的损伤,进一步证实迷走神经对海马的调控。图2展示了迷走神经介导的肠脑双向调控机制。
图2 迷走神经介导肠脑双向调控(引自Zhu et al.,2023)
肠脑“对话”的化学成分——短链脂肪酸和神经递质
肠道微生物通过代谢碳水化合物、氨基酸等底物,合成短链脂肪酸(SCFAs)、色氨酸衍生物、神经递质前体及次级胆汁酸等多样化代谢产物,构建起肠道与大脑之间“对话”的化学信号网络。这些信号分子可通过血脑屏障、迷走神经通路或免疫途径,调控中枢神经系统的神经元活性、神经递质平衡及神经炎症反应,深刻影响大脑发育、认知功能、情绪调控及行为表现。SCFAs、5-羟色胺(5-HT)、谷氨酸(Glu)和γ-氨基丁酸(GABA)是其中的关键化学信号分子,在肠脑交互中发挥重要作用。
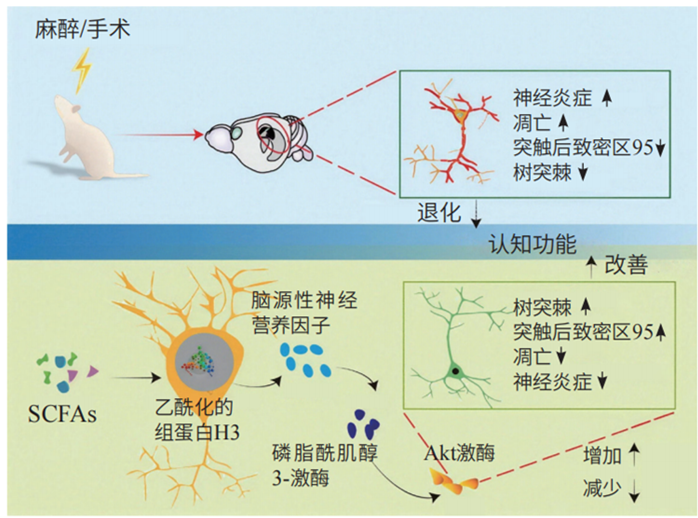
SCFAs —— 神经元的“营养剂”?以丁酸为代表的SCFAs,是我们吃下的膳食纤维被肠道微生物发酵后产生的有益物质。它们不仅能帮助维持肠道内健康的酸碱环境,还能促进保护性黏液的分泌,增强肠道屏障,守护我们的内在健康。更重要的是,这些小小的脂肪酸分子具有远距离影响大脑功能的能力。它们可以进入血液循环,并穿过血脑屏障,直接抵达与学习和记忆密切相关的海马部位。在那里,它们发挥着双重功效:一方面,SCFAs像“营养剂”一样,促进海马神经元的生长并增强其突触连接可塑性,这是学习记忆的基础;另一方面,SCFAs又能巧妙地“关闭”一些促炎因子的基因表达,减少大脑中有害的炎症因子,从而为海马神经元创造一个更适宜的局部工作环境。麻醉和手术常导致神经损伤和炎症反应,突触可塑性降低,导致在围手术期常见的认知障碍。王秋筠团队的研究发现,围手术期出现认知障碍的大鼠肠道微生物群失调,并伴随SCFAs水平的改变,补充SCFAs可以减轻海马神经元损伤和炎症反应,并恢复突触可塑性,从而改善大鼠的认知功能(图3)。
图3 SCFAs通过影响海马神经元改善大鼠围手术期认知障碍(引自Liu et al.,2025)
5-HT——主要由肠道产生的“快乐神经递质” 5-HT,又称血清素,是我们体内一种重要的化学信使,它在调节情绪、睡眠、食欲以及认知功能方面都扮演着重要角色,常被称为“快乐神经递质”。
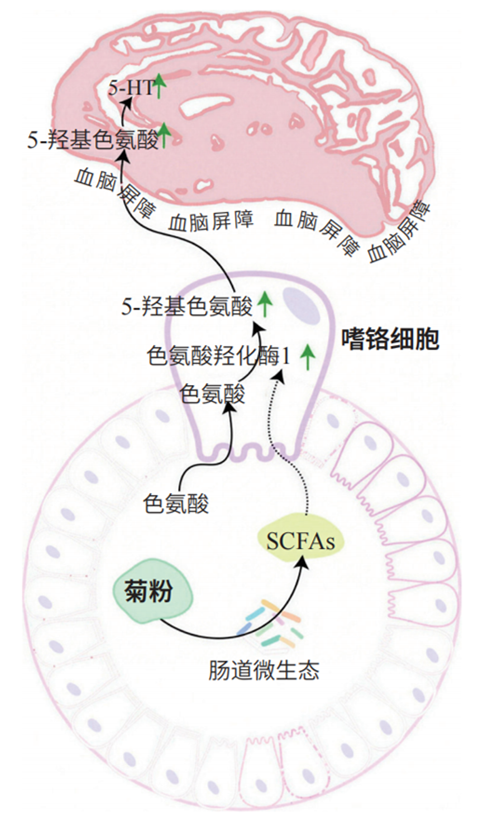
听到神经递质这个名称,你也许会认为它是在大脑中产生的,但一个令人惊讶的事实是,我们身体中大约95%的5-HT并非产生于大脑,而是由肠道内的嗜铬细胞合成。5-HT由嗜铬细胞释放后进入血液循环,穿过血脑屏障后,作用于大脑皮质和海马等广泛区域。这些区域分布着5-HT1A、5-HT3等多种受体,共同调节我们的情绪和学习记忆等过程。
图4 菊粉影响肠脑轴调节(引自Li et al.,2024)
2024年,昆明医科大学李宽团队在《植物医学》(Phytomedicine)期刊上发表了一项研究,该研究观察到,摄入酒精会诱发小鼠出现类似焦虑和抑郁的行为。研究团队深入分析后发现,这是因为酒精破坏了肠道屏障功能,干扰了中枢神经系统内的5-HT功能。而补充益生元菊粉则显示出积极的治疗效果:菊粉改变了肠道微生物群构成,能有效调节5-HT代谢并增加大脑中5-HT的浓度。由此可见,肠道健康,尤其是肠道菌群的平衡,对维持正常的5-HT系统功能具有重要意义。
Glu和GABA——兴奋与抑制的“平衡搭档” Glu是大脑中主要的兴奋性神经递质。作为“兴奋担当”的Glu,堪称肠脑轴的“油门”,负责促进神经信号传递,参与学习和记忆过程。但Glu?需维持平衡,一旦过量积累,就像“油门踩太猛”,会引发“兴奋性毒性”,损伤神经细胞,这也是阿尔茨海默病、帕金森病等神经退行性疾病的重要诱因之一。
GABA则是中枢神经系统中的主要抑制性神经递质,对维持神经系统的兴奋与抑制平衡至关重要。某些益生菌(如双歧杆菌)能直接产生GABA,调节大脑的兴奋与抑制平衡,让过度兴奋的大脑“慢下来”,缓解焦虑并提升专注力。爱尔兰科克大学和加拿大麦克马斯特大学的研究人员联合发表在《美国国家科学院院刊》(PNAS)上的研究表明,给小鼠喂食鼠李糖乳杆菌JB-1,能通过迷走神经影响大脑,改变GABA受体的表达,从而起到缓解焦虑的作用。所以,考试前喝酸奶可能还真有些科学道理——其中富含的益生菌(如乳酸杆菌)能帮助增加人体内的GABA水平,缓解紧张并提升专注力。
健康的大脑功能依赖GABA和Glu之间的精妙平衡,GABA/Glu的失衡不仅会诱发睡眠障碍,还可能引发代谢紊乱甚至肠道炎症,进而损害认知功能。许多药物的研发正是基于这一原理。例如,相关研究证实,传统中药酸枣仁可以通过提高GABA水平、降低Glu水平来帮助改善睡眠和认知能力。图5清晰地展示了GABA如何作为一个关键的“跨系统信使”,在ENS、内分泌系统和自主神经系统(ANS)之间传递信息,成为串联肠脑对话的典型代表。
图5 GABA在ENS-HPA-ANS三个系统的协同中作为跨系统信使的典型代表串联肠脑通信(引自Almutairi et al.,2024)
肠脑“对话”的免疫成分——炎症因子和胶质细胞
肠道微生物不仅通过迷走神经和代谢产物与大脑进行对话,还扮演着免疫调节器的关键角色。这一角色离不开由炎症因子与小胶质细胞等免疫细胞构成的免疫调控网络——它们既是肠道免疫状态的“传感器”,也是中枢神经功能的“调节器”,通过双向信号传导,串联起肠道健康与大脑稳态。前文提到的SCFAs、5-HT、GABA、Glu等化学信使,同时也是重要的免疫调节分子。它们共同构建了菌群-免疫-脑轴,通过调控炎症与免疫反应影响大脑。
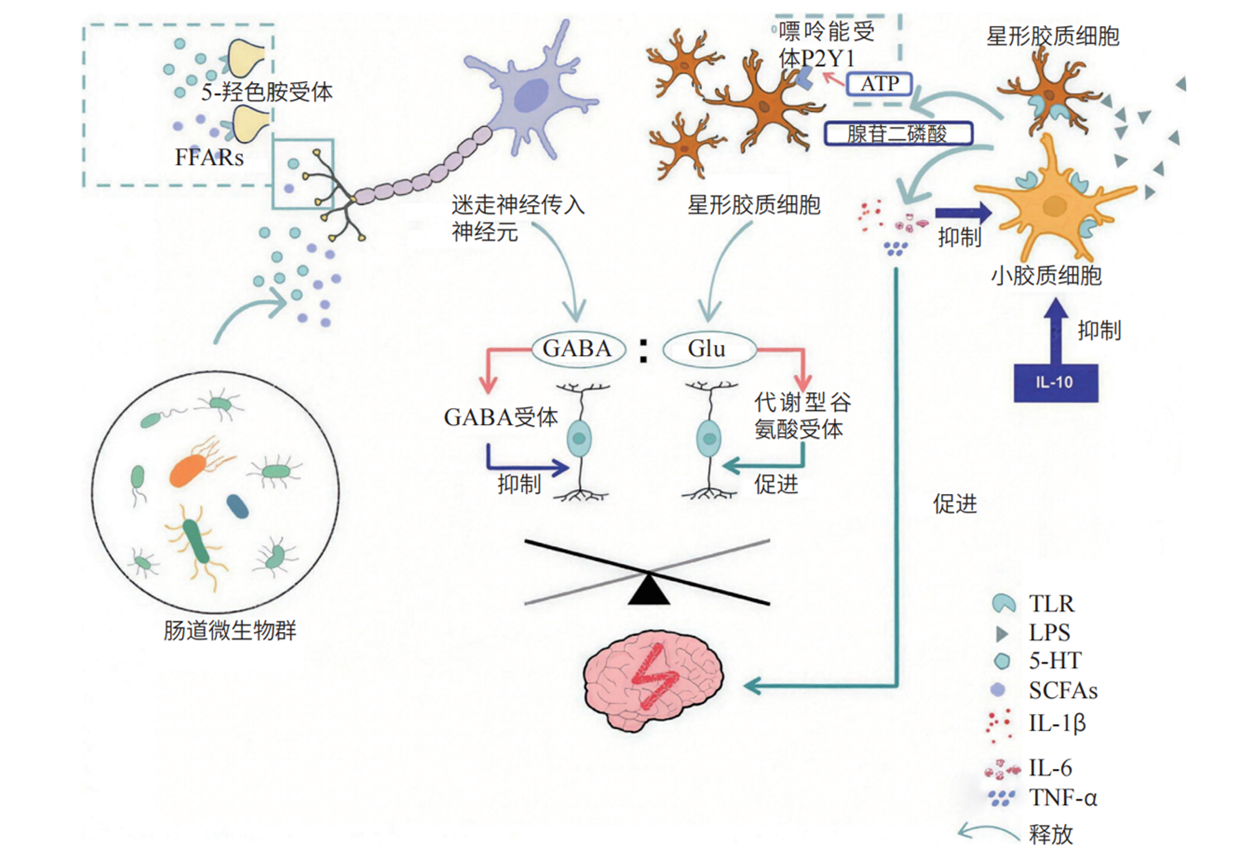
肠道微生物产生SCFAs或调节肠嗜铬细胞分泌5-HT等信号分子,这些信号分子可以被迷走神经元的游离脂肪酸受体(FFARs)和5-HT受体感知,从而将肠道信息传递到中枢神经系统。要注意的是,肠道菌群向免疫系统传递的信号并非总是有益的。例如,南方医科大学刘宇洋团队发表在《分子神经生物学》(Molecular Neurobiology)上的综述,就详细介绍了癫痫发生过程中肠脑轴的多层次调控机制:当菌群失调、致病菌增多时,其释放的脂多糖(LPS)等内毒素会进入血液系统引发全身炎症,导致胃肠通透性障碍和血脑屏障功能受损,这使得LPS可以穿过血脑屏障进入大脑与Toll样受体(TLR)相互作用,激活小胶质细胞释放腺苷三磷酸(ATP),并进一步激活星形胶质细胞。活化的小胶质细胞和星形胶质细胞释放大量炎症因子,如肿瘤坏死因子α(TNF-α)、白介素-1β(IL-1β)和白介素-6(IL-6),进而引起神经炎症反应。持续的神经炎症会导致神经损伤,白介素-10(IL-10)在LPS刺激后可能抑制小胶质细胞的过度激活。此外,活化的星形胶质细胞释放Glu,改变GABA和Glu之间的平衡。肠道菌群通过迷走神经的传入神经元,与中枢神经系统的小胶质细胞、星形胶质细胞发生复杂的相互作用,最终导致癫痫等脑部疾病的发生(图6)。
图6 肠脑轴在癫痫发生的多层次调控机制中发挥作用(引自Liu et al.,2024)
养脑先养胃,优化肠脑轴的科学策略 肠脑轴对我们的脑功能有着显著的调节作用——从这一科学视角重新审视某些经典健康建议,能够让我们更深刻地理解其重要性。
一是饮食方面,营养专家建议适当摄入发酵食物,如酸奶和泡菜,因为它们富含益生菌;也建议适当补充全谷物和坚果类食物,因为它们提供益生菌需要的膳食纤维,有助于肠道内有益菌生长,促进SCFAs产生。同时,营养专家也建议避免摄入某些物质,如人工甜味剂,因为这种成分会杀死部分益生菌;再如酒精,因为它们会破坏肠道屏障,导致毒素进入血液。
二是保持规律作息。人体肠道微生物群有着精准的昼夜节律。早晨,双歧杆菌活跃,帮助分解早餐中的Omega-3;下午,乳酸杆菌进入高产期,大量生产GABA;深夜则是有害菌的“活跃期”,此时它们会加速产生内毒素。肠道菌群的昼夜节律会因我们混乱的作息而被破坏,其代谢活动的平衡也会被打破,从而增加有害物质的生成,对大脑产生不利影响。因此,保持健康的作息并非老生常谈,而是一种重要的科学生活策略。
此外,我们也常常被建议通过运动、冥想等方式来缓解压力。这是因为慢性压力会直接导致肠道菌群失调,影响SCFAs、5-HT等产生,同时长期压力也会减弱迷走神经的张力,使机体更容易产生神经炎症,甚至诱发抑郁与认知障碍。
随着肠道菌群的功能日益明晰,它们对脑疾病的影响也越来越受重视。目前,研究人员正在探索通过粪菌移植来重塑人体肠脑轴健康。部分案例已显示出粪菌移植具有改善认知功能的潜力,这为由菌群失调引发的认知和情绪情感问题提供了新的解决思路。
———————
本文作者周湛是上海交通大学药学院/溥渊未来技术学院在读本科生;赵文娟是上海交通大学药学院副研究员,从事神经药理学与免疫药理学研究