感染人类免疫缺陷病毒(HIV)的人终身都要服用抗逆转录病毒药物。但使用工程化抗体的试验表明,艾滋病的“功能性治愈”可能近在眼前。
全球约有4000万人感染HIV。尽管治疗手段的进步意味着HIV感染不再像过去那样致命,但研究人员至今也未能找到根治方法。相反地,HIV感染者终身都要服用多种抗逆转录病毒药物进行治疗。
然而,2025年研究人员报告了一项重要突破,表明艾滋病的“功能性治愈”确实有可能实现。所谓“功能性治愈”,指无需持续治疗而能长期控制住HIV的一种方式。两项使用工程化抗体的独立试验表明,部分参与者在干预结束后很久都未服用抗逆转录病毒药物,仍能保持健康状态。
其中一项试验是FRESH试验,由南非夸祖鲁-纳塔尔大学和非洲健康研究所的病毒学家通比 · 恩东古(Thumbi Ndung’u)领导。在该试验中,20名参与者中有4人在未服用抗逆转录病毒药物的情况下,将HIV控制在无法检测到的水平——维持时长的中位数为1.5年。另一项是在英国和丹麦进行的RIO试验,由伦敦帝国理工学院的临床医生兼HIV研究专家莎拉 · 菲德勒(Sarah Fidler)领导,34名HIV阳性参与者中,有6人维持病毒控制至少两年。
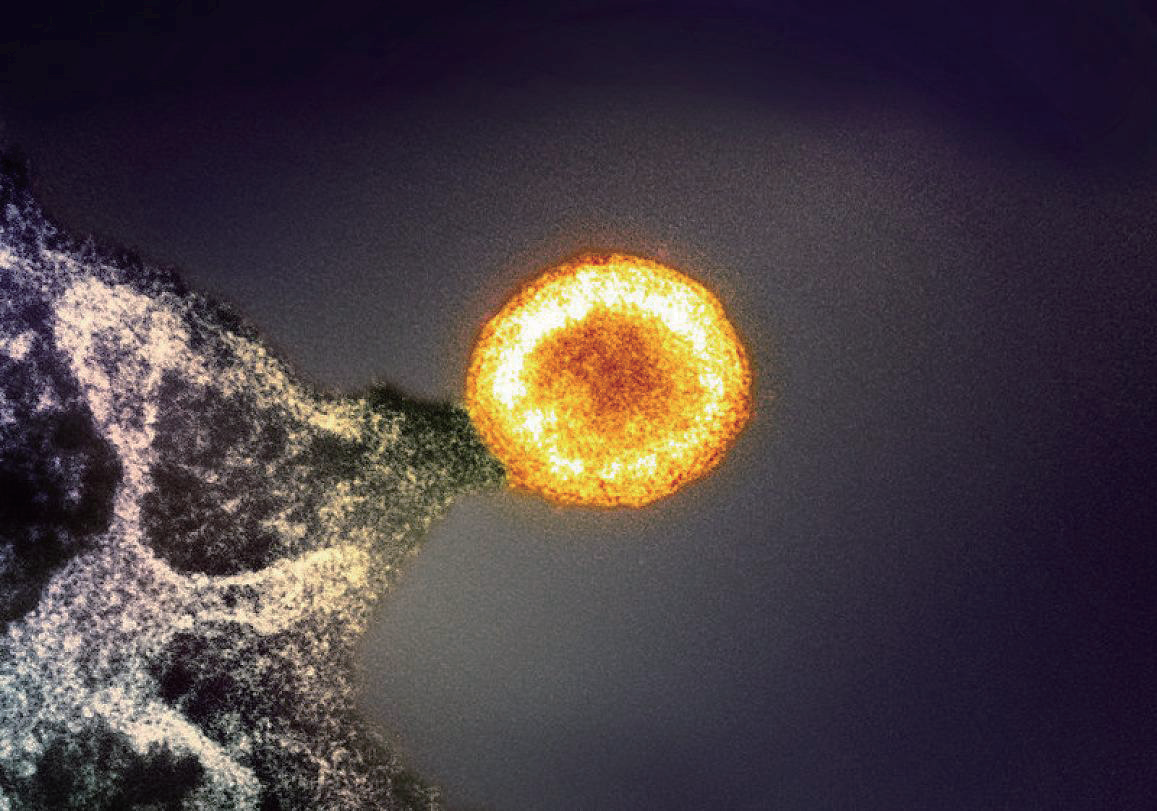
HIV颗粒正从受感染的T细胞中释放出来。单个受HIV感染的T细胞在凋亡前可释放出数以千计的新病毒颗粒,不过它们并非都具备感染其他细胞的能力
这些具有里程碑意义的概念验证试验表明,免疫系统可以被调动起来对抗HIV。研究人员目前正计划开展更大规模、更具代表性的试验,以评估是否能够通过优化抗体来惠及更多人。
菲德勒说:“我确实认为这类疗法有机会真正改变现状,因为它们是长效药物——即使完全从体内清除,其效果仍能持续。迄今为止,我们还没有见过有类似效果的疗法。”
HIV感染者如果服用抗逆转录病毒药物,可长期保持健康生活,但他们的寿命通常会比未感染者短。对许多患者来说,每日服药——甚至是较新的双月注射疗法——仍会带来沉重的经济负担、现实困难和社会压力,包括病耻感问题。“大约在过去的15到20年里,我们一直在大力探索怎样才能做得更好。”菲德勒说道。
她表示,理想的愿景是“实现人们所说的艾滋病治愈或艾滋病缓解”。但实现这一目标面临着巨大挑战,因为HIV堪称伪装大师。这种病毒在感染发生后进化速度极快,以致人体根本无法迅速产生新抗体来识别并中和它。而且,一些HIV以非活跃状态潜伏在细胞中,使得免疫系统无法识别。这些逃逸策略也让此前的一系列治愈尝试均以失败告终。除少数特殊的干细胞移植病例外,现有干预措施始终未能达到完全治愈的效果,即彻底清除人体内的HIV。
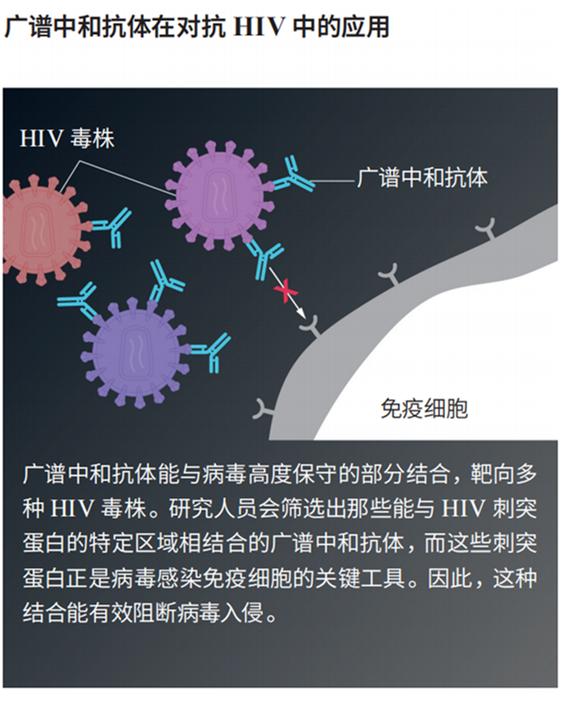
功能性治愈将会是下一个重大突破。该希望来自一种罕见现象:部分长期感染HIV的患者最终确实会产生能够中和病毒的抗体,尽管为时已晚无法完全清除病毒。这些强效抗体靶向HIV外膜蛋白中至关重要且高度保守的部分,病毒正是利用这些蛋白质来感染细胞。此类抗体能够识别多种HIV毒株,因而被称为“广谱中和抗体”。
科学家正竞相寻找最有效的广谱中和抗体,并通过工程化改造,将其开发为一种功能性治愈方案。FRESH和RIO试验可以说是迄今为止最有前景的尝试。
在FRESH试验中,科学家选择了两种抗体。这两种抗体结合使用很可能对被称为HIV-1 C亚型(在撒哈拉以南非洲地区占主导地位)的毒株有效。该试验招募了高感染率社区的年轻女性作为参与者,试验本身隶属于一个覆盖更广泛目标与内容的社区赋权项目。这些女性在几年前感染HIV后,即通过该项目在三天内开始了抗HIV治疗。
与此同时,RIO试验选择了两种经过充分研究、被证明具有广泛效用的抗体。其参与者主要是40岁左右的白人男性,他们同样在感染HIV后不久就开始接受抗逆转录病毒药物。其中,大多数人感染的是HIV-1 B亚型毒株,该亚型在欧洲更为常见。
研究人员联合使用两种抗体,就是为了降低HIV产生耐药性(这是抗体治疗中的一个常见挑战)的可能性,因为病毒需要发生多重突变才能同时逃避两种抗体的作用。
两项试验的参与者均先接受了一次抗体注射。随后,他们暂停了抗逆转录病毒治疗。研究人员希望此类抗体(经过改造,可在体内存留约半年时间)能与免疫系统协同作用,杀死活跃的HIV颗粒,从而将病毒控制在可控范围内。如果效果未能持续,在抗体被分解后,参与者体内的HIV载量就会上升,他们将不得不恢复抗逆转录病毒治疗。
然而,令人兴奋的是,两项试验的结果均表明,在部分参与者体内,干预措施触发了一种持续的、自主的免疫反应——研究人员称其效果堪比疫苗。
在RIO试验中,34名接受广谱中和抗体治疗的参与者中有22人到第20周时都未出现病毒载量回升的情况。此时,他们接受了另一次抗体注射。96周后——那些抗体早已消失——仍有6人体内的病毒载量维持在较低水平,无需恢复抗病毒治疗。
该研究还纳入了另外34名参与者作为对照组,他们仅接受生理盐水输注,其中大部分人在4至6周内就不得不恢复治疗。截至第20周时,除3人外,其余所有人均已重启治疗。
研究人员在FRESH试验中观察到了类似的模式——尽管该试验主要是一项安全性研究,未设立对照组。20名参与者中有6人在输注抗体后维持了48周的病毒抑制效果,其中4人甚至在超过一年的时间里都没有继续治疗。在干预实施两年半后,仍有1人未恢复抗逆转录病毒治疗。
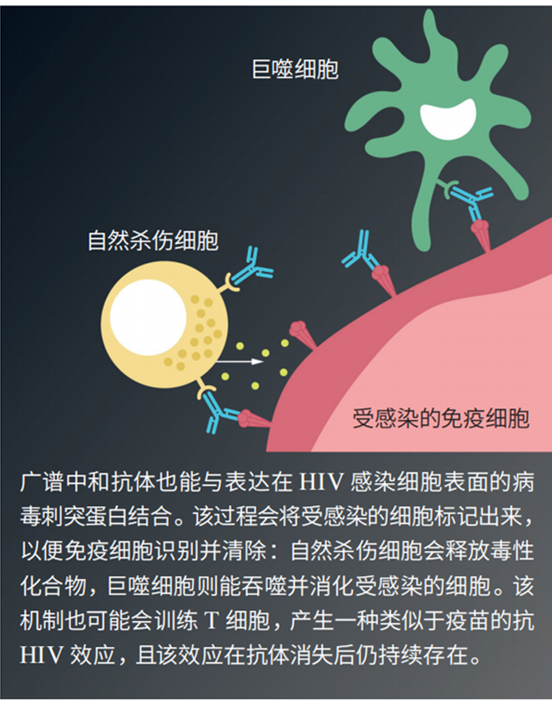
目前尚不清楚病毒载量何时会回升,因此研究人员在称处于缓解期的参与者为“功能性治愈”这件事上持谨慎态度。然而,这些抗体似乎明显在“诱导”免疫系统对抗病毒。它们附着在受感染的细胞上,向免疫细胞发出信号,引导其前来清除感染细胞。
此外,重要的是,研究人员认为,抗体引发的这种免疫反应可能还会刺激一种名为CD8+ T细胞的免疫细胞,该细胞会“追杀”HIV感染细胞。这一过程可能会形成一种“免疫记忆”,帮助人体在抗体消失后继续控制HIV。
这种反应类似于在一小群HIV感染者(不到1%)身上观察到的免疫控制能力。这类感染者被称为HIV“精英控制者”。他们无需借助抗逆转录病毒药物就能抑制HIV的复制,将其主要限制在小型病毒储存库中。约翰 · 霍普金斯医学院的传染病专家乔尔 · 布兰克森(Joel Blankson)说:“这些试验帮助部分参与者做到了类似的事情,实在令人兴奋。这或许能教会我们如何更有效地做到这一点,以便让更多人获得缓解。”他是2024年《免疫学年度评论》(Annual Review of Immunology)上一篇关于天然HIV控制者论文的作者之一。
科学家确切知道的一点是,如果人们在感染后不久——当免疫系统仍然完好、病毒储存库较小时——就开始抗逆转录病毒治疗,实现持续控制的可能性会更高。
但在感染后很久才开始服用抗逆转录病毒药物的人群(即所谓慢性感染者)中,“治疗后病毒控制”现象也有可能发生。“只是这种情况发生的概率较低。由此可见,这些研究中采用的治疗策略有可能同样适用于慢性感染者。”布兰克森表示。
RIO试验中还有一个特别有前景的发现:这些抗体同样能作用于潜伏在某些细胞中的休眠HIV。这些储存库正是患者停止治疗后病毒载量回升的根源所在,而人们通常认为抗体无法作用于它们。研究人员推测,经抗体激活的T细胞能够识别并清除那些表面仅表达微量HIV的潜伏感染细胞。
与此同时,FRESH试验通过联合使用另一种名为维沙莫德(Vesatolimod)的药物,更直接地靶向了顽固的HIV储存库。该药旨在刺激免疫细胞对HIV威胁作出反应,并有望使休眠的HIV颗粒从其潜伏的细胞中“暴露”出来。一旦发生这种情况,免疫系统便可在抗体的帮助下识别并清除它们。
恩东古表示:“FRESH试验的结果令人兴奋,因为这可能意味着该治疗方案在某种程度上是有效的。不过,由于这是一项小型研究,显然很难得出非常确切的结论。”他的团队仍在分析数据。
恩东古计划获得资金后在南非进行一项规模更大、纳入慢性感染者的试验。与此同时,菲德勒团队正在招募RIO试验的第三组参与者,以确定在给参与者注射抗体前暂停抗逆转录病毒治疗更长时间是否会引发更强的免疫反应。
另一项在英国开展的名为AbVax的相关试验将在治疗方案中加入一种T细胞刺激药物,以观察能否增强抗体持久的、类似疫苗的效果。作为该研究的主要研究人员,菲德勒表示:“或许将不同的治疗策略相结合,能够增强免疫系统的不同模块,这正是未来的发展方向。”
菲德勒和恩东古也将继续跟踪那些体内病毒得到抑制的参与者——他们自确诊感染HIV以来,首次摆脱了每日用药的负担。
资料来源 Knowable Magazine