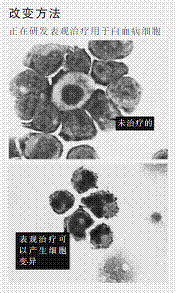
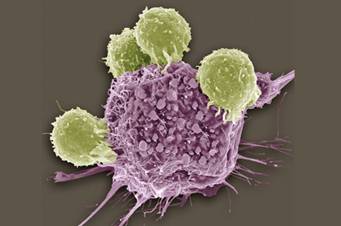
研究者正竞相开发“虚拟细胞”,这种技术有望通过预测基因活性等特性,彻底改变生物医学领域。
人类细胞中充斥着数万亿个分子,包括大量的蛋白质、碳水化合物、脂质和核酸。细胞内分布着细胞器和其他结构,其错综复杂的组织形式让巴洛克式建筑都显得简单朴素。细胞质宛如一个繁忙的化学实验室,分子在此不停地发生反应、重组与重塑。在细胞核内,成千上万个基因不断地开启和关闭,将看似混乱的状态转化为协调一致的生命活动,从而支撑细胞存活与增殖。
这种复杂性远超人类大脑当前能够完全理解或预测的范围。然而,许多研究者认为,人工智能(AI)凭借其强大的信息整合和处理能力,或许可以胜任这项任务。二十多年前,研究者便开始构建方程组,用来模拟细胞的部分运作机制。如今,他们已研发出由AI驱动的细胞“复制品”——这些模型如同大语言模型一样,通过海量数据自主学习。ChatGPT三年前的惊艳亮相,给虚拟细胞的构建者们带来了灵感。艾伦研究所从事AI研究的科学家卡西亚 · 凯齐尔斯卡(Kasia Kedzierska)说:“大家希望生物学领域也能迎来这样的突破性时刻。”
面向现实需求的虚拟细胞技术
这类模拟活体细胞的虚拟细胞对多个研究领域都大有裨益。在制药实验室中,科学家可以利用它们快速评估大量药物,而无需经历成本巨大且复杂的实验过程;它们还能成为工程化细胞的测试平台,助力改造细胞以实现新功能;根据患者分子特征定制的虚拟细胞,可帮助医生选择个性化药物;研究者甚至能将细胞模型整合进虚拟组织和器官,以探讨诸如肿瘤环境如何影响肿瘤生长等问题。
陈-扎克伯格基金会(CZI)的科学AI负责人西奥法尼斯 · 卡拉莱佐斯(Theofanis Karaletsos)说:“这类由AI驱动的细胞模型还能帮助研究者梳理涌入分子数据库中的海量多元信息,构建整合性的知识图谱。”
与ChatGPT等AI工具一样,AI细胞模型也承载着诸多厚望。“每当有新模型问世,总是会被说成是最好的。”Arc研究所的计算生物学家哈尼 · 古达齐(Hani Goodarzi)说道。他本人也开发过此类模型。2025年6月,他与20多位研究者共同发起了“虚拟细胞挑战赛”,这项年度赛事对各类相关模型进行了实测。首届赛事要求参赛者预测沉默人类胚胎干细胞中特定基因的影响。该挑战赛类似于1994年启动的结构生物学竞赛——帮助研究者基本解决了蛋白质折叠问题——旨在推动生物学领域的技术进步。
即便相关模型在测试中表现出色,一些科学家仍然认为,要让它们产出新科学发现或是为生物学家提供实质性的帮助,还有很长的路要走。微软研究院的亚历克斯 · 卢(Alex Lu,研究的是AI如何识别生物数据模式)指出:“尽管热度很高,但这些模型的实际表现仍不尽如人意。”有些模型的预测能力甚至与较简单的模拟无异。俄亥俄州立大学的计算生物学家马琴(Qin Ma,音译)说:“模型泛滥本身就是一种不好的信号。若有一个足够强大的模型,就无需涌现如此多的同类型产品。”
模型开发者则认为成功只是时间问题。“虽然问题尚未解决,但这种方法是极具潜力的。”赛拉治疗公司(Xaira Therapeutics)生物医学AI部门负责人王博(Bo Wang,音译)说道。该公司希望利用虚拟细胞技术进行药物研发。
从“方程模拟”到“AI驱动”
受计算能力提升的启发,研究者大约在25年前就开始尝试构建虚拟细胞。最初,他们采用基于大量方程组的计算方法,来模拟新陈代谢、蛋白质合成、DNA复制等细胞过程。
2012年,现就职于西奈山医学院的计算系统生物学家乔纳森 · 卡尔(Jonathan Karr)与斯坦福大学的同事共同推出了首个全细胞模型——生殖支原体的硅基版本。之所以选择这种微生物,是因为其基因组是当时已知细菌中最小的——仅含500多个基因,而常见的大肠杆菌则有4000多个基因。为复刻该生物体的代谢过程,模型计算了700多种代谢物在1100个化学反应中的浓度变化。通过对染色体和蛋白质合成细胞器(即核糖体)进行建模,这个模拟细胞在一定程度上还原了真实细胞的内部结构。
这张图展示了首个全细胞模型所包含的元素
2022年,伊利诺伊大学厄巴纳-香槟分校的细胞生物学家兼生物物理学家赞 · 卢西-舒尔滕(Zan Luthey-Schulten)和同事推出了一个基因数量稍微少些但更为精密的模型。该模型基于一种经实验室改造过(仅保留493个基因)的极小细菌细胞。研究者利用冷冻电子断层扫描技术收集真实细胞的成像数据,将模型构建为3D形态,从而增强了模型的真实性。这种级别的细节处理需要高昂的计算成本:模拟细胞20分钟的生命活动,就需要高性能GPU运行8到10小时。
科学家还为大肠杆菌等其他细菌开发了类似的全细胞模型。这些模型启动后,能逐秒模拟细胞的代谢、生长和分裂过程。卡尔说:“这些模型的核心优势是能够预测短期细胞动态,比如特定分子浓度的变化。”卢西-舒尔滕也坚信,终有一日研究者一定能创建出人类细胞的计算模型。
但王博指出,这些非AI模型只能遵循开发者设定的生物学规则,我们还不清楚其背后的数学方程能否还原真实细胞过程。此外,慕尼黑工业大学的计算生物学家法比安 · 泰斯(Fabian Theis)表示:“这些模型无法处理研究者最想解答的诸多问题。可以说,它们在某些预测任务上完全失败了,比如在预测基因沉默的影响方面。”
虚拟细胞挑战赛则反映了人们对新型由AI驱动的模型的期望。这类模型不再依赖固定方程组,而是利用海量实验数据,自主学习细胞的运作原理。斯坦福大学的生物物理学家史蒂夫 · 奎克(Steve Quake)在谈到他与CZI同事开发的AI模型TranscriptFormer时说道:“我们没有教它任何生物学知识。”
这些模型能充分利用大量的新数据,尤其是单细胞基因活性的测量数据。例如,CZI的CELLxGENE数据库就收录了超过3500万个人类和小鼠细胞的基因活性数据。卡尔强调:“模型开发者还乘上了技术发展的东风。”
当AI细胞模型开始“无师自通”
与GPT-5、Claude、Gemini等通用AI相似,目前已发布的AI细胞模型大多是基础模型,从理论上来讲,它们无需额外训练就能探究多种细胞过程。不过,目前AI细胞基础模型仅能捕捉生物学的冰山一角,完成的任务也比较有限,包括细胞分类、预测细胞对基因活性变化的反应等。研究者希望最终能将它们整合为更全面的系统。泰斯说:“构建一个‘一统天下’的模型是我们的目标。”
加州大学旧金山分校的计算生物学家克里斯蒂娜 · 西奥多里斯(Christina Theodoris)及其团队于2023年5月在《自然》(Nature)杂志上介绍了早期的细胞基础模型Geneformer,其开发旨在改进先前一款功能较弱的AI模型。那款旧模型可分析基因互作网络并预测对其进行修改的效果。2021年,西奥多里斯团队在《科学》(Science)杂志上发表论文称,他们使用那款模型鉴定出一种分子,可能可以治疗以心脏瓣膜钙过量沉积为特征的心脏病。其他科学家也一直将这种分子作为潜在疗法进行研究。但这一成功来之不易:研究者必须自己从实验数据中推导出基因网络并将其提供给模型。西奥多里斯表示:“开发Geneformer就是想看看我们能否构建一个具备基因网络基础知识的模型。”
她和团队成员使用了近3000万个人类细胞的基因活性数据训练Geneformer,发现它能够推断基因间的相互作用,并预测修改特定基因的效果。随后,研究者又用健康人群和心肌病患者的心脏细胞基因活性数据对其进行新一轮的训练。它最终筛选出了几种基因,这些基因的失活有望让功能减弱的心肌细胞恢复正常。
Geneformer团队进一步开展了实验验证(这超出了大多数AI研究团队的常规操作)。他们利用CRISPR基因编辑技术,在实验室培养的心肌细胞——这些细胞携带了可诱发心肌病的基因突变——中敲除了两个关键基因。结果发现,敲除其中任意一个基因都能增强细胞的收缩力,这表明抑制这些基因功能的药物可能对患者有益。西奥多里斯说:“这一结果证明,Geneformer能为研究指明新的方向,并且可以加速药物研发。”
尽管如此,Geneformer还是与许多AI细胞模型一样,仅基于人类的数据进行训练,虽然少数其他模型也纳入了小鼠数据。而奎克、卡拉莱佐斯等人2025年早些时候在预印本平台bioRxiv上发布的TranscriptFormer模型,在进化维度上独具优势。研究者开发了该模型的三个版本,其中最全面的版本用了来自12个物种的1.12亿个细胞的基因活性数据进行训练,这些物种包括人类、鼠类、线虫、海绵等。
多样化的训练数据或许优化了其性能。研究者表示,在人类罕见细胞类型分类任务中,TranscriptFormer的表现优于王博团队于2024年推出的scGPT和前面所说的Geneformer模型。该模型还能对未纳入训练集的物种细胞进行分类,区分感染新冠病毒的肺细胞与健康肺细胞,并预测药物对细胞的影响。卡拉莱佐斯说:“这些表现尤为值得关注,因为该模型未接受任何额外的训练,它具备了研究者们所说的零样本学习能力。这表明,我们可以利用此类工具探索基础生物学问题。”
研究者还可以将细胞基础模型整合到AI科学家这类虚拟助手中。AI科学家能梳理研究文献、提出假设、基于真实数据开展模拟实验并撰写研究结果。2025年早些时候,哈佛大学的计算生物学家马林卡 · 齐特尼克(Marinka Zitnik)及其同事发布了一套包含600多种工具的资源库,助力研究者开发AI科学家,TranscriptFormer便是其中之一。她说:“得益于该模型的设计方式,研究结果产出的速度更快、准确性也更高。”
AI细胞模型面临的发展瓶颈
那么,是什么在阻碍虚拟细胞技术的发展?
当前大多数AI模型依赖单一类型的数据:基因活性测量数据。马琴表示,研究者才初步尝试纳入细胞图像等其他类型的信息,这可能会催生出更强大、更实用的模型。即使近年来细胞数据数量激增,但仍不足以支撑模型的发展。卡尔说:“数据的局限是细胞模型发展的一个巨大障碍,这导致我们能探索的问题范围非常有限。”
卡尔指出,尽管像CELLxGENE这样的数据库已经问世,但许多研究结果最终并未存储在可供其他科学家便捷访问的中央存储库中。他认为,该领域需要构建一个类似蛋白质数据库(PDB)的资源库。PDB曾助力AlphaFold——这款蛋白质折叠预测模型或许是目前科学界最成功的AI模型,其两位开发者于2024年获得诺贝尔化学奖——取得重要突破。PDB还以标准格式收录了几乎所有经实验测定的蛋白质结构,部分原因是大多数资助机构和期刊要求研究者将新测定的蛋白质结构添加到该数据库中,而针对细胞数据,目前没有这样的要求,且其多样性要远超蛋白质结构。卡尔说:“单靠一项技术无法呈现细胞的全部特征。”
为了改进现有模型,研究者还需要通过有效的评估手段来衡量其性能。然而,至于该如何有效评估这些模型,科学界尚未形成定论。模型完成初始训练后,开发者通常会进一步调试以提升某些特定能力,然后再进行测试。这一做法与GPT-5等主流基础模型的开发过程类似——它们在向公众开放之前都会经过大量的微调。但一些研究者认为,测试应该评估模型的零样本性能。泰斯表示:“如果模型真能推断出对生物学的基础性理解,那么它们在微调之前就应该具备这种能力。”
多项评估近期开发的AI细胞模型零样本性能的研究发现,这些模型存在明显不足。例如,凯齐尔斯卡等人曾将scGPT、Geneformer这两款基础模型与一款更为原始的AI模型及两种非AI方法进行对比测试。令他们惊讶的是,在细胞分类等任务中,更简单的方法在表现上反而要优于这两款基础模型。相关研究于2025年早些时候发表在《基因组生物学》(Genome Biology)杂志上。
西奥多里斯则反驳称,这些任务相对简单,因此更简单的方法也能完成,测试并未挖掘出Geneformer的真正实力。
然而,伦敦大学学院的博士后研究人员康斯坦丁 · 阿尔曼-埃尔策(Constantin Ahlmann-Eltze)及其同事2025年8月在《自然-方法》(Nature Methods)杂志上发表研究称,即便经过微调,一些AI细胞模型仍表现不佳。他们设定的任务是预测某些基因对其他基因活性变化的反应。结果发现,一个基础数学公式在预测的准确性上要高于五个细胞基础模型和另外两个AI模型。“我非常惊讶。根据已发表的论文,这些模型看起来都非常出色。”阿尔曼-埃尔策说道。
这类研究仅测试了有限数量的模型,且采用的标准各不相同。但凯齐尔斯卡表示,大家对这些模型应具备的功能以及相应的性能评估方法有了更清晰的认识。她指出,CZI在2025年早些时候发布了新的基准测试工具,能让研究者根据标准指标来评估不同模型的性能。
即便是对当前虚拟细胞技术提出过批评的科学家,也对AI方法的未来持乐观态度。凯齐尔斯卡说:“我不会放弃这些模型,它们的失败也能为我们提供很多信息。我坚信我们终有一日会打造出真正优秀的模型。”
卡拉莱佐斯对此表示认同:“TranscriptFormer将是我们开发出的最‘笨拙’的模型。”
资料来源 Science