保证足够蛋白质摄入才可保证身体健康是大家的共识。但有许多针对动物的实验发现了违背直觉和经验的现象,即极低蛋白质摄入的饮食反而帮助动物活得更久。此类现象背后的原因是什么?关于人类衰老的研究可从中获得怎样的启示?
蛋白质常常以乏味的形状被送到嘴边,比如一块寡淡塞牙的鸡胸肉或一根健身特供蛋白棒,但这不妨碍现代人对它们怀有“科学告诉我要吃下足够多优质蛋白”那样的迷恋。
面对超市货架,你会看到占据了蛋白薯片、蛋白水、蛋白曲奇饼干等五花八门的蛋白质零食。面对最新版美国人膳食指南,你则会发现蛋白质推荐摄入量从每公斤体重0.8克提高到了1.2~1.6克。
“蛋白质摄入不足会导致各种健康问题”已不再是要特意找文献背书的共识。而似乎与此共识相悖的一类科学现象则是:从单细胞酵母到昆虫再到啮齿动物,都会因蛋白质摄入量被大幅减少而延长寿命!当然,大众对此鲜有了解。
那么,严格限制蛋白质摄入有没有可能令人类的寿命延长?
首先需要先明确,人体依靠蛋白质构建和修复组织,若饮食中蛋白质提供的热量占总热量的比例不超过7%,长此以往不仅无法延年益寿,反而可能引发营养不良问题。科学家向实验动物施以对人类而言相当极端的蛋白质限制饮食/低蛋白饮食,旨在探究生物感知营养的机制、机体应对营养过剩或不足的策略,以及如何影响健康和寿命的种种机制。动物研究的结果或可为人类提供启示。
虽然人类不应践行此类极端的低蛋白饮食,但正如加拿大生理学家斯图尔特·菲利普斯(Stuart Phillips)所言:“通过探寻其中原理,我们可以学习如何应对衰老、怎样健康地老去。”
在极限控蛋白后,小鼠经历了什么?
热量限制是一种广为人知的长寿饮食策略。
过去一个多世纪以来的调查显示,将实验动物的总热量摄入减少20%至50%,其寿命就会延长。如今有些认可这种理念的人士践行着相对温和的热量限制饮食。
菲利普斯则指出,蛋白质限制饮食就好比“轻量版”热量限制。
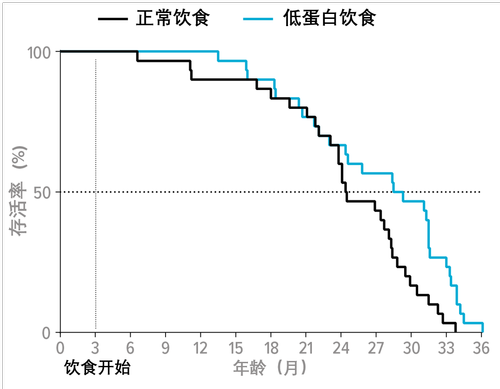
2025年的一项研究表明:自由进食普通饲料的小鼠,最长寿命为1008天;喂食同款饲料但热量仅相当于正常水平80%的小鼠,能活1179天——对小鼠而言已是高寿。这两组饲料的蛋白质占比均为18%。第三组小鼠享用无热量限制的自助餐,不过饲料的蛋白质占比仅6%;结果,它们的寿命介于前两组之间,最长达1115天。
除了寿命延长,还有健康状况的改善。
研究人员发现,那些接受热量限制或蛋白质限制饮食的小鼠,其血糖和胰岛素水平更低,胰岛素敏感性更高。这些都是代谢健康的标志。此外,随着年龄增长,自由进食组小鼠的身体状况往往因衰老不断恶化,限制组的健康指标却有更长保质期。不难想见,后者体脂率也更低。事实上,当实验进行一年后,限制组小鼠身形消瘦,体重约为正常小鼠的2/3。
研究团队向30只雄性小鼠喂食蛋白质占比20%的标准饲料,并向另外30只喂食蛋白质占比仅5%的饲料。结果显示,蛋白质摄入更少的小鼠寿命更长。
另一项发表于2025年末的《细胞》(Cell)文章聚焦于衰老的分子标志。
我们知道,机体会在衰老过程中经历一系列变化,比如不稳定的活性氧自由基造成组织损伤。而接受低蛋白饮食的小鼠不同寻常。
根据文章作者介绍,它们有多个器官在DNA和蛋白质层面都表现出多种抗衰老特征,比如其体内具有保护作用的抗氧化酶水平升高。此类益处在中年个体身上尤为明显,这说明低蛋白饮食的益处在生命周期的不同阶段的效果不一。
演化智慧:蛋白充足时重拳出击,营养匮乏时唯唯诺诺?
科学家尚未明确蛋白质限制饮食使小鼠更瘦、更健康、更长寿的原理。有人推测实验小鼠身形消瘦的直接原因是缺乏构建与维持身体组织的营养;当然,也有可能是机体将有限能量都供给了大脑功能。不过此类解释相对片面浅显。
剑桥大学神经内分泌学家克莱芒斯·布卢埃特(Clemence Blouet)把人体比作汽车:你可以高速行驶,代价是消耗大量燃料、加速汽车磨损;你也可以坚持每小时25公里的低速平稳行驶,好处是汽车使用寿命会更长。
长期处于高蛋白、高热量摄入的“快车”生活,可能导致那些加速衰老的氧自由基不断堆积。再者,人体内能促进生长和衰老的系统会被蛋白质激活。
饮食限制则可减少有害自由基的产生和衰老反应的发生,令机体更长久地维持良好运转状态。
菲利普斯提出了另一种理论:当营养供应不足时,人体迫进入高效运转模式,循环利用合成蛋白质的氨基酸原料。“在这种状态下,许多年龄相关的生物过程也有了更高效率,运转状态非常好。”
美国彭宁顿生物医学研究中心的生理学家克里斯托弗·莫里森(Christopher Morrison)则认为,低蛋白饮食带来延寿效果的背后存在更深层次的生物调节策略。莫里森与同事研究了一种由肝脏分泌、名为成纤维细胞生长因子21(FGF21)的激素。
当蛋白质摄入不足时,FGF21似乎能向大脑传递信号——“注意!饮食中的蛋白质含量不足!”若对小鼠进行基因改造,使其缺失FGF21,它们摄入低蛋白饮食后,不仅无法延寿,反而会更早死亡。
换言之,只有当大脑接收到蛋白质不足的信号,并调节身体反应,低蛋白饮食才可真正发挥延寿作用。
既然蛋白质匮乏时的延长寿命是一种选择(尽管这是无意识的行为),那么,机体在营养富足时默认更短寿命也是一种主动选择。悉尼大学的营养生物学家斯蒂芬·辛普森(Stephen Simpson)指出,上述现象看似违背直觉,但对于需要在生存和繁衍间求得平衡的生物而言,这完全合乎演化逻辑:
如果蛋白充足,我就“趁热打铁”,将能量、资源都投入到生长、繁殖;而这种选择的代价是,我难以及时修复氧自由基或其他应激源造成的组织损伤,当然,我接受此代价,即便它意味着折寿数月。从演化角度来看,多出来后代足以平衡被削减的寿命。
反之,假如营养匮乏,我就“蛰伏等待”,激活保护性和修复性的抗衰老机制,希望撑到食物充足时再进行繁殖,即便这意味着长期瘦小孱弱。
以上理论有实证支持。辛普森与同事研究发现:相较于保持高蛋白摄入的小鼠,低蛋白饮食组小鼠的精子数量、卵泡数量等生殖指标均有所下降。
或许有人会问:所谓的“趁热打铁”与“蛰伏等待”现象,其底层的微观分子机制是如何运转的?
菲利普斯认为,若可揭示发挥作用的相关分子,我们有望以此为基础,开发出可助人类健康老去的药物。
举例来说,目前已知哺乳动物雷帕霉素靶蛋白(mTOR)分子介导的生理系统能调节生长、繁殖和衰老;低蛋白饮食则可抑制mTOR——另一种具备抗衰老潜力的药物雷帕霉素也有此效果。
人类应怎样管理蛋白质摄入
需要再次强调,以上谈及的所有研究数据均来自动物实验。如莫里森所言:“我们还并不真正了解,长期的低蛋白质饮食会对人体造成何种影响。”
科学家不可能招募一大群人并要求其长期坚持低蛋白饮食,接着在数十年里观察志愿者的寿命。不过他们能通过问卷调查采集信息,对受访者的饮食情况与疾病及生存状况进行关联分析。
菲利普斯表示,此类流行病学研究的结果虽不尽相同,但总体而言,蛋白质摄入量较高的人群,遭遇血管疾病和2型糖尿病的风险略高。当然,这里存在干扰变量——大量摄入动物蛋白也意味着同时摄入饱和脂肪。相比之下,主打植物蛋白的饮食组并不面临同类风险。
另一大研究难点在于,不同年龄段的人群对蛋白质的需求不同。
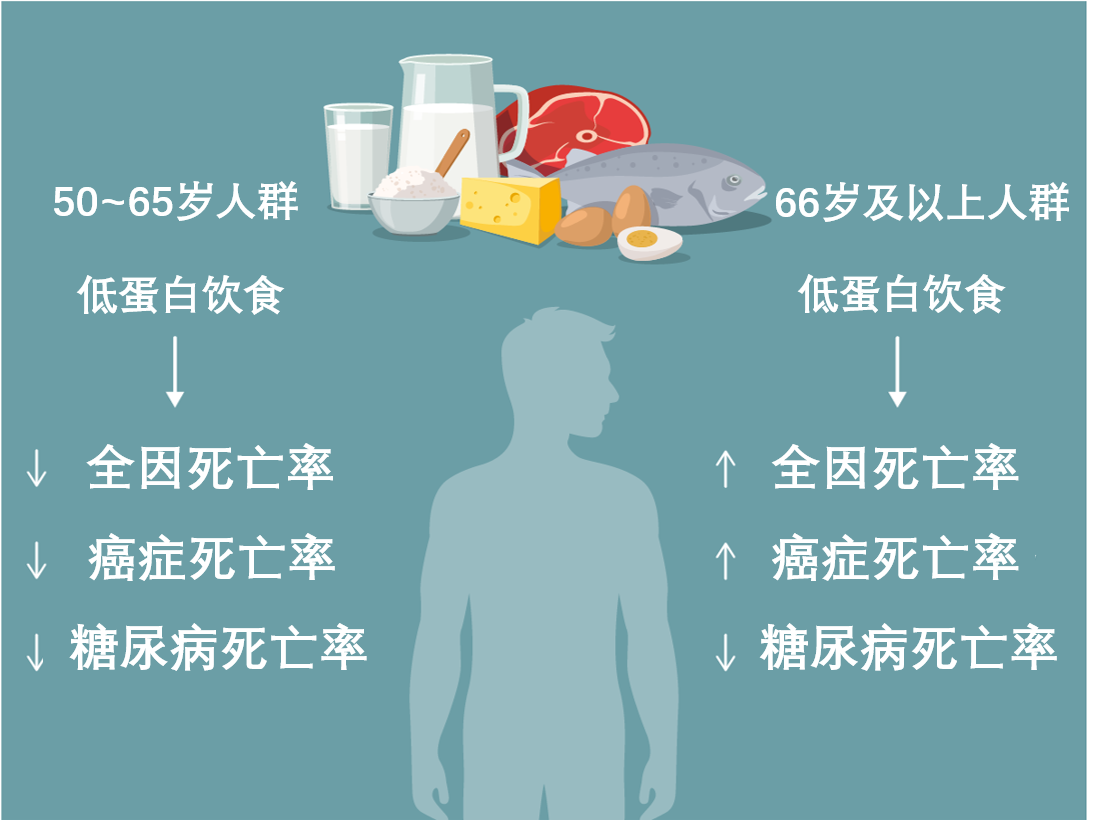
曾有研究者发现,低蛋白饮食相较高低蛋白饮食,前者在50~65岁人群中关联着更低的因癌症等各种原因死亡的风险,在65岁以上人群中却关联更高风险。鉴于此,总体上更有益健康的饮食习惯或许是,中年时期保持较低水平至平均水平的蛋白质摄入,65岁后适当增加摄入量。
针对人类的观察性研究表明,蛋白质需求量因年龄而异,低蛋白饮食的影响也存在差异。在50~65岁的成年人中,低蛋白饮食与癌症、糖尿病及其他原因导致死亡的风险降低相关;而在66岁及以上的人群中,低蛋白饮食虽仍与较低的糖尿病死亡风险相关,却与其他原因导致的死亡风险升高相关。
此外,长期坚持特定饮食方式对人类而言是艰巨挑战。辛普森曾深入观察从蝗虫到人类的一系列物种,最后得出结论:缺乏蛋白质补充的身体会产生强烈的蛋白质渴求。
举例来说,参与辛普森团队项目的一批志愿者历经数日饮食干预,期间被要求从一份限定菜单上自由选择食物,而所有菜单食物的蛋白质热量占比均为10%。结果志愿者猛吃咸味零食,仿佛渴求蛋白质的鲜味,最终他们的总热量摄入随之增加。这显然算不上成功的饮食控制。
资料来源:
The curious case of low-protein diets
END