
科学家正在寻找能使人类健康长寿的基因蓝图
厄文·卡恩(Irving Kahn)是美国华尔街最年长的证券交易人,尽管已年逾百岁高龄,仍然非常活跃,科学家希望更多人能与他媲美。
在任何一个工作日的早晨,你可能会看到卡恩正前往他在曼哈顿的办公室,在那里他的职务是投资者和金融分析师――看似寻常,却又非比寻常――卡恩差不多自1928年以来就一直在这一行工作了。
今年106岁高龄的卡恩是那些活到百岁以上仍能保持心智健全并且出奇健康的老人之一,这些百岁老人引起了衰老研究者们的关注。托马斯·波尔斯(Thomas Perls)是美国马萨诸塞州波士顿大学的一位老年医学研究专家和新英格兰百岁老人研究项目主任,他回忆起早年曾遇到过两位百岁老人,改变了他以前对高龄老者健康状况明显不好的想象。当波尔斯在一个康复中心进行康复训练时,他看到了“一位百岁老人出去后打算为每个人弹奏钢琴;而另一个百岁老人,一个退休的裁缝正在帮人们补衣服,教别人如何缝纫,进行职业治疗。”
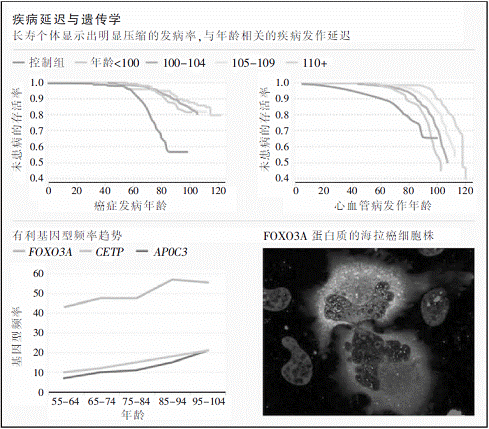
但是研究数据日益显示,达到如此高龄的老人正获得“生物学上的援助之手”。例如,波尔斯最近的研究支持了一个被称为“发病率压缩”的假设,这个假设是指寿命比平均寿命长得多(至少100岁)的个体趋向于能更长久地保持健康,与年龄有关的疾病比如癌症和心血管疾病的发病时间会延迟。“这些疾病直到他们生命的大约最后5%的时间才会出现。”波尔斯说。若事实如此,那么对极其长寿现象的研究将使医学家洞悉许多常见疾病的病理并且找到与之对抗的新方法。
抵抗衰老的“盔甲”
评估遗传对普通人群健康衰老之贡献的很多重要研究都是在斯堪的纳维亚做的,那里有和平的政治环境和完善的社会基础设施,使其他地方的那些过早缩短人寿命的外部因素的影响最小化。“过去100年来,我们基本上达到了研究人类的实验室条件。”卡里·克里斯坦森(Kaare Christensen)开玩笑说,他是欧登塞的南丹麦大学的一位专门从事人类衰老研究的遗传流行病学家。克里斯坦森从异卵和同卵双胞胎的研究中发现,大约25%的长寿可归因于遗传因素。而且,他怀疑这种遗传贡献有一种明确的年龄依赖关系。“在60岁以前,遗传因素在我们研究过的人群中并不是那么重要的因素,”克里斯坦森说,“但是60岁以后,遗传因素的影响会增加,而且在非常高的年龄则似乎变成最强的因素。”换句话说,健康的生活方式和环境对于大多数人是否能活到70岁是关键的决定因素,但是70岁之后能否长寿就日益取决于他们的基因了。
然而,健康的生活方式可能并不是对于每个想长寿的人而言都是必须的。许多研究衰老的专家现在相信那些百岁老人拥有有益的遗传因素能保护他们历经生命中的衰老变迁。唯有超过了一定年龄――当不太幸运的人的健康开始衰退时――这些遗传因素才显现出来。
纽约的阿尔伯特·爱因斯坦医学院的老年医学专家尼尔·巴尔齐莱(Nir Barzilai)是这个领域的重要研究者。他对一大群德系犹太人进行了很多年的跟踪研究,试图理解是什么使极其高龄者与他们的同辈区别开来。“我们研究了2 500人,年龄分布在60岁到112岁之间,其中年龄在95岁以上者有将近600人。”巴尔齐莱说。他的目标是找出那些在最老的人群里比在那些只活到平均寿命的人身上更常见的基因组变量。“大多数基因型在频率上并不发生改变,因为它们与寿命无关,”他说,“因此,那些频率确实会发生变化的基因型要么因为它们杀死人类而下降,要么因为它们促进长寿而上升。”
有人可能会期望这些“长寿基因型”是完美切合健康的,即没有与增加疾病风险有关的变量。但是若干研究结果表明事实并非如此。例如,“莱顿长寿研究”发现一群90多岁老人的基因组与一群作为控制组的年轻人的基因组一样,可能包含导致癌症、糖尿病和其他疾病的同样的风险因素。这意味着长寿基因组中的其他变量以某种方式使它们的主人免受那些潜在的有害基因的影响――克里斯坦森在家族研究中也观察到了这种影响。“在丹麦,我们发现长寿者的孩子与其他人相比罹患癌症的概率要小25%。”对巴尔齐莱而言,像这种模式表明了极其高寿者的基因组可能为临床医学研究者理解健康如何随着时间恶化提供指导。“真正控制我们的衰老速度的,”他说,“是保护机制和保护基因。”
搜寻开始
对于大多数具有遗传因素的疾病而言,搜寻起作用的基因是以全基因组关联研究(GWAS)的方式进行的。这本质上是一种对个体变量――单核苷酸多态性(SNPs)的摸底调查――这在具有感兴趣的性状的个体上和在控制组的个体上,从统计上而言是差不多相同的。但是,为了避免给研究者带来错误的有利结果,研究者为目标结果设置了一个很高的门槛。而且,要发现罕见因素或是作用不大的因素几乎是不可能的,因为它们在一个大样本研究中可能呈现为噪音。“一个单一的遗传变量或者甚至是一组遗传变量有足够大的影响在全基因组关联研究中脱颖而出,独立地与长寿有关,是非常不可能的。”波尔斯说。
为了避开这个问题,波尔斯和他在波士顿大学的同事保拉·塞巴斯蒂亚尼(Paola Sebastiani)开展了一种不同的全基因组关联研究。他们并不是关注个体的SNPs,而是关注群体的SNPs,寻找似乎在长寿个体中发挥协同作用的遗传变量,这些遗传变量受个体差异的影响很微弱。这些单核苷酸多态性群体可能后来会显露对基因组的依赖性――一定是一起起作用的一组变量――这就建立了一个保护性的有利于长寿的生物环境。波尔斯和塞巴斯蒂亚尼发现了许多这种“指纹”,但是他们2010年的论文却在一年后被《科学》杂志撤销了,因为技术错误使他们的分析受到了质疑。波尔斯和塞巴斯蒂亚尼研究组与美国康涅狄格州纽黑文市的耶鲁大学遗传流行病学家合作解决了这些技术问题,并在2012年的《公共科学图书馆―综合》上重新发表了他们的研究成果。波尔斯承认论文撤销给他们的研究笼罩上了一层阴霾,但是他支持他的研究组的发现:一组281个单核苷酸多态性与至少130个在百岁老人身上似乎显著富集的基因有关。“有一组遗传变量一起很可能互相影响并与环境相互作用对这些极其长寿者产生了重要的影响,”波尔斯补充道,“随着研究对象的年龄越高,这个研究模型的准确性也变得越高。”
这项研究中发现的若干基因在动物研究模型中也出现了。确实,动物研究的数据大体上在揭示人类遗传变量与健康衰老的关系上比全基因组关联研究(GWAS)更为有效。在人类研究中一个复现率最高的关联基因是一个叫做E4的载脂蛋白E基因,它并不与长寿有关,而是与虚弱有关――不可理解的是这个遗传变量极大地增加了罹患老年痴呆症和心血管疾病的风险。但是,有些研究者单纯地把它视为一个疾病风险因素,并不情愿称其为一个真正的“衰老基因”。至于衰老基因,基因中的遗传变量编码了一个被称为叉头框O3A(FOXO3A)的调节因素――是人类身上与调节蠕虫寿命的基因daf-16作用相当的基因――一而再再而三地与各种人群的寿命有关。“这个基因在汉族中国人、日本人、德系犹太人、南欧人和德国人身上都一再复现,”德国基尔的克里斯蒂安-阿尔布雷希特大学的健康衰老研究组的负责人斯蒂芬·施雷伯(Stefan Schreiber)如是说,“这意味着遗传变量的起源一定非常古老。”FOXO3A是控制生长和新陈代谢活动的一组信号通路的一部分。在进一步支持新陈代谢通路对衰老的重要性的研究中,巴尔齐莱在德系犹太人中也发现了相似的结果。尤其是,他找到了在基因中编码了参与类脂化合物代谢作用的降低功能性胆固醇酯酶转运蛋白(CETP)和载脂蛋白C3(APOC3)含量的两种蛋白质的遗传变量。“它们看起来发挥了长寿基因的作用――这些变量在60岁老人中的复现频率是8%-10%,在百岁老人中的复现频率则大概是20%。”巴尔齐莱说。

那些活到很老而仍然享受健康的人可能有遗传优势
然而,百岁老人的研究困难重重。例如,这里有一个控制组的问题:百岁老人经历了环境和生活的诸多变化,这些并不一定和现代人群相匹配。“如果你研究1910年出生的百岁老人,实际上你需要的研究人群是那些同样在1910年出生并且50岁时去世的个体,而要做这种研究几乎很少甚至根本没有可获取的DNA。”尼古拉斯·朔尔克(Nicholas Schork)说,他是美国加利福尼亚州圣地亚哥市斯克里普斯研究所的一位生物信息学家。另一方面,当代医疗手段和饮食的极大改善意味着成为控制组的人群中可能隐藏着秘密的百岁老人――那些有着普通的基因型在今天可以活到百岁高龄而在条件艰苦的年代本来很可能更早就去世的幸运者。“我打赌,控制组中只有一小部分人将活到非常老,”波尔斯说,“但是实际上可能有比以前我们想象的还要多的人能活到100岁。”
超级老,超级健康
研究者们正在制定更加精明的策略来找出支持长寿的生物学因素。施雷伯的研究组就是开始关注“超级百岁老人”――那些活到110岁高龄的稀有个体的研究者之一。“我们正开始研究极其长寿者,并且运用我们所有的基因组和基因研究工具以真正深入地进行探索。”施雷伯说道。他提到他已经成功运用这种方法研究克罗恩病:通过专注于研究那些在极小的年纪就患克罗恩病的孩子,他发现了若干致病的遗传因素。
另一种方法是寄希望于发病率压缩模型,关注那些“生物学意义上很年轻”的80多岁和90多岁的个体。朔尔克参与的斯克里普斯研究所的威尔德利研究就是这种研究思路。“如果有些人80岁了还像50岁的人一样健康,那么研究他们能够为我们研究是什么原因使人们长寿提供线索。”他说。
至于全基因组关联研究(GWAS),从人群中找出可能的长寿基因的困难一部分来自于科学家撒的网太广了。考虑到长寿基因的大部分好处可能是在我们养育子女之后才发挥作用,那么这些遗传变量很可能缺乏进行扩散的进化动力,而只是作为“传家宝”从父母传给孩子。这当然有事实依据――例如,卡恩的三个兄弟全都活到了100岁以上。因此,若干研究组和团队工作,比如受到美国马里兰州贝塞斯达美国国立老化研究所(NIA)支持的多国长寿家族研究项目,正在试图更好地掌握这种家族遗传关系。“我们正在研究长寿者密集的家族,我们用他们的配偶作为控制组,”克里斯坦森说,他是这个研究项目的研究者之一,“我们对这些个体进行了全基因组关联研究,现在我们进入到测序阶段。”
随着测序技术变得越来越便宜和越来越强大,它有可能成为遗传研究领域的一项关键技术。“我认为直到我们能分析和破译我们的百岁老人的全部基因组序列,才会有重大进展。”朔尔克说。巴尔齐莱早就对这个方法感兴趣了:他的研究组提议资助对百岁老人进行全基因组测序,却未能得到NIH的支持,但是最终却为他们赢得执政官基因组X奖奠定了基础。这个竞赛将奖励能够为百岁老人志愿者(被称为“百个百岁老人”)进行最快最好最便宜的测序的基因测序团队一千万美元的奖金。这个测序努力继续得到了来自巴尔齐莱和波尔斯的支持,这两位科学家都认为这是一个很好的开始。“一百个人并不是一个足够大的研究样本,”波尔斯说,“但是这是朝着正确方向迈出的了不起的一步。”
但是,巴尔齐莱告诫不要把遗传分析本身视为研究的终点。他想看到遗传变量是如何转化成生理影响的,比如一个人的新陈代谢指标的变化直接反映了他们的健康状况。“譬如测量血液中的某样东西,然后就能告诉我们疾病是否与之有关。”他说。他指出尽管在不同的基因中可能有很多遗传变量,但是它们可能都产生延长寿命的相同结果。“我们的所有研究结果都与某种表型有关,”巴尔齐莱说,“功能性胆固醇酯酶转运蛋白(CETP)的表型是CETP的含量降低,载脂蛋白C3(APOC3)的表型是APOC3含量降低。它们两者的表型则是胆固醇含量发生变化。”他进一步提出尽管在若干遗传学研究中,FOXO3A的遗传变量都与长寿有关,但是它们的生理影响还有待揭示。
幸运的是,还有许多其他的可能,对老人的健康进行纵向研究能提供与基因型的研究结果进行比较的表型数据。这包括了两项从2000年开始在旧金山的加利福尼亚大学进行的骨质疏松症研究,其中一项关注男人,另一项关注女人。“那些研究对象中许多人已经去世了,因为他们活到了70多岁和80多岁,”波尔斯说。“但是他们碰巧与我们的百岁老人的孩子们差不多是同一时期出生的,而这些百岁老人的孩子们绝大部分都还活着。”
尽管有这么多困难,欧洲和美国的研究者们都还受限于缺乏对长寿研究的资助。例如,受到NIA支助的长寿研究联盟,开展了许多关于人类老龄化的遗传研究,却仅仅依靠有限的并且在缩减的预算运转着,朔尔克说。另一方面,这个领域从NIH前院长弗朗西斯·柯林斯(Francis Collins)那里获得了有力的支持。柯林斯是NIH的基因科学兴趣小组背后的推动力量,这个小组把衰老设想成许多疾病之间的一个重要联系。根据这个观点,理解衰老可能指示了治疗或者预防一些被证明除此以外很难克服的疾病的一个切入点,比如老年痴呆症和心血管疾病。“你体内有比你实际得病还要多的疾病遗传易感性――因此使一种疾病显现或是保护你的遗传机制就变得极为重要了,”施雷伯说,“研究长寿就是探究这种遗传机制的一种方法。”
资料来源 Nature
责任编辑 彦 隐