通过遗传连锁研究,识别了一种与结肠癌敏感性有关的新基因,其作用方式,可能是打乱基因组的平衡。
医师们早就清楚,在某些家庭内,有易患诸如乳腺和结肠癌等癌症的趋势。观察结果显示,虽然饮食和其他环境因素影响癌的发展,但也不可否认,对该病的敏感因素,也能遗传。过去几年来,可造成这些敏感性的基因,已成为遗传学家们最广泛寻查的目标。如今,刊登在这期《科学》上的文章,提供了有力证据,说明造成结肠癌敏感性的,可能是一种重要的新基因。
人们希望把新基因作为一种工具,对具有高风险率的个体进行癌前检查,最终减少该病的发生,在当今美国,每年都有约55000人死于该病。这一敏感性基因的共同发现者之一,芬兰赫尔辛基大学的夏佩尔和约翰。霍普金斯大学医学院的沃格尔斯坦估测,在200位西方人中,就有1人携带着这种新基因。所占的比例,较导致很普遍遗传病,如囊纤维变性的基因频率,要高出10倍。“可以确定,如果说这个新基因不是唯一最普遍的话,起码也是最普遍者之一”夏佩尔说。
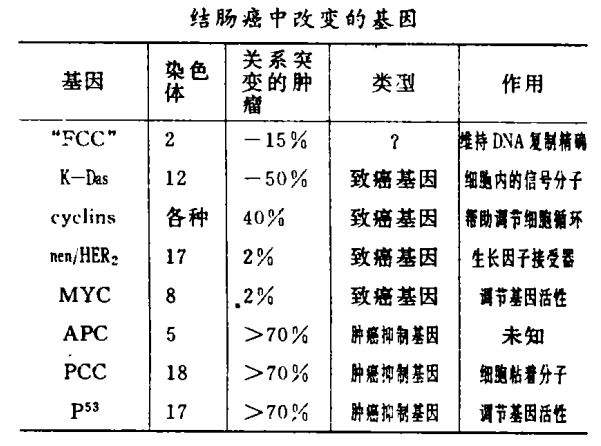
而且结肠癌敏感性基因,可能具有新的活动方式。夏佩尔-沃格尔斯坦小组和至少另外两个研究小组都已表明,结肠癌细胞显示出高度的遗传不稳定性,标志是在整个基因组内遍布着突变,暗示着是敏感性基因导致了不稳定。而在几个基因中的突变,与遗传性结肠癌和被认为无遗传源的大量“偶发性”癌的发展息息相关。这些活动,没有一种完全一致(见表)。事实上,在结肠癌内,新基因所在基因组的不稳定性,可能受到至少另外某些基因变化的影响。
无论是在临床上,还是在实验室内,新基因是结肠癌的象征。所以这一发现,招致了其他研究人员的关注,虽然尚未分离到这一基因本身。“它非常令人注目。这些文章将产生极大的影响,”在国家卫生研究院,人类基因组工程国家中心担任领导的科林斯说。在麻省的坎布里奇,怀特海研究所里的兰德也有同感,热烈欢呼这一发现是:“过去一年里,人类遗传学上最激动人心的发展,”
漫长曲折的探索之路
夏佩尔-沃格尔斯坦所经历的,大约是4年前开始的一条曲折的探索之路。沃格尔斯坦因探索造成结肠癌发展的基因变化而颇负盛名。他是导致被称做家族性腺瘤息肉瘤(FAP)病的遗传前质基因的共同发现者之一。
该病患者发育许多结肠息肉,其中有些继续形成完成的癌肿瘤。但FAP很少见,仅占结肠癌病例的1%;更常见的,有15%的病例,是在家庭中发作,即使这些家庭成员不具有息肉或先质的其他明显标志。家庭成员还倾向于患其他癌,包括子宫内膜、卵巢、肾癌在内。在这些家庭内,似乎是显示出一种遗传敏感性趋势。但也同时出现了一些有争议的问题,因为这些家庭成员,也同时担负着饮食和其他环境因素的责任。1989年,沃格尔斯坦和夏佩尔进行协作研究,试图以不可置疑的方式,即通过鉴别基因,表明这些家庭内,确存在敏感性。
开始进行的遗传研究,目的是测定在这些家庭中结肠癌和其它癌症,与已知影响癌病发展的基因是否有联系,这类基因包括P53、Dec以及引起FAP的APC基因。这些连锁研究,并无什么结果:“与已知基因不存在任何联系,它们逐个被排除了。”夏佩尔说。这就使得问题更加复杂了。当时研究人员进一步扩大了研究,结合可能永久存在于患结肠癌或其它癌的家庭成员中的整个基因组中的标志,但在未患癌的成员中,这些标志是不存在的。如果标志和疾病之间的这种明显连锁可被找到的话,它将说明,标志处于或接近成因基因的位点上。
研究人员集中对两个大的家庭进行了追踪探索,一个来自北美洲,而另一个来自新西兰。夏佩尔、沃格尔斯坦及其同事,检查了250个标志,结果还是一无所获。“当时,我们真正开始怀疑,我们的追踪路线是否对头?”沃格尔斯坦说,有一位27岁的家庭成员患了结肠癌,对于该病的发展,这个年龄是非常年轻的,沃格尔斯坦说:“这给了我们极大鼓励,说明这些家庭中,确实存在著致病的遗传成分。”
夏佩尔说,约在同时,有效的重要新手段出现了,由在法国巴黎的韦森巴赫的小组和在威斯康星州,马什菲尔德医学研究基金会里的韦伯所发展了一组新探针。这些新探针,用于测定所谓的“微随体DNA”,即遍布整个基因组的短的重复DNA顺序。在个体与个体之间,这些顺序的长度变化很大,作为遗传连锁的标记,它们能提供高度的信息。最后,在对345个标记进行了全部检验之后,研究人员集中了寻查的目标:把位于2号染色体上的一个微随体标记和家族性结肠癌联系在一起,国家癌症研究所的癌症遗传学家哈里斯评论道,那确实是出人预料的,因为结肠癌基因所处的这个位置“直到目前还无人怀疑。”
当夏佩尔-沃格尔斯坦的小组,开始对他们在研究着的遗传缺失的性质进行更深入探索的时候,出现了更加令人吃惊的现象。因为没有其他基因与遗传性癌症敏感性有联系,包括APC基因在内,这些都是典型的肿瘤抑制基因。研究者们开始推测,新基因也许是一种肿瘤抑制基因,其作用是阻止细胞的生长,但当因突变而丧失或失活时,阻碍生长的功能丧失,致使恶性肿瘤形成。典型肿瘤抑制基因的标志之一。就是在肿瘤细胞内,两个拷贝至少丧失一个。
但是夏佩尔-沃格尔斯坦的小组,在由家族性结肠癌的2号染色体标志鉴定的区域内,并未发现有任何缺失。研究者们所发现的,是完全不同类型的异常性。在不同肿瘤内,处于2号染色体标位点上的微随体DNA,其长度是变化的,指示它已经丧失或获得了核苷酸,更令研究者们吃惊的是,在他们所分析过的几乎全部家族肿瘤样品内的另外几个染色体位点上,他们看到了微随体DNA相似大小的变化。
支持性证据
并不是只有夏佩尔-沃格尔斯坦的小组发现微随体不稳定。施堡顿(Thibodeau)和其同事在进行自己的研究工作时,并不知道其它小组的发现。在他们所检验的90位结肠癌中,发现微随体高度变异者有13位,另有12位显示了小得多的变异。
因为不同的小组观察到了微随体标记的不同样品,综合其结果显示,在基因组中的这一区域内,遍布了突变。沃格尔斯坦说,“真正有意义的事,是在整个基因组内,确有上千种变化出现。”它们的出现,绝不可能是独立现象。说明在结肠癌细胞内,作为整个DNA的编码是不准确的;显然是由于基因突变,造成了DNA复制期间的大规模的错误。正如施堡顿所指出的:“我们习惯认为,是简单活动造成了遗传病。但在这里,我们所碰到的事件,可能是由单一基因造成的突变,影响到整个基因组的活动。”
现在,假定结肠癌敏感基因是处于由夏佩乐-沃格尔斯坦小组所鉴别的2号染色体位置上,并假定FCC(家族性结肠癌)是一种应受到谴责的基因。至少是在被称做家族起源的结肠癌中负有责任,而且,它也可能在某些“偶发性”结肠癌中起作用。当夏佩尔-沃格尔斯坦的小组在“偶发性”结肠癌中观察到微随体不稳性时,他们并不知道施堡顿所研究的肿瘤是家族起源。他们发现这种肿瘤占13%(检验过的46名中有6名),这一比例,和梅奥小组的结果相似。沃格尔斯坦说,这些结果可能意味着与不稳性有关的肿瘤,终归是导致于以前未曾预料到的遗传敏感性。
的确,两个小组的发现提示,微随体不稳性的存在,把关系共同起源和性质的结肠癌,划为不同的两个亚组,由家族性肿瘤和偶发性结肠癌所确定的临床特征,夏佩尔-沃格尔斯坦和施堡顿小组所发现的不稳定性是类似的。例如,这些不稳定性,主要是出现在离直肠最远的结肠片段内。施堡顿的工作结果也提示,比起结肠癌来,它们不可能是致死性的。
但是,现在的新的工作结果,所提出的疑问,远比其解决的问题要多。其中最大疑点是:2号染色体的性质是什么?它又是如何可影响到DNA的精确复制呢?夏佩尔-沃格尔斯坦指示,它可能是为DNA复制所必要的因子编码。当然,解决问题的唯一方法,是把这个基因找出来。这将要花费多长时间,却是难以预料。夏风尔说,其标志,至少可以暗示出该基因的位置。对于研究者而言,无疑是一种意外收获。但是,这个位置宽达9分摩,大约为900万个碱基对。
同样重要的是,由该基因所诱发的突变,是如何导致结肠癌的问题。一种可能性是,它们诱导APC或其它基因的变化,这些变化,已由沃格尔斯坦和其他人在结肠癌中测定到了,证据仍是初步的,但沃格尔斯坦评论说,他们已在癌前结肠瘤中,发现了微随体的不稳定性, · 说明这些改变发生的很早。
一旦研究者们分离了该基因本身,就可以应用它对人群进行大规模筛选,以便观察是谁在遗传它,这可能对于降低死亡率有益。正如沃格尔斯坦所说:“如果癌症被尽早发现的话,在总体上,就可预防来自结肠癌的死亡,”
[Science,1993年5月7日]