卢大儒
复旦大学生命科学学院特聘教授
基因技术教育部工程研究中心主任
基因技术助力解密新冠病毒,对研究病毒感染机制、疫苗和药物开发具有重要指导意义。
2019年底起至今在全球肆虐的新冠肺炎突如其来,来势汹汹,究竟是怎么回事?人们是怎么迅速找到不明原因肺炎的病原体的?这种病毒为什么具有很强的感染性和致病性?为什么又狡猾多变?如何能够快速诊断出患者,甚至发现无症状的携带者? 又是如何研发出针对性的疫苗,预防病毒的感染的? 这一切均离不开基因与基因技术。
基因技术及其四个最重要、最基本的代表
基因是建造大楼的“图纸”,也是长成参天大树的“种子”,是生命的密码、生命的本质、生命的语言,也是最基本的因素。而生命是基因的活动和表现形式,是基因的舞台。历史上,多少基因在“生命舞台”上表演过,又有多少基因在经历风雨的洗礼后逐渐“逝去”,没有永远的主角。生命永远绚丽多姿,而基因是生命的中心,一切都是为了DNA的复制、传承。
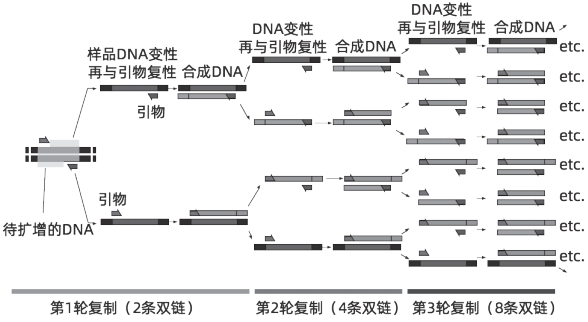
基因技术有四个最重要、最基本的代表,也是基因技术的“四驾马车”:一是重组DNA技术,这个技术就是把不同来源的DNA、分子进行重新组合,是当时最早实现基因重组的一种技术方法;二是DNA聚合酶链式反应(PCR)技术,有了PCR技术,研究人员可以在1~2小时内,在试管里将基因放大数百万倍;三是DNA测序技术,它是阅读生命基因、解码生命最重要的一种技术;四是基因编辑技术,它可以准确地修改基因,对于基因的功能研究、物种改良、基因治疗都非常重要,也是近几年生命科学研究的热点。
2020年是特殊的一年,新冠肺炎疫情在全球肆虐。其实在疫情发现之初,科研工作者借助基因技术就逐步揭开了新冠病毒背后的秘密,如追寻新冠肺炎病原体、助力新冠肺炎诊断及新冠肺炎疫苗和药物开发、探究新冠病毒感染与致病机制等。
追寻不明原因肺炎致病元凶立头功
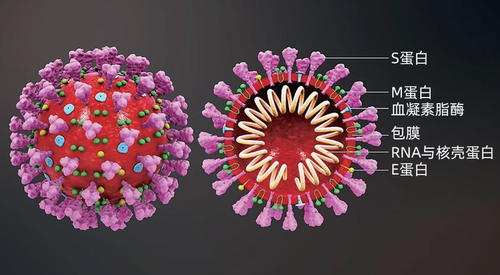
新冠病毒呈球状,直径约为100~140纳米。基因组为约有3万个核酸的单股正链RNA,为最大的RNA病毒之一。
2019年12月24日,武汉市某医院将一名来自华南海鲜市场不明原因肺炎患者的肺泡灌洗液样本进行二代测序(NGS)。NGS是一种高通量测序方法,可以对生物样本的DNA或RNA样本的碱基对进行快速测序。3天后,检测和分析人员就通过NGS和生物信息比对迅速发现该未知病原体与急性呼吸综合征冠状病毒(SARS-CoV)的相似度约81%,结果显示这是一种新的冠状病毒。这种病毒从核酸序列上比对分析,与当年的SARS-CoV非常相似。应该说,NGS测序技术在这次新冠肺炎病原体锁定中立了头功。 此前,若想破解不明原因的病原体要花费大量的时间,更多的人力物力,而现在通过NGS对病原体测序并与信息数据库比对,只需要3天,甚至更短的时间即可确定此次病原体为一种新的冠状病毒。
PCR技术
基因测序技术在发现不明病原体的过程中发挥着重要作用。NGS测序发展迅速,应用广泛,成本急剧下降,得到的数据量也越来越大,这也意味我们已经进入了基因组时代。基因测序技术在今天迅速普及,能够让研究人员迅速地认识、挖掘、锁定不明原因传染病中的病原体。值得一提的是,现在采用微小的只有U盘大小的第三代纳米孔测序仪,可以在现场花数小时就能发现疾病样本中不明原因的病原体。
这次的新冠病毒感染能力远超当年的SARS,如果还是像当年那样,要经过半年才鉴别出病原体,那后果不堪设想。幸亏,NGS在当今能够迅速发展和应用,真是天佑中华!
解决新冠肺炎快速精准诊断难题
病原性疾病的病原体检测是预防和治疗的关键,机体在病毒感染后会产生特异性抗体,免疫学检测就是检查其特异性抗体,这是病原性疾病诊断的重要方法。然而,由于病原体感染存在窗口期,往往是感染后1~2周内,难以早期诊断。 此外,对一些病原体,我们还有很多未知,更是无从下手。
任何病原体均有独特的遗传物质,所以基于此进行的基因检测(又称核酸检测)具有简单、灵敏和特异的优点,可用于感染性疾病快速而准确的检测。由于基因检测的灵敏特异性,病原体早期的感染也能够检测到,不存在窗口期。因此,核酸检测成为病原体检测的首选和金标准。
尽管核酸检测会出现“假阴性”的问题,但依然是不可缺少的金标准。同时,临床上要加强核酸检测的各种质量管理和控制,克服各种不确定因素,最终让核酸检测更加快速、灵敏、稳定、安全、方便、简单。
基因检测技术有很多,如分子杂交法、PCR技术、等温扩增技术、第一代DNA测序方法、原位杂交与荧光原位杂交(FISH)技术、基因芯片检测法和高通量测序等,这些技术在不同疾病诊断当中发挥重要作用。
在临床应用中,荧光定量PCR和等温扩增检测在这次新冠病毒筛查和诊断中发挥了重要作用,不仅能够将患者准确检测,而且可以将无症状感染者筛查出来, 国家食品药品监督管理总局采用绿色通道批准了一批这方面的核酸检测试剂盒上市,能够在0.5~2小时内完成检测,不少试剂盒可以免提取核酸直接检测。
助力疫苗开发,预防和阻断病毒感染
病原性疾病的根源在于病原体,自然界宿主对入侵病原体也有各种招数应付,其核心招数是通过机体的免疫识别和应答。例如,限制性内切酶、Cas核酸酶、RNA干扰(RNAi)等都是对外界病原体在核酸水平上进行特异的识别并清除。高等生物则发展了专门的在蛋白质和细胞层面上的免疫系统网络,包括先天免疫和特异性免疫。与疫苗直接相关的就是通过体内B淋巴细胞产生针对病原体的特异性抗体。
疫苗是将病原体及其代谢物,经过人工减毒、灭活或利用基因工程等方法制成的用于预防传染病的免疫制剂。疫苗保留了病原菌刺激动物体免疫系统的特性。接种疫苗后,当机体再次接触到这种病原时,免疫系统便会识别并阻止病原菌的伤害,其核心是通过诱导产生特异抗体。疫苗的发明是人类历史上具有里程碑意义的事件。控制传染性疾病最主要的手段就是预防,而接种疫苗被认为是最行之有效的措施,所以预防新冠肺炎最重要的手段就是研发疫苗。
新冠疫情暴发后,中国立即布局了五条技术路线研发疫苗:一是灭活疫苗,制备新冠病毒并进行灭活,经过安全性、有效性评价以后就可以用于临床试验,这是经典的病毒疫苗制备方法;二是重组基因工程疫苗,通过基因工程大量生产新冠病毒刺突糖蛋白(S蛋白),并将其注射到人体产生抗体;三是腺病毒载体疫苗,用腺病毒作为载体,表达新冠病毒S蛋白,重组的腺病毒可以高效感染人体,刺激机体产生抗体;四是核酸疫苗,主要是mRNA疫苗,用脂质体纳米颗粒(LNP)等材料包裹核酸,注射到人体内,可以表达出S蛋白,并刺激人体产生抗体,抵抗感染;五是流感病毒双重疫苗,以国内上市减毒流感病毒疫苗为载体,携带S基因,既可以预防新冠病毒,又可以预防流感。
由中国军事科学院军事医学研究院陈薇院士带领的研究团队和康希诺生物股份公司联合开发的重组新型冠状病毒疫苗(腺病毒载体)于2020年3月份在国际上最先进入临床试验。美国莫德纳公司(Moderna)成功研制出针新冠病毒的mRNA疫苗,也最早进入了临床试验。
从2020年底起陆续有疫苗获批进入临床使用;到目前为止,国际上已经有十多种疫苗获得紧急授权使用,包括美国莫德纳公司的mRNA疫苗,美国辉瑞公司和德国BioNTech公司联合研发的mRNA疫苗,强生公司的腺病毒疫苗,英国牛津大学与阿斯利康公司联合研发的腺病毒疫苗,俄罗斯加马列亚国家研究所研发的“卫星-V”腺病毒疫苗等。
中国从2020年底至今在第一时间批准了国药集团和科兴公司的3款灭活新冠病毒疫苗,今年先后批准了康希诺公司等单位研发的腺病毒疫苗和安徽智飞龙科马公司等研发的重组亚单位蛋白疫苗。复星医药与德国BioNTech公司合作的mRNA疫苗在香港和澳门获准紧急使用。这样,中国一共有6种疫苗获批紧急授权使用。
除了灭活疫苗制备以外,其他各种疫苗研发均离不开基因技术,是在基因重组等技术基础上开展研发的;如果要研发针对各种新冠病毒的变异体的疫苗,无论哪一种疫苗研究均离不开基因技术。根据病毒变异,借助基因工程技术,可以迅速地改变S蛋白基因序列,制备出针对变异病毒的各种疫苗。
基因技术推动新冠病毒药物研发
新冠肺炎是一种新的疾病,致病机制尚需进一步研究,且缺乏有效药物,基因技术又该如何助力特异药物的开发?基因技术主要从以下几个方面助推新冠病毒药物研发:加速致病机制研究,揭示病毒的结构特征,明确药物靶点;帮助建立病毒感染计算,蛋白、细胞模型以及药物筛选模型;帮助建立新冠肺炎动物模型,开展药物安全性有效性研究;通过制备病毒蛋白,筛选抗体,进行安全评估研究。
目前,研究人员发现新冠病毒有29种蛋白,针对这些蛋白,他们进行了结构功能性研究、药物设计和筛选。其中,根据病毒生活周期,药物筛选策略包含以下几个方面:一是设置拦路虎,抑制病毒进入细胞,如通过靶向小肽、小分子和中和抗体对病毒表面的刺突糖蛋白进行封闭;二是断粮草,抑制病毒蛋白酶活性,如PL、3CL蛋白酶抑制剂,阻止病毒的转录、翻译;三是以假乱真,抑制病毒RNA依赖RNA聚合酶活性,如瑞德西韦(Remdesivir)就是一种抑制病毒RNA复制、转录的一种核苷酸类似物;四是寻求其他靶点,抑制病毒融合、包装、转运,如弗林蛋白酶(Furin)抑制剂、跨膜丝氨酸蛋白酶(TMPRSS2)抑制剂等。
新冠病毒的模型图及解剖照片
不同新冠肺炎患者的症状与治疗效果千差万别,重症患者、轻症状患者、无症状患者差异很大,产生差异的原因很多,如年龄问题、其他伴随疾病、治疗方案、病毒感染数量的多少以及病毒在患者体内的变异程度、患者的遗传基因多态性等,基因技术有助于我们揭示新冠病毒感染和治疗的差异因素,更好地实现精准医疗。
探究新冠病毒感染与致病机制
新冠病毒是如何感染人的呢?依托于基因技术和其他分子细胞生物学方法的研究发现,新冠病毒借助其表面的刺突糖蛋白(S蛋白)与人体细胞表面血管紧张素转化酶2(ACE2)结合,同时S蛋白会被跨膜丝氨酸蛋白酶(有辅助病毒感染的作用)裂解,进而激活。
针对ACE2,研究人员系统地开展了相关性研究,用于阐明病毒感染的动态机制,指导精准医疗。美国得克萨斯州大学的研究人员借助低温冷冻电镜技术解析了新冠病毒的刺突糖蛋白,新冠病毒通过与SARS病毒相同的受体ACE2进行感染和传播。我国西湖大学的研究人员成功解析了新冠病毒感染受体ACE2的全长结构,对研究病毒感染机制、疫苗和药物开发具有重要指导意义。
通过病毒序列的研究,南开大学的研究人员首次发现,此次的新冠病毒S蛋白中多了一个新的功能域位点——弗林蛋白酶切位点。正是由于这一包装机制的改变,新冠病毒刺突糖蛋白获得了更高的侵染细胞的效率,这可能也是其传播能力强于SARS-CoV的一个原因。
通过对人体细胞ACE2基因表达分析,发现新冠病毒除了感染肺部以外,也可能感染其他组织器官。例如,感染患者有些伴有腹泻等消化道症状,在粪便中检测到新冠病毒。病毒可能从血液中转移到肠道内。神经细胞也可能是感染区域,患者可以出现嗅觉和味觉失灵。通过进行单细胞RNA测序(RNA-seq)分析发现,气道、食道、肺、心脏、肾、回肠和膀胱都是ACE2高表达的组织和器官,所以要对这些器官加强保护。
新冠病毒的突然出现和肆虐,给人类社会敲响了警钟:非常原始简单的病毒可能对人类世界造成毁灭性的打击,我们要全面加强病毒的防治研究,同时也要审视暴露的各种问题,重视基因技术在病原体预防诊断和治疗研究中的生物安全防控。