老鹰具有凌空捕捉小兔的千里眼,金鱼的视神经能够在受损后再生,神奇的造化安排了许多不可思议的自然现象。但作为万物之灵的人类,反倒视觉脆弱,既无鹰视之锐利,亦无再生之能力。在医学高度发达的21世纪,心、肝、肾都可以移植的今天,唯独人眼和人脑是不能够移植的,究其原因在于人类视神经不能有效再生,因而,当人类罹患青光眼、视神经炎、黄斑变性或外伤等,造成视神经变性,引起视力的不可逆性继续损害,直至失明。
维持视觉的生理基础
视觉是人体感知外界刺激最重要的功能之一,视觉障碍直接影响到人类的生存质量,而维持良好的视觉有赖于正常眼球的光路通透和视路灵敏。在现阶段,造成视觉障碍的大多数光路系统(角膜-房水-晶状体-玻璃体)的病变,目前已经有了完善的治疗措施。比如,白内障患者可通过为其摘除混浊的晶状体并植入人工晶体而重见光明,因角膜病致盲患者可望通过角膜移植恢复视力,近视眼可通过戴镜或激光手术矫正视力等,光路系统致盲已成为可防治性盲。相对而言,随着社会老龄化等问题,凸现的是视路系统疾病难以防治的现状,视路病变的不可逆性进展成为失明的主要危险。
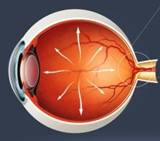
所谓视路,是指从视网膜及其轴索纤维构成的视神经,以及一路向上传递神经冲动直到大脑视觉皮层的整个通路(视网膜-外侧膝状体-视皮层)。其中,对于维持视觉至关重要的,是视网膜神经元的存活和视神经轴索的结构、功能的完整。视网膜内层由感光细胞(视锥及视杆)、双极细胞和节细胞组成。视锥接受强光刺激和辨别色觉,视杆则接受弱光刺激。当视细胞层感受光刺激后,将光刺激转变为神经冲动,传导到双极细胞层,再传到视网膜神经节细胞层,通过神经节细胞的轴突纤维组成的视神经、视交叉、视束、外侧膝状体、视放射,最后传到大脑枕叶视皮层产生视觉。促进视神经再生以及恢复其与脑神经联系,可以为视路疾病提供防治方案,因此具有重要的临床意义。
影响视神经再生的主要因素
所谓视神经再生是指存活的视网膜神经节细胞(RGC)生长出新的轴突到中枢神经系统的特定靶位置并恢复正常功能,它包含四层含义:神经保护、轴突延长、与靶组织再联系、功能恢复。目前,研究仍处在如何保护视神经和促进轴突延长上,而影响视神经再生因素主要包括以下三个方面。
1.再生抑制因素 视神经属于中枢神经,损伤后许多因素构成了抑制轴突延长的微环境,包括髓鞘相关抑制分子、神经胶质细胞形成的疤痕组织、神经营养因子的运输被阻断或减少等。其中,髓鞘相关抑制分子是一类轴突生长抑制因子,主要有Nogo、髓鞘相关糖蛋白(MAG)和少突胶质细胞髓磷脂糖蛋白(OMGP)。中枢神经系统胶质细胞主要为星形胶质细胞和少突胶质细胞,视神经损伤后,星形胶质细胞进行有丝分裂,分泌纤维蛋白,形成致密胶质瘢痕来包裹损伤区,这种胶质瘢痕使再生轴突不易通过,也被认为是造成视神经再生失败的重要因素。同时,星形胶质细胞和少突胶质细胞还会产生一些神经生长抑制因子阻碍轴突延长。视神经损伤后由于轴浆运输被阻断,造成神经营养因子的减少,也阻碍了其再生。
2.再生促进因素 视神经损伤后,也会产生一些促进轴突再生的因素,包括巨噬细胞、小胶质细胞的激活、神经营养因子的释放等。小胶质细胞被认为可通过清除髓鞘碎解物而改善抑制轴突再生环境。实验发现,大鼠晶状体损伤可明显促进视神经轴突再生,其机制与激活的巨噬细胞有关。同时,激活的巨噬细胞、Muller细胞、神经胶质细胞也会分泌许多神经营养因子,如神经生长因子(NGF)、脑源性神经营养因子(BDNF)、睫状神经营养因子(CNTF)、胰岛素样生长因子(IGF)等,促进视神经的再生。
3.视网膜神经节细胞再生潜能 视神经损伤后难以再生,很大程度上与节细胞自身的再生能力降低有关。在鱼等低等动物以及哺乳动物的胚胎期和新生期,视神经均可再生,而随着哺乳动物的发育成熟,RGC自身的再生能力逐渐丢失,视神经变得不可再生。交叉共培养实验表明,胚胎期大鼠视网膜可伸展轴突到达胚胎期和成年的脑组织,而成年大鼠的视网膜与胚胎期和成年的脑组织均不能延长轴突。一些特定基因如Bcl-2等随着大鼠发育成熟而高表达或低表达,造成了RGC自身生长能力的降低。
促进视神经再生的主要方法
近几年,围绕上述三大影响视神经再生的因素,展开了许多相关方面的研究,其中许多研究取得了不错的效果或者给予人们新的认识,为今后的研究和治疗提供了方向。
1.神经营养因子的使用 视神经受损后,多种细胞可以产生神经营养因子,这些营养因子能明显提高节细胞存活率,但大多不具有促进轴突再生的能力。CNTF在多个实验中被证实能明显地促进轴突再生,新近也发现促红细胞生成素和粒细胞集落刺激因子也能有效促进再生。虽然单个营养因子的使用不能有效促进视神经再生,但多种因子的联合应用却被证明具有较好效果,将成纤维细胞生长因子、神经营养因子3和脑源性生长因子联合使用,就比单独使用神经营养因子3效果显著,能产生明显的促再生作用,各种因子之间的不同作用机制有一定的互补性,使其表现出协同作用,而不仅仅是效果相加。
2.神经胶质细胞的应用 包括星形胶质细胞、少突胶质细胞、小胶质细胞等,胶质细胞在神经系统中发挥着支持、营养、保护、清除、转运等重要作用。在视神经再生方面,参与病理过程的主要有星形胶质细胞和少突胶质细胞,如同双刃剑,对视神经再生既有促进作用又有抑制作用,如何最大程度发挥其促进作用减少对再生的抑制已成为促再生研究的一个新热点。
3.干细胞的应用 在细胞替代方面,研究较多有胚胎干细胞、骨髓间充质干细胞、神经干细胞和神经祖细胞、嗅鞘细胞、诱导多能干细胞以及来源于眼球的干细胞和祖细胞,后者是目前较为成功的干细胞类型,可以在发育的不同阶段被分离出来,分化为节细胞特性的细胞,其中视网膜干细胞和祖细胞,可以从离体的胚胎期或新生期视网膜中分离,也可以从成人的睫状边缘区获得。在成人视网膜中还鉴定出了一个Muller细胞亚群,也具有干细胞特性是通过成纤维细胞重编程而获得,具有多种分化潜能,避免了干细胞应用的伦理问题。
4.调节细胞内信号通路 无论是周围环境对视神经再生的抑制还是各种因子对再生的促进,都是通过细胞内的信号通路传导而发挥作用的,而且RGCs自身的再生能力也与胞内信号通路有密切的联系。近年来的研究涉及mTOR通路、ROCK通路、调控KLF家族成员的表达、cAMP的作用等。因此,通过调节胞内信号通路,直接给予再生刺激,成为研究视神经再生的一个方向。
5.去除再生抑制因素 改善不利于轴突生长的微环境,去除抑制视神经再生的因素是最早的研究方向,近年来人们利用免疫学原理,通过抗体、疫苗等方法中和髓鞘相关抑制分子,尤其是OMPG、MAG、Nogo三种蛋白,去除其对轴突再生的抑制作用;还有研究证明,使用EGFR抑制剂能明显促进视神经再生。
6.电刺激的应用 神经元的电生理活动本身对神经元就具有刺激和保护作用,之前在高眼压、视网膜缺血、视神经损伤等模型中证明了电刺激能有效减少RGC的凋亡,对视神经具有保护作用。
主要问题及对未来的展望
虽然上述提到了许多种促进视神经的方法,但并没有一种能够取得明显的效果,而且大多数实验都只是动物实验,在人体的效果如何还有待进一步验证。在可操作性方面,上述很多方法操作复杂,如外周神经移植、神经营养因子的应用等,很难大规模应用。临床使用之前,许多方法的安全性、毒副反应也是要考虑的问题,如干细胞的应用、基因的调控等。即使能够成功使轴突再生,再生的轴突如何与脑组织形成联系、恢复视神经功能甚至恢复视力等都是必须要解决的问题。同时,上述问题也正是今后视神经再生研究和发展的方向,在真正实现人类视神经再生上我们还有很长的路要走。