在医院的血管外科,有一种疾病堪称“沉默的炸弹”——升主动脉扩张病。它会让心脏上方的主动脉壁像被吹大的气球一样呈现病理性扩张趋势,一旦在高压血流下破裂,或引发心肌梗死、脑梗,致死率极高。在美国,它是第八大致死病因,而我国发病率还高于西方。
面对这种凶险疾病,医生们却长期处于困境中:传统开放手术患者死亡率高达20%~25%,近三成患者因高龄、脏器缺血等无法手术;想做微创治疗,又因升主动脉“短而弯”的特殊结构,加上高压血流冲击下管壁大幅摆动,成了国际公认的难题,亟待科学家探索破解困局。
从临床困境出发,先闯“微创”难关
“病人等不起,我们必须找到更安全的治疗方式。”这是瑞金医院冯家烜教授团队最初的执念。作为国内率先开展升主动脉病变腔内修复术的团队之一,他们面对的第一个难题,就是如何在“短而弯”的升主动脉里,用微创方式植入移植物,重启血管功能。
升主动脉就像心脏通往全身的“第一主干道”,直径只有几厘米,却要承受心脏泵出的高压血流,还会随着心跳不断摆动。传统微创器械很难在这样的“动态环境”里精准定位,稍有不慎就可能引发大出血或脏器缺血。
研究团队仔细研究每一例手术的影像资料,经过无数次讨论和模拟操作,终于摸索出一套独特的分型方法,即给不同形态的升主动脉“分类贴标签”,针对每一类设计专属的手术路径和操作技巧。
2019年,他们将这些临床经验整理成文,发表在《美国心脏病学会杂志》(JACC,国际心血管领域权威期刊)上。这一研究成果为后续研究打下了关键基础。
传统模型“不达标”,转向基因编辑找突破
“以前用手术构建的升主动脉瘤模型,总觉得差点意思。”冯家烜教授回忆道。团队早期曾用“Cover-then-cut”手术法(先包裹主动脉,再切开制造扩张)构建大动物模型,成功率在当时已是全球最高,但问题依然明显:手术造出来的“病”,和人类自发的升主动脉扩张病差别很大。
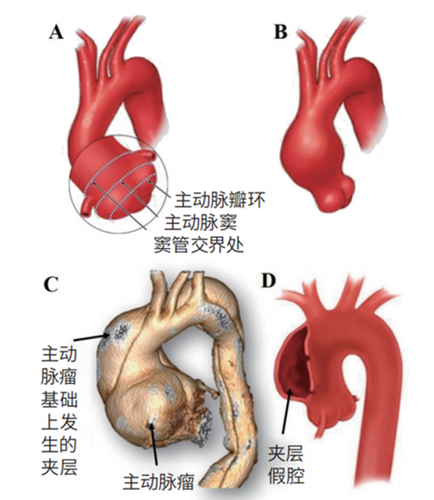
升主动脉扩张病常发于升主动脉段,是高危致命性疾病
最关键的缺陷在病理层面:人类患者的主动脉壁会出现弹性纤维断裂、胶原蛋白紊乱等“本质性病变”,而手术模型只是机械性地让血管扩张,管壁结构并没有真正“生病”。用这样的模型测试药物,就像在“模拟考场”里考试(考不出真实水平)——得出的结论可能与临床实际偏差极大,更无法解答疾病的遗传起源问题。
就在这时,基因编辑技术带来了新希望。
2018年,中国科学院脑科学与智能技术卓越创新中心周昌阳教授团队与冯家烜团队合作,用CRISPR/Cas9基因编辑技术,在小鼠身上敲除了FBN1基因的特定位点。
FBN1基因是个“关键选手”:它能合成原纤维蛋白-1,这种蛋白是主动脉壁弹性纤维的“骨架”。一旦FBN1基因突变,就会引发马方综合征——患者的升主动脉会逐渐扩张,最终面临破裂风险。
这次实验很成功,携带突变基因的小鼠果然出现了和人类相似的升主动脉扩张症状;更令人振奋的是,当团队用基因编辑技术修复突变后,小鼠的血管病变明显改善。
但新的问题又出现了:小鼠的升主动脉太细,样本量少得可怜,根本无法开展精确的定量研究,而且小鼠的血流速度、血管压力和人类相差悬殊,药物在小鼠身上的效果很难直接推广到人身上。
“必须做大动物模型!”团队一致决定。而最合适的候选者,就是家猪。猪的主动脉壁结构和人类高度相似,都以弹性纤维为主,其血流动力学机制也更接近人体。培育出携带FBN1突变的猪,成了团队的下一个目标。
跨界合作养“马方猪”,养殖场里的科研攻坚
培育模式猪,光靠医学团队远远不够。冯家烜教授找到了上海市农业科学院的“养猪专家”——涂尾龙高级畜牧师和吴潇研究员。这是一次典型的“跨界合作”:医学团队懂疾病机制,农业团队懂猪的育种和基因检测,双方的结合恰好能解决难题。
冯家烜教授团队与吴潇教授团队在上海银蛇临床中心的合影。左起:张恒、冯家烜、吴潇、何川、蒋玮
冯家烜教授(左)与涂尾龙高级畜牧师在上海市农业科学院的工作合影
实验的第一步是“建群”。团队先克隆出10头携带FBN1基因突变的F0代公猪,再让它们与10头健康的上海母白猪交配,生下F1代小猪。接下来是“筛选”:从F1代中找出携带突变基因的杂合子母猪,再让它们与F0代公猪回交,生下F2代。
这个过程远比想象中的复杂
涂尾龙团队需要在养殖场里搭建专门的“实验猪舍”,控制温度、湿度,记录每头猪的饮食和健康状况;吴潇团队则要负责“基因检测”——从每头小猪身上取一点耳组织,提取DNA后用专业仪器检测,判断是否携带突变基因,以及是杂合子还是纯合子(纯合子的病变症状会更明显,更适合做模型)。
团队一共养了135头F2代小猪,每一头都要经过严格检测。经过DNA提取,PCR扩增、酶切和测序验证,终于在135头小猪里筛选出7头符合要求的猪,他们称之为“马方猪”。
为了让这些珍贵的模型猪能长期用于研究,团队还将“马方猪”的克隆胚胎冷冻保存,纳入了上海市农业科学院的国家级地方猪遗传保种库。这意味着,未来不需要再重复漫长的育种过程,随时可以复苏胚胎,培育新的“马方猪”。
2025年2月18日首批利用基因编辑技术构建的“马方猪”模型的猪仔出生
突破效率瓶颈,让模型“标准化量产”
“7头猪太过珍贵,远远不够。”冯家烜教授很清楚,要开展高通量的药物测试或器械研发,需要大量标准化的模型猪。而传统的回交育种方法,从亲本筛选到后代表型验证,至少需要3~5年,还会因为猪的遗传背景差异,导致每头“马方猪”的病变程度不一样——有的扩张明显,有的症状轻微,根本无法满足实验的一致性要求。
这时,吴潇研究员团队提出了新方案:放弃传统回交,直接用基因编辑技术“定制”模型猪。他们针对猪的基因设计了4种不同的编辑方案,每种方案都会导致不同严重程度的突变——就像“精准调控”疾病的轻重,然后再通过影像学检查,筛选出病变程度最接近人类患者的方案。
2025年2月18日是一个值得纪念的日子:首批用基因编辑技术构建的“马方猪”在上海市农业科学院诞生了。6个月后,在上海银蛇临床中心,团队用CT、核磁和超声对这些猪进行了全面检查,结果令人振奋:基因编辑猪的升主动脉直径达到1.9厘米,而同龄健康猪只有1.2厘米,扩张了58.3%;主动脉窦直径3.24厘米,而健康猪只有1.77厘米,扩张了83.05%;另外两个关键指标——主动脉瓣环直径、主动脉窦管交界直径,也分别扩张了84.75%和63.7%。所有数据都符合升主动脉扩张症的建模要求。
“我们未来的目标是实现‘标准化量产’。”吴潇研究员说。以前需要3~5年的育种过程,现在几个月就能完成,而且通过精准的基因编辑,模型猪的病变可控、可重复,为后续研究扫清了最大障碍。
让患者受益
如今,这些“马方猪”已经成了实验室里的“特殊研究员”。科学家在它们身上测试新的药物,比如能修复弹性纤维的小分子化合物,观察药物是否能延缓甚至逆转主动脉扩张;也在测试新型微创器械,比如更贴合升主动脉形态的支架,看是否能在高压血流下稳定固定,减少并发症。更重要的是,这个模型为“基因治疗”提供了关键平台。
冯家烜团队计划接下来在“马方猪”身上测试体内基因编辑技术:通过导管将基因编辑工具输送到主动脉壁,在活体动物身上直接修复FBN1基因突变。如果成功,未来或许能通过一次微创治疗,从根本上治愈与马方综合征相关的升主动脉扩张病。
这场跨越医学实验室与农业养殖场的攻坚,还在继续。从临床手术经验的总结,到小鼠模型的探索,再到“马方猪”的培育和标准化量产,每一步都凝聚着科学家的坚持与智慧。他们的目标很简单:让那些被升主动脉扩张病威胁生命的患者,早日用上更安全、更有效的治疗方法,让“沉默的炸弹”不再可怕。
————————
本文作者张恒是瑞金医院血管外科博士;吴潇是上海市农业科学院研究员;冯家烜是上海交通大学附属瑞金医院血管外科主任、教授