C60分子极为稳定,可承受高达至少20 GPa的静压,有人认为在此高压下C60会变成比钻石还硬的固体。本文报道室温下对C60施以压强达20±5 GPa的快速非静压,可将其瞬间转化为大量的人工合成钻石结晶的实验情况。
福勒烯分子具有笼状结构,且其笼中含有12个正五边形和偶数个正六边形。直至最近,才有人制得其可供微量分析的量。福勒烯分子族中最出众的是形似足球的C60,其性质具有实用意义。在C60分子上加缀碱金属原子,生成的化合物在33 K时成为超导体,其抗压力性能也非常突出,不论是对单分子还是对具有大量SP3杂化轨道并呈准稳态因而与钻石结构相似的C60密集体施加压力,均可产生比钻石更硬的相。若施加非静压(Pc≈15 GPa),产生低对称的相;若施加准静压(Pc≈20 GPa),产生绝缘体。
我们以往的实验在室温或甚至低至约10 K进行,由于实验完后压力减小,反应小室随减压而解体,因此无法找回试样以供分析。为了尽可能找回部分样品,我们的实验没有使用压力介质,只是使用了一层内径为1 mm的叶蜡石垫片,将C60粉末包裹其中。图1中的试样A是用纯C60粉末通过常规方法制得并由P. 伯尼尔(P. Bernier)和A. 雷萨特(A. Rassat)用色谱柱分离出来。试样B和C是用市售巴基球粉末(斯特塞姆Strem化学品公司产品)制得,据产品说明书,该巴基球粉末为含2~12%的C70,实验时未经进一步处理即直接使用。我们还在装置中加了一个橡胶外圈,这样可以保留实验后减压时小室解体的碎片。试样A实验在一个钻石砧小室中进行,这些钻石彼此略微倾斜,在整个小室内形成一定的压力梯度。试样C实验中使用的是标准条件。而在试样B实验中我们引入了一片碳钢剃刀来增加试样中的非静压。在室温下我们以每分钟1 GPa的速度加压,使用一个装在施压体上的张力测量计作为粗略的压力仪。当对试样A加压至25±5 GPa(试样B和C为20±5 GPa)时,产生了爆炸,与先前所见的一样。这次,即便发生了爆炸,我们仍能找回整个试样。我们的钻石的材料是钻石小晶粒(>40 μm)与钴的烧结物,未经处理之前,它们是不规则的黑色物体,我们将其全面抛光至平滑光亮且明显与试样材料有区别。每次实验后,这些钻石砧与试样接触的一面并无可观察得到的变化,仍保持其抛光了的表面。
图1. 完成C60向钻石转化后的试样A照片
爆炸过后,样品仍包在叶蜡石中间,并具有圆盘形状,直径1 mm,高0.1 mm,有开裂纹,可以破碎,在表面上有树枝晶生成,图1是试样A的照片,爆炸后的试样变得透明,呈琥珀色亦即红褐色,在样品表面和叶蜡石垫片边上有一些黑色粉末。我们用X光和电子分光谱仪给样品定性,采用FeKα射线对试样A的Gninier粉末样品进行照射,只显示了钻石(d=2.06?)面心立方结构(f. c. c.)的反射谱线,试样C的粉末样品没有谱线,试样B的粉末样品在d=2.06?处仅显示了很弱的宽谱线,但在2.04?处有一条更宽更弱的谱线。采用此法精确测量,未发现有其他相如C60或石墨等。不过我们估计仍有大约5~10%未转化的C60残留。
我们将3种试样各取一小块样品在玛瑙研钵中碾碎,同时样品刮擦了玛瑙研钵。碾碎后的粉末送往一个覆盖有多孔碳薄膜的铜栅极,然后用电子分光谱仪分析。因为这时的粉末试样可能含有碳不同的相、叶蜡石残留物或从玛瑙研钵上刮擦下来的SiO2碎末,所以我们直接在每一小片碎片上使用电子衍射谱仪用X光进行能量色散分析。但是,用光学显微镜和电子显微镜观察,发现样品形状不是层状的,此外,所有的试样都如SP3无定形碳一样透明,在各种样品碎片中,晶粒大小为20~1000?。试样A实验采用的压力最不对称,其结晶最好,成品比例最大。相反,试样C实验用的压力较对称,用X光测量其样品,因为反射过宽且弱而测不到谱线。而条件介于两者之间的试样B产生了小粒的钻石。
虽然已经很清楚在静压条件下C60很稳定,可以承受各向均等的压力达20 GPa,但是,由我们的实验可以推断,在非均向高压下,C60不稳定,甚至在室温下即可转化为钻石相。
我们注意到,X光法探测碳化合物的灵敏度低,因此试样的主体部分(1 mm直径、100μm高的圆盘)必定是钻石,而不仅仅是一块从钻石砧中出来的无法用光学方法测定的碎片、如果产生的钻石样品来自砧的表面,我们应会发现砧的表面粗糙不平,但并无此现象发生 · 而且,试样被一层叶蜡石垫片包裹其中,如果试样中的钻石来自砧,则意味着钻石砧上的钻石穿过叶蜡石垫片进入试样,这毫无道理。我们还要指出,即使可能发生这种情况,这也只是在试样表面即与砧直接接触的部位发生。实际上,在试样表面找到的只是黑色粉末,最好的结晶是在试样的核心部位找到的。
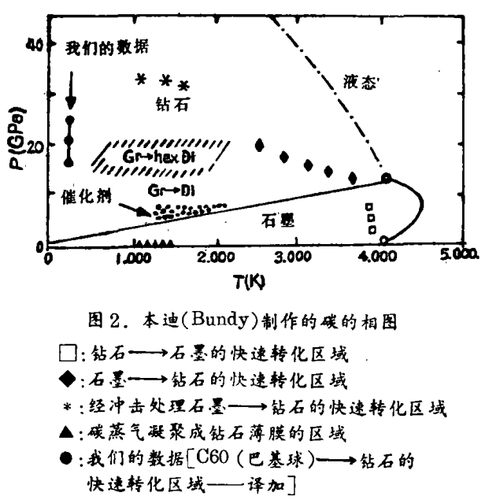
图2显示的是本迪(Bundy)制作的碳的相图。虽然,钻石在室温与2 GPa的压力下是比石墨稳定的相,但是因为转化过程的动力学速度极慢,不可能在正常条件下生成钻石。要将石墨转化为钻石,须将温度升至高于室温起码几百度,并使用冲击处理(P>30 GPa,T>1000 K)或者使用催化剂如熔融态的镍(P>6 GPa,T>1200 K)。该转化的困难在于石墨层状结构的高稳定性,石墨要加热到4000 K才熔化,而且由石墨的SP2平面结构转化为钻石的SP3网状结构很困难,因此完成该转化需要高温高压。目前人造钻石工业过程中使用催化剂,其部分作用是将碳原子从石墨中分解出来,然后这些碳原子凝聚形成在该温度及压力下稳定的同素异形体——钻石。虽然C60可被视为卷曲闭合的石墨层片,但是我们必须考虑到,C60分子中位于正五边形顶点上的碳原子主要以SP3杂化轨道成键(钻石中的碳原子全部以SP3杂化轨道成键)。该特点使C60较易转化为钻石。当大量球形的C60密集在一起,并且每60个碳原子中有48个具有准四面体的配位结构,此时碳原子的空间排列相当接近于钻石中的情况,这意味着只要略作重排即可导致整个结构的改变而转化为钻石。事实是,我们需要用非均向条件使C60在单轴即切割式的压力下出现不稳态,从而诱发反应。福勒烯在各向同性的压力下可能很稳定,只是均性地变形,但它们可能承受不了单向的挤压而转化为钻石。
[Nature,1992年1月16 日]