常用处方药氟喹诺酮类药物会导致罕见但严重的致残副作用,研究人员正在努力探索其中原因。

2014年,米瑞安·范斯塔弗伦(Miriam vanStaveren)去加那利群岛度假时不幸感染了病毒。她的耳朵和鼻窦总是跳动作痛,所以她在度假地去看了医生,医生给她开了6天疗程的抗生素左氧氟沙星。三周后,在她回到阿姆斯特丹后,她的脚跟踺开始疼痛,然后延伸到膝盖和肩膀,最后她的整个腿脚都一阵阵疼痛,还伴随有疲劳和抑郁。“我病得越来越重,整天都生活在痛苦中。”她说。以前她是一名活跃的网球运动员和徒步旅行者,如今这位61岁的内科医生几乎连路都不能走了,必须四肢并用才能上下楼梯。
从那时起,她去看了各种各样的医学专家。一些医生认为她的症状只是身心失调,另一些医生诊断她患上了纤维肌痛症或慢性疲劳综合症。然而,范斯塔弗伦确信是抗生素毒害了她。
氟喹诺酮类抗生素问题的发现和警示
她不是抗生素副作用的唯一受害者。左氧氟沙星是氟喹诺酮类药物的一种,是世界上最常用的抗生素之一。2015年在美国,医生开了3200万张含有这种药物的处方,使其成为美国第四大最常用的抗生素类药物。但对一小部分人来说,氟喹诺酮类药物声名不佳。在一些网站和Facebook群组中,成千上万服用氟喹诺酮后受其副作用影响的人在这里交流他们的经历。他们中许多人描述了一种渐进毁灭性的后果,包括从精神、感官到肌肉、肌腱和神经等方面出现的症状,而且这些症状即使在停止服用药物后仍然会继续存在。
几十年来,监管机构和医学界一直对抗生素短期疗程是否会产生如此严重的长期影响表示怀疑。但是,在病人群体的持续投诉之后,相关方的态度在2008年开始发生了变化。当时美国食品药品管理局(FDA)宣布了一系列关于氟喹诺酮类药物相关副作用的强烈警告,包括肌腱断裂和不可逆转的神经损伤。2016年,FDA认可了抗生素会产生永久性损伤的问题,即氟喹诺酮类相关性致残作用(FQAD),并建议只有在严重感染的情况下才能使用这类药物。此举引发了其他监管机构的重视并对抗生素进行重新评估:2017年,加拿大卫生部就氟喹诺酮类药物罕见的永久性致残副作用对医生们提出警告;欧洲药品管理局(EMA)预计将在2018年6月份的听证会之后,发布药品安全性评估的结果。
氟喹诺酮是很有价值的一类抗生素,对大多数人来说是安全的。然而,它们的副作用能让成千上万的人深受其害。科学家正在与病人合作一起探寻导致FQAD的原因。他们找到证实氟喹诺酮的毒性且令人信服的例子,证实抗生素不仅会杀死人体微生物,而且还会严重损害人体细胞。其实,此前对抗生素副作用的调查一直集中于药物如何破坏人体微生物群上。位于坎布里奇的麻省理工学院的医学工程师詹姆斯·柯林斯(JamesCollins)说道:“抗生素也在破坏我们的细胞,而且对细胞产生相当严重的损害。”
喹诺酮类抗生素最初是在20世纪60年代开发的,它通过阻断被称为拓扑异构酶II来杀死细菌,这种酶通常在细胞复制过程中负责解开DNA,并通常会切断DNA的双螺旋结构,通过切口穿越一段DNA链,然后修补好切口,而氟喹诺酮通过与酶结合阻止它们修补切口。20世纪80年代,研究人员在喹诺酮结构中加入了氟原子,使得这种抗生素能够渗透到全身组织中,包括中枢神经系统,并提高它们对付更广范围细菌感染的有效性。
一些FDA批准的氟喹诺酮类药物在出现严重不良反应和几例死亡后迅速从市场上撤下。例如,1999年因导致肝脏损害而撤回的曲氟沙星。但另外一些则成为了治疗严重感染和日常疾病的首选药物,尽管会导致产生一些罕见的副作用。“这些药物使用量非常大,因为它们非常有效。”田纳西州利普斯科姆大学药学院研究拓扑异构酶的生物化学家乔·德威斯(JoeDeweese)说道。20世纪90年代,环丙沙星被作为接触炭疽孢子的预防性药物而用于波斯湾服役的美国军队。2001年,在一系列炭疽恐怖袭击之后,环丙沙星销量激增,美国疾病控制和预防中心(CDC)建议为任何有可能处于炭疽暴露风险中的人提供60天的环丙沙星疗程。
但在那时,一些人已经发生了潜在的问题。1998年,现供职于纽约哥伦比亚大学新闻学院的美国记者史蒂芬·弗里德(StephenFried)出版了一本名为《苦药丸》(BitterPills)的书,讲述了他妻子因氧氟沙星而导致的严重而持久的神经反应,由此在一些网站上引发了一系列相关报道。比如到2001年,喹诺酮类抗生素不良反应论坛上已有超过5000个帖子。已故的杰伊·科恩(JayCohen)当时是加州大学圣地亚哥分校的精神病学家和医学研究员,通过这些网站接触了一些病人,并发表了45个案例研究。科恩警告说,在服用氟喹诺酮后,一些人多个器官出现严重问题。这些影响迅速并持久,有的可持续数月或数年之久。
由于他的依据来自于在线论坛,科恩的研究在当时基本被忽略了,但相关的投诉和病人的请愿仍在继续中。从20世纪80年代到2015年年底,FDA收到了超过6万名患者的报告,其中详细描述了与5种氟喹诺酮类药物相关的数十万例“严重不良事件”,最常见的是肌腱断裂,以及神经系统和精神病学症状,其中包括6575例死亡报告。FDA说,他们收到的不良事件的报告,是由药品制造商、医生甚至由消费者直接呈送上来的,不能直接得出与药品相关严重问题的结论。尽管如此,氟喹诺酮类药物引起的投诉比其他更广泛使用的抗生素要多,但据估计,只有1%~10%的不良事件呈报给了FDA,这意味着氟喹诺酮类药物可能仅在美国就对数十万人造成了伤害,哥伦比亚大学医学院的血液学家查尔斯·班尼特(CharlesBennett)如是说。
2008年,FDA发布了“黑盒”警告,提醒那些使用抗生素的人群,氟喹诺酮类药物有可能导致肌腱破裂的风险;2013年,又增加了不可逆转神经损伤风险的警告,这些提示信息被放置在药品标签的黑盒子里,呼吁人们关注或严重危及生命的风险。随着越来越多的警示,患者开始对药品制造商提起诉讼,声称他们没有充分了解风险。这些案件或胜诉,或败诉,或获得了未公开金额的赔偿,许多案件仍在进行中。制造商提出,他们已经对风险进行了适当处理,并与FDA合作更新安全标签。
2015年11月,FDA投票承认FQAD是一种综合症,其依据178个明确的例子:一些原本健康的人因治疗小病而服用氟喹诺酮,进而发展为致残和潜在的不可逆转疾病。
抗生素导致线粒体损伤的研究
加州大学圣地亚哥分校的比阿特丽斯·戈罗姆(BeatriceGolomb)在过去十年时间里一直在进行氟喹诺酮不良影响的研究。她的第一个研究对象是大卫·梅尔文(David Melvin),这名警官之前一直是骑自行车的,2007年在服用左氧氟沙星后,不得不使用轮椅。戈罗姆表示,越来越多的证据表明,氟喹诺酮类药物能破坏线粒体,而线粒体是人类细胞的能量工厂,是由数十亿年前共生的细菌进化而来。这种伤害会影响身体的每一个细胞,由此解释为什么会出现各种各样的症状,且随着时间的推移会变得越来越糟糕。
英国剑桥大学研究线粒体生物学的麦克·墨菲(Mike Murphy)表示,许多种药物都有线粒体毒性问题。由于线粒体与它们的细菌祖先有一些相似之处,抗生素可能对它们构成特定威胁。例如,研究人员已经证明,氨基甘酸类抗生素可以通过破坏耳朵里毛细胞中的线粒体而引起耳聋。
研究人员表示,从20世纪80年代开始的独立研究表明,氟喹诺酮会削弱线粒体的功能,但柯林斯和他的同事2013年的一项研究最令人信服。此次研究报告指出,几种类别的抗生素会引发氧化应激(即在线粒体作用过程中形成反应性的含氧分子),在小鼠体内表征出抑制哺乳动物细胞的功能。“我们很惊讶这种效应有多强烈,以及这种效应在不同类别的抗生素中有多普遍,但产生影响最大的是喹诺酮类药物。”柯林斯表示。
制药研究人员也发现了这个问题:2010年,美国康涅狄格州格罗顿的辉瑞公司的毒理学家伊冯·威尔(Yvonne Will)和她的同事报告称,在药物的初期研制阶段就检测到了对线粒体的损伤,不过他们发现一些抗生素对线粒体有影响,而另一些则没有。他们测试的每一种氟喹诺酮都对人体肝脏细胞中的线粒体产生破坏作用,不过威尔表示不可能通过这些研究来推断临床结果。
但柯林斯认为,在抗生素研究人员和医学界中,线粒体损伤的可能性仍然没有得到广泛重视:“人们普遍认为抗生素不会影响哺乳动物细胞。”一个问题是目前还没有可用来检测人体细胞线粒体损伤的可靠的生物标记物,以将细胞学研究与临床经验联系起来,也无法准确理解氟喹诺酮类药物破坏人体细胞的机制。例如,FDA在2013年的抗生素安全性评估中引用1996年的一项研究报告称,环丙氟沙星在哺乳动物的各种细胞系中导致线粒体DNA断裂。但是,位于田纳西州纳什维尔的范德比尔特大学研究氟喹诺酮类药物的生物化学家尼尔·奥舍夫(Neil Osheroff)对这一结果表示怀疑。他在自己的实验室测试后发现,在治疗剂量内,医生开出的氟喹诺酮对人类的DNA几乎没有影响。同时,线粒体损伤并不是唯一的影响:2015年一项关于人类肾脏细胞的研究报告称,氟喹诺酮类物质可以在几种修改DNA的酶的活性位点上与铁原子结合,从而导致不良的表观遗传变异。
在2017年9月的一次会议上,班尼特报告的一些初步数据提示为什么只有一部分人会因氟喹诺酮而产生严重的副作用。他采集了24名报告产生神经系统方面副作用的病人的唾液样本,这些副作用包括如失忆、恐慌症和抑郁等。研究人员发现其中13人(57%)都发生一种基因突变,而通常人口中只有9%的人有这种基因变异。因为申请专利的原因,班尼特并没有透露是哪种基因,但他透露说似乎是与喹诺酮类代谢不良有关的一个位点有关。这种突变可能会导致药物在细胞中积累的程度达到危险的高水平,包括大脑中的细胞。班尼特目前正在与另外100名参与者进行一项试验,以确定是否能复制这一结果。如果复制实验成功,今后有可能通过基因测试来确定那些不应使用这类药物的人群。
抗生素安全性问题研究缺乏支持
《自然》杂志在采访时,科学家在被问及氟喹诺酮问题时,大部分都认为需要更多的研究来了解这类药物的副作用。柯林斯希望通过其他动物模型来探索抗生素对线粒体的损伤。他和墨菲还发现,在实验室研究中,抗氧化剂和氟喹诺酮类药物同时使用似乎可以减轻对线粒体的影响。墨菲还感兴趣于避免药物中线粒体毒性的实验。他在一家进行几项这类实验的公司中也拥有一部分股份,但他说,这样的试验既困难又昂贵,特别是在病人垂危时使用的那些药物。
戈罗姆目前正在进行一项没有资金支持的在线调查,收集成千上万名患者的信息。几乎得不到资金支持是药物安全研究的典型特征。班尼特说,研究已在市场上销售多年的药物并不是美国国立卫生研究院等研究机构的首要任务,制造商没有动力去资助上市后药品的安全性研究,特别是对于像环丙氟沙星和左氧氟沙星这样的非专利药品,其中绝大多数的销售量都来自于仿制药公司。
另一个因素是,科学家不愿公布制药公司是担心对他们产生不利的结果。“针对那些揭露药物问题和化学药品危害的人的敌对行动由来已久。”戈罗姆说。她引用了默克制药公司的一份医生名单,这些医生披露了治疗关节炎的抗炎药罗非昔布(Vioxx)的一些问题,导致这一药物因引起心脏病发作和中风风险增加而退出市场。2009年,作为澳大利亚Vioxx集体诉讼案的一部分,法庭上宣读的默克公司的一份内部电子邮件显示,这些医生的名字被标以“中立”或“败坏名声”等标签(默克对《自然》杂志的置评请求未作出回应)。这种咄咄逼人的策略是“一个非常大的问题,”班尼特表示,“他本人过去就曾受到过制药公司的威胁。”
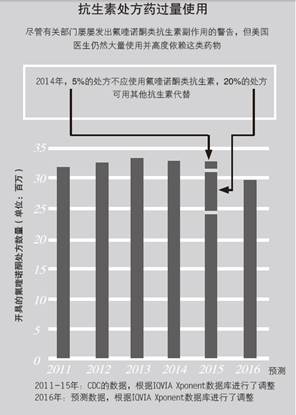
奥舍夫认为,对于氟喹诺酮类药物的担忧更为紧迫。他和其他科学家一致认为,医生在能够使用其他药物的情况下,不应该为相对较轻微的感染开出氟喹诺酮类药物。此外,FDA在药品标签上的警告效果甚至微。根据CDC的数据,2011年至2015年间这类药物的处方量并没有下降。班尼特说,这表明官方的警告还不足以让医生改变他们的习惯。他指出,在过去的4~5年时间里,单是氟喹诺酮类药物的标签就已经修改了20次。“医生几乎跟不上这种变化速度。”尽管如此,位于北卡罗来纳州达勒姆一家名为IQVIA的健康数据公司提供给《自然》杂志但未正式公布的数据显示,美国氟喹诺酮类抗生素处方量在2016年下降了约10%,而2017年上半年的统计数字表明处方量再次下降。
范斯塔弗伦表示,尽管她自己就是医生,但仍然找不到一个相信她的医生。她正在等待EMA的建议,希望EMA能像FDA一样,承认氟喹诺酮类相关致残作用(FQAD)并提出警告。目前,EMA对正在进行中的审查不予置评。范斯塔弗伦表示,“我希望医生们能了解这些风险,不管这样的风险有多罕见,我非常希望能看到这些警告的发布,并且能被认真地对待。”
资料来源 Nature
责任编辑 游溪
――――――――
本文作者乔·玛钱特(Jo Marchant)是驻伦敦的一名科学记者。