可靠的生物标志物可以帮助被诊断为非侵袭型乳腺癌的患者免除手术和放射治疗。
倘若有更好的乳腺癌标志物被发现的话,外科医生黄雪莉也许不需要动那么多的乳腺癌手术
十二年前,玛莉·简·拉平斯基(Mary Jane Lapinski)女士在马里兰州巴尔的摩市当地的医院进行了一次乳腺癌筛查。她的乳房X线照片显示左乳房区域有多个斑点。医生诊断为乳腺导管原位癌(DCIS)――这是一种早期的非侵袭性的乳腺导管肿瘤。一位外科医生告诉她采用乳房肿瘤切除术可以去除病灶,但是医生更推荐乳房切除术,也就是将整个左乳房切除。“我当时在想,这不合逻辑。”拉平斯基女士说道,那时她才48岁,“这太令人难以置信了,一个非侵袭性的肿瘤的治疗方式居然和侵袭性的肿瘤一样,甚至还要做更大的手术。”
在X线照片上,拉平斯基女士乳房内的异常细胞呈现出一种特征性的灰色区域分布。大多数乳腺导管原位癌并不会发展成侵袭性的乳腺癌,少部分则可以发生恶化导致癌细胞转移,并最终导致患者死亡。据来自北卡罗来纳州杜克大学的乳腺癌外科医生兼研究员黄雪莉(Shelley Hwang)估计,目前而言,大约20%~30%的乳腺导管原位肿瘤会在20年内发展成为具有侵袭性的乳腺癌。尽管如此,大多数肿瘤医生认为最好还是通过切除病灶和放疗来避免癌症的进一步发展。
但是,肿瘤学家们目前尚不能确定哪一类乳腺导管原位癌会往致死的方向发展。一些乳腺癌生物标志物有助于判断哪些癌前细胞会发展成为浸润癌,通过检测该种生物标志分子,便能够为治疗指出更加明确的方向。不幸的是,乳腺导管原位癌的自然发展过程很少为人所知。许多女性进行了手术,这让追踪乳腺导管原位癌的发展进程变得十分困难。就职于加拿大多伦多新宁健康科学中心的放射肿瘤学家艾琳·拉科维奇(Eileen Rakovitch)认为,“如果能够筛选并治疗那些有发展成为浸润癌风险的患者,许多女性就可以避免不必要的手术治疗。”
诊断的进展
在20世纪80年代乳房造影术广泛推广之前,乳腺导管原位癌占美国乳腺癌病例的3%。如今,这个比例已经上升到接近1/3。但是DCIS的发现并不能对女性的健康状况或者未来的发展说明太多的问题。任职于新罕布什尔州汉诺威市达特茅斯大学盖泽尔医学院的内科医生兼癌症流行病学家H·吉尔伯特·韦尔奇(H.Gilbert Welch)说,“在没有临床症状的患者身上发现肿瘤病灶是完全可能的。”韦尔奇和休斯顿得克萨斯医学中心的阿奇·布莱耶(Archie Bleyer)估计,在2008年,有70 000名没有临床症状的女性通过乳房筛查造影确诊为乳腺癌早期,这占经筛查确诊乳腺癌患者的31%。
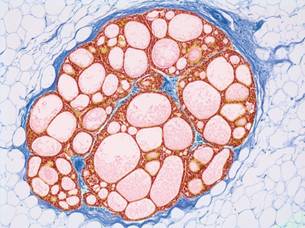
乳腺导管原位癌是一种常见的非侵袭性乳腺癌
大多数确诊为DCIS的女性会进行乳房肿瘤切除术或者乳房切除术――甚至行双侧乳房切除,并进行放疗。但是这些治疗方式带来的好处却不明显。一项基于超过10万名乳腺导管原位癌患者的观察性研究引发热议,因为这项研究表明,行乳房肿瘤切除术或者乳房切除术来治疗DCIS的患者,术后20年内死于乳腺癌的比例为3.3%,与一般人群的风险并没有太大的差别。(据美国癌症协会统计,此比例在一般人群中为2.7%。)
理想的情况下,DCIS患者应该接受评估来决定手术是否是最佳选择。尽管目前在临床上并没有配套的评估方案,内科医生们已经开始尝试使用分子标志物来预测患者的术后情况。加利福尼亚州雷德伍德基因健康中心提供一种称为基因表达谱DX DCIS评分的测试,这种测试对实施了乳房肿瘤切除的DCIS患者进行术后评分,根据评分预测肿瘤复发的风险,将风险划分为低、中、高三个级别。这种测试首先通过乳房活检采取组织样本,然后测定七种癌症相关基因的表达量。(这些基因与细胞的增殖与激素受体表达相关。)
研究员拉科维奇对实施了乳房肿瘤切除术的DCIS患者进行了回顾性研究,验证了DCIS评分的科学性。在这项由基因健康中心资助的研究项目中,拉科维奇和她的同事使用这个评分方式对718名患者的样本进行评估。“评分定性为中度风险和高风险的患者癌症复发率是低风险患者的两倍左右。”拉科维奇如是说。同时她补充道,现有的检测手段可以筛查出复发高风险的患者,但是低风险患者的评估还要综合评估病史和肿瘤的性质进行判断。
寻找分子标志物
可靠而有效的检查手段有助于预测肿瘤的转归,甚至可以达到避免不必要手术的目的,但这种手段目前还处在探索阶段。黄认为,无论是什么检查手段,都极有可能需要通过检查一系列的分子标志物并加以综合处理来实现。她补充道,“我们尝试检测了尽可能多的单个的分子标志物,但结果并不符合我们的预期。”
来自圣弗朗西斯科州加利福尼亚大学的分子病理学家西娅·提斯狄(Thea Tisty)和她的同事们已经鉴定出三种与细胞增殖相关的蛋白质COX-2,p16和ki67,这三种蛋白质与侵袭性乳腺癌的发生密切相关。提斯狄的团队发现,1 162名DCIS术后COX-2、p16和ki67表达阳性的妇女八年内浸润性癌变的比例为20%。如果这些因子表达均为阴性,则这个比例降至4%。
提斯狄说道,“这些标志物可以预测癌症前期是属于幼稚型的、基底膜无浸润型的,还是属于转移性和具有致死性的。”她的小组还有一项待发表的研究工作,这项工作鉴定了几种潜在的调控细胞死亡的蛋白质生物标记物。提斯狄补充道,澳大利亚、美国和英国还在开展四项前瞻性研究,这些研究试图说明这三种标志物的作用机理。
其他生物标志物的研究也取得进展。侵袭性乳腺癌常常会阻止抑癌基因的表达。SYK是这些基因其中的一个,SYK的表达似乎可以决定癌前细胞最终是否会发生转移。一项研究表明女性中与SYK表达相关的55种基因的异常表达会明显减少患者的存活率。
杜克大学的癌细胞生物学家杰弗里·马克斯(Jeffrey Marks)发现,循环系统的分子标志物对于早期诊断的价值不大。马克斯和他的同事选择了90种存在于血液中的分子标志物,但没有一种对提示良性肿瘤的癌变有帮助。他认为:实验的开展非常困难,很难在独立的人群样本中进行验证。
一些研究人员在寻找一些信号分子,希望通过这些分子来判断哪些DCIS损伤有较大的风险发展成为浸润型的乳腺癌。任职于马萨诸塞州波士顿哈佛医学院的计算机生物学家安迪·贝克(Andy Beck)和他的团队致力于检测基因组改变的模式。他们使用癌症基因组图谱收录的侵袭性乳腺癌的DNA图谱,寻找到在侵袭性乳腺癌相关基因中被复制和删除最为频繁的位点。“我们的做法基于最基本的设想,在乳腺浸润癌基因中出现的这些特异的位点对于浸润癌的发生发展是有帮助的。”贝克说道。
在这项研究中,这些基因标志物对癌变的影响是惊人的。对271名女性的研究表明,这三个特异基因位点发生额外复制的女性,发生浸润性乳腺癌的概率是阴性对照组的17倍左右。这个团队目前把研究对象扩大到浸润癌中常见的20个染色体突变区域。通过与斯坦福大学、华盛顿大学以及护士健康研究中心的合作,贝克的团队发起了一项包含了1 400名患者的研究,目标是预测侵袭性乳腺癌的复发和发生随时间进展的风险。
研究人员已经意识到癌症前期样本的基因多样性对于预测癌症的发生发展有帮助。随着癌症前期细胞基因和表观遗传改变的发生和积累,这种多样性变得更加复杂。一些研究已经表明多样性可以预测癌症的进展情况。马克斯现在正在研究DCIS损伤组织细胞的基因多样性。理论上讲,如果DCIS组织内的细胞具有更多的异常基因,可以预见到它们有更大的可能性发展成为适宜浸润和侵袭周围组织的癌细胞。
只有当科学家们探明能够提示浸润型癌症发展趋势的分子标志物,DCIS患者才能对自己的未来有清晰的把握。拉平斯基女士始终没有选择实施手术。她选择了黄医生的治疗方案,后者建议她加入一项为期三个月的雌激素抑制剂他莫昔芬的临床研究中。在研究即将结束之际,医生建议她进行手术,但她选择放弃手术并继续接受他莫昔芬的治疗,随后换用雷洛昔芬。每年拉平斯基女士会到黄医生那里做常规体检和乳房造影筛查。尽管其他人对拉平斯基女士的选择不太理解,她自己却不认为这是一种有风险的选择。“每一个人都有选择的权利。”她说道,“这种选择应该因人而异,只要是合适的,就是好的。”
资料来源 Nature
责任编辑 彦 隐