
大约20个月之前,我开始失眠。自从我和我的同事发表了一篇描述一种可以用来设计基因组且被称为CRISPR-Cas9的细菌系统的论文以来,已有近两年时间了。
世界各地的实验室将这一技术应用于生物学研究领域的速度令我震惊,从修改植物基因,到改变蝴蝶翅膀的图案,再到微调老鼠疾病的模式,凡此种种,不胜枚举。但同时,这一技术快速成为改变基因组的工具这一事实对于其本身的哲学和伦理上的影响,我却没有去多想。
例如,基因组编辑是否应该用于非医疗性质的基因强化,这类问题离我所熟悉的研究领域很遥远。所以我对自己说,这是生物伦理学家首先要考虑的问题。和大多数其他研究人员一样,我只想利用这项技术帮助我在我的研究领域内取得成果。
迄今,用CRISPR-Cas9操纵细胞和生物体的应用越来越广泛,然而出乎我意料的是,有人把这一技术应用于人类卵子、精子或胚胎的研究从而改变人类遗传基因的做法似乎已不可避免。2014年春的那段时间里,我经常彻夜难眠,躺在床上想是否应该远离这一场关于伦理道德的激烈争辩,虽然它是由我所参与创建的这一技术所引发的。
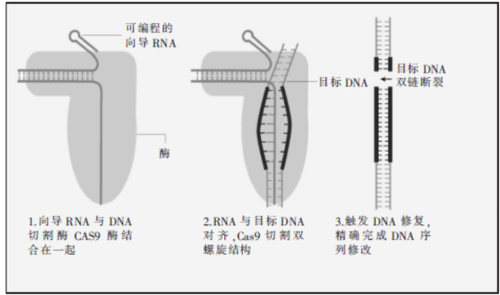
CRISPR-Cas9工作原理
规律成簇的间隔短回文重复(Clustered regularly interspaced short palindromic repeats),简称CRISPRs,是在细菌的遗传密码中发现的重复序列。它是通过将入侵噬菌体和质粒DNA的特殊片段整合到CRISPR中,从而创建入侵病毒的基因记录。
如果重复遇到某种病毒,细菌就可以产生一段与病毒序列相匹配的RNA,这种“向导RNA”与切割DNA的Cas酶结合起来,可以发现并“隔离”匹配的病毒序列,从而阻止病毒复制。
通过对“向导RNA”的设计,研究者可以对Cas酶进行编程(普遍使用的是Cas9),使其与他们想要在细胞基因组里“替换掉”的特定DNA相匹配,从而触发DNA修复过程,导致研究人员感兴趣的基因序列发生改变。
令科学家群体兴奋的CRISPR
“真令人难以相信,竟然如此成功。”这是2012年12月,我的一位一直在尝试使用CRISPR-Cas9从事研究的同事发出惊叹。这是我在实验室里感受到的令人兴奋的经历,其他一些科研合作伙伴也从这项基因编辑技术中体会和分享着CRISPR给他们带来的兴奋之情。
一种新的分子分析工具通常需要几年时间才能被普遍接受。然而,即使是在2012年后半年,在我和我的同事发表了我们最初研究的几个月时间里,至少有6篇论文描述了CRISPR-Cas9在基因组修改工程中的应用。
2013年初,包括描述编辑人类干细胞基因组以及改变整个有机体(以斑马鱼为例)的技术等在内的数篇论文的发表,使我们预感到将有一场十分激烈的争论发生。到2014年底,科学家们已利用CRISPR-Cas9技术做了许多事情,如用来提高小麦抗病虫害能力,复制小鼠肺特定染色体易位的致癌效应和修改成年老鼠的基因变异(这种基因突变会导致人类遗传性疾病酪氨酸血)等。
然而,CRISPR-Cas9的另一项潜在应用引起了更为复杂的伦理道德问题。2014年2月,研究人员描述了如何利用这一技术对猕猴胚胎基因组进行精确的修改。猕猴基因与人类基因非常接近,通常用于模拟人类遗传疾病的研究。这种修改将导致猕猴胚胎发育过程中的大部分细胞基因发生变化,包括它们的卵子或精子,这种改变还将意味着对它们的后代的链式改变。
记者们争相探寻我对这项研究的看法,这令我悚然警觉。在拜读了这些论文之后,我从办公室窗户中嘹望远处的旧金山湾,心中思考着,如果接下来记者联系到我,并想知道我对人类胚胎基因编辑工作有何看法时,我要怎么说呢?“是否要不了多久,就会有人将这一技术运用在人类身上了吗?”第二天早上在饭桌上,面对丈夫,我心中的疑问突然脱口而出。
与此同时,我收到了被潜在毁灭性遗传疾病困扰的许多人的多封电子邮件。其中一封邮件中,一位26岁的女子说发现自己携带有BRCA1突变,当她70岁时患上乳腺癌的机率约为60%,她正在考虑是否要进行乳房和卵巢切除手术,她想知道运用CRISPR-Cas9技术治疗是否意味着可以让她避免患上乳腺癌,从而避免切术手术带来的痛苦。
猕猴研究和与病人及其家属的交流让我忙得不可开交。每天都有描述CRISPR-Cas9研究的新论文出现,我的收件箱里塞满了来自各地研究人员寻求建议或请求协作的邮件。所有这些都有可能对我的生活产生直接影响,然而我认识的大多数人与我的研究工作都没有交集。包括我的邻居、我的大家庭成员、我的父母和儿子的同学等,基本上都对CRISPR-Cas9都没有什么概念。我觉得我和他们就像是生活在两个不同的世界里。
在2014年底,虽然我一直不愿参与对这个问题的公开讨论,但我的责任心改变了我想超脱事外的初衷。显然,政府、监管机构和其他人都没有关注基因编辑研究的飞速发展,除了使用这项技术的科学家,谁又会来公开讨论它所产生的影响呢?
CRISPR引发的伦理道德争论
我第一次认真介入这场伦理道德的争论是1月份在加州纳帕举行的为期一天的会议上。我也是这一由创新基因组计划主持并发起会议的组织者之一。与会的18人中包括有科学家、生物伦理学家、电影制片人以及加州大学伯克利分校的行政管理人员,我们一起讨论了基因工程可能对卫生保健、农业和环境产生的影响,并重点讨论了这项技术对人类生殖细胞系——卵子、精子和胚胎——的修改所产生的影响。
会议后不久,我们在《科学》杂志上发表了一篇阐述我们观点的文章,敦促全球科学界避免使用任何基因编辑工具修改人类胚胎并用于临床,我们还建议召开公开会议,开展对非科学家人群的科普教育,进一步探讨如何负责任地进行基因组工程的研究和应用。
纳帕会议以来,我在学校、大学和企业,以及美国、欧洲和亚洲等地,共发表了60多次关于CRISPR-Cas9的演讲,我曾在美国国会大楼前,与为美国总统提供科学建议的白宫科技政策办公室的工作人员谈过这个话题;我也曾回答过加州州长和其他人提出的一些问题,这类讨论将我从埋头科研的宁静氛围里推到了由CRISPR引发的道德困境中。
作为一名生物化学家,我从来没有用动物、人体或人体组织做过研究实验,对于其他一些研究领域中固有的伦理困境,如克隆、干细胞和体外受精等,我都不甚清楚。但通过一些同事对我的提点,让我对一些问题有了不同理解。例如,涉及人体或人体组织的实验,各个国家对其的监管都有所不同,而体外受精所带来的伦理困境在历史上也由来已久。
2015年是我最忙最紧张,也是最令我沉迷的一年。有时我真希望自己可以走下这忙碌的“旋转木马”,仅仅几分钟也好,让我有时间处理一下其他的事情。为了不影响我与实验室成员的科研进展,我与他们在一起做研究的时间大多只能放在晚上或周末,或通过电子邮件交换意见。而照料我心爱的菜园,以及与13岁儿子一起到加州田野上踏青这类事也因此全都顾不上了。
在我的一位同事就CRISPR-Cas9的辩论“浪潮”即将到来提醒我三年之后,我仍然不清楚什么时候这一“浪潮”将会达到波峰。但在2015年结束之际,有些事情我已经可以肯定。
关于CRISPR更广泛的对话
参加纳帕会议的18名与会者都是美国人,大多数都是科学家,纳帕会议只是关于CRISPR更广泛对话的一个起点,但会议决议涉及两个很重要的方面。
2014年七、八月份时,我开始产生了一些担心,在科学家向更广泛的群体普及相关知识之前,CRISPR-Cas9的使用要么本身是危险的,要么会被视为危险的。如果我的邻居或朋友说:“这一切正在发生,而你为什么并没有告诉我们?”我不会怪他们。从科学的角度来看,不久前发表在《自然》杂志上的相关评论,帮助传达了这样一个信息,即那些主导这项工作的人必须意识到,他们有责任就人们所担忧的相关问题做出解释。
4月份发表的一篇文章提出CRISPR-Cas9将被用来修改人类不能存活胚胎的基因,使得关于这些问题的讨论更为迫切,从那以后,有关这个问题的大量听证会和峰会纷纷在世界各地举行。其中最突出是中国科学院、美国国家科学院和英国皇家学会在华盛顿联合主办的一个专门讨论人类基因编辑问题的会议。
如今由于国际合作对科学发展的巨大影响,原则上科学家可以在一定程度上通过自审制度改变全球科学事业的发展方向。我认为,让公众相信科学的最好办法是鼓励人们充分了解某项技术,并积极参与其应用范围的讨论。在这个科技知识和资源全球共享,并且发布和获取数据资料也比以往任何时候都更加方便快捷的世界里,这一点尤显重要。
此刻,让我感到兴奋的是基因工程对人类生活的潜在积极影响,以及我们对生物系统的更多了解。我的同事们经常给我发电子邮件,讲述他们使用CRISPR-Cas9对各种不同生物体的研究,从培育抗虫害的生菜,到降低菌类植物菌株的致病性,再到修改人类细胞,以期有一天能够治愈困扰人类许久的诸如肌肉萎缩症、囊性纤维化和镰状细胞性贫血等的多种疾病。
我认为,鉴于他们的研究工作有可能产生的社会、伦理和生态影响,科学家可以有一些超前的考虑。例如,为生物系学生提供一些关于如何在非科学家群体中普及科普教育的培训,这也许能改变科研带来的某些伦理困境。至少可以让未来的研究人员更好地胜任他们的工作任务。例如,知道如何令人信服地描述某个研究目标,及如何判断记者的动机并确保他们在新闻报道中准确表述,这些对于每一个研究人员的科研生涯都有很重要的意义。
资料来源 Nature
责任编辑 遥 醒