“最近两年分子遗传学中发生着一次小小的演变”。Francis Crick近期刊登在美国“科学(Science)”杂志上的一篇文章就是用这些话作为开场白的,Francis Crick是这个现代的,并且因为他曾和James Watson一道发现了著名“DNA双螺旋泳”而闻名于世的学科的先驱者之一。两年以来,分子生物学实际上就已开始解析高等机体(鸟类、哺乳动物……)的基因结构。令人大吃一惊的是,这些机体的基因严格地说毫无条理性,这像分子生物学迄今所曾研究的诸如细菌及其病毒简单机体里的情况一样。相反地,近期分析的动物基因里的信息却像一段分成为一小段一段的,被一些显然毫无意义的字分开的句子,看来无意义的部分甚而往往更比有意义部分有更多的增殖。概括地说,高等机体的遗传信息似乎比细菌更加混乱。
这中间有某种颇为令人费解的事情:首先,人们更多地预期到了由数十亿个细胞组合起来的,在组织上归群为二、三百个不同的类的并以配合协调的方式从整体上起功能性作用的某些机体,它们所具有的遗传学组成远比由一个单细胞形成的某个细菌遗传学组成还要周密得多。其实情况看来是它的反面,这个预料不到的发现从一开始就在生物学家中间掀起了一股轩然大波。人们提出了许多的问题;而且已经开展了一场争论,来了解这个“新的事实”是否仅仅是把迄今有关基因结构和功能的现行理论略加修改,或是了解一下这场争论是否把它打乱。科学史中带有一定特色的就是那些因为有了发明创造而成为新一代的研究者们,就倾向于这种动乱,可是,正如Francis Crick在美国“科学(Science)”杂志上的这篇文章所指出的那样,学科的某些先驱者的态度都试图做些让步把“新的事实”纳入到老的理论中去。
嵌锒基因
作为遗传颗粒的基因是由脱氧核糖核酸或DAN形成的。自从1953年F. Crick和J. Watson发现“双螺旋体”以来,人们就知道遗传信息是以一连串要素核苷酸的形式保存在这个巨大分子里。
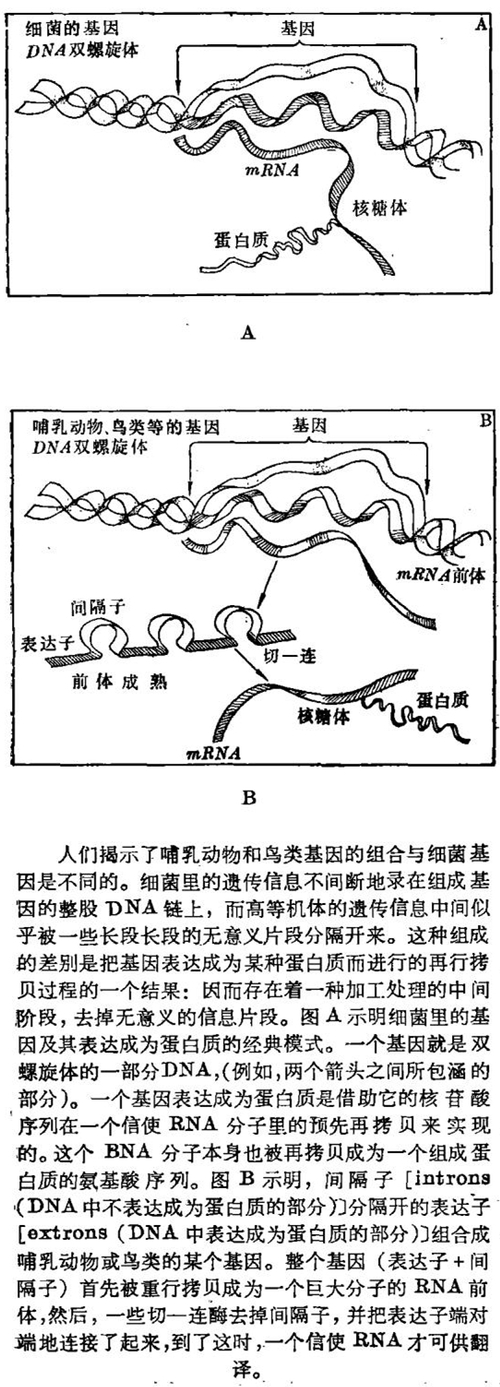
一个细胞里的遗传信息保持在染色体里并控制细胞的代谢。自60年代初F. Jacob和J. Monod的工作发表以来,人们这才正确认识基因是怎样实现这种控制的:在染色体DNA链上组成一个基因的某个核苷酸序列被重行拷贝成为一股RNA(核糖核酸)的核苷酸序列,这个序列就组成为信使RNA(图A)。遗传信息的表达阶段称为转录。信使RNA的核苷酸序列然后再拷贝成为一种氨基酸的序列形式,这个序列即组成某种蛋白质,它具备了某种酶的活性或者在细胞里起到一种既定的功能。这就是遗传信息的翻译阶段。因此,组成一个基因的某个DNA序列归根结底是以组成一种蛋白质的氨基酸序列形式表达的。简而言之,一个基因“编码”一个蛋白质。细胞里的基因的这种表达方式完全具有普遍性,从细菌细胞直至演化最高级的活体生命的细'胞一概如此。
这个“新的事实”是,在迄今所研究过的鸟类和哺乳动物的基因里,DNA的一些长核苷酸序列却进到了某个基因的组成中,它们翻译不出蛋白质来。更甚者,这些不表达的部分却插在基因的部分之间,这部分倒被转录成为信使RNA。一个新颖的术语已经流行起来了:基因的表达部分叫作表达子;不表达的以及插在表达部分之间的部分就是间隔子(图B)。例如人体珠蛋白β-链的基因就包涵3个表达子,它们被两个间隔子分隔开:小鼠免疫球蛋白重链的稳定部分有4个表达子和4个间隔子;鸡卵清蛋白不少于7个表达子和7个同隔子!那么现在来谈谈他们的嵌锒基因这个论题吧。
这时在高等机体的遗传表达中迅即出现了第二个特点:即导致从基因到蛋白质的重行拷贝过程,这在活体生命中包涵了一个补加阶段,即信使RNA的成熟(图B)。整体性基因(就是说,表达子+间隔子)实际上在转录水平上首先被重行拷贝成为一个长分子的RNA形式,它在某种程度上就是信使RNA的前体。那么为了在间隔子和表达子两者间的连接水平上切断这个长分子,就必须把间隔子切割下来,再把表达子端对端地连接上去(捻接),这就涉及到—些酶:这个过程产生了一个信使RNA,在这个信使RNA中,遗传信息终于具备了一种线性规则,并且为翻译做好了准备,就像细菌中出现的情况一样。已在进行的许多研究,旨在分离切一连酶以及了解这些酶是怎样“辨认”它们应该施行切割的,RNA前体所在的地方。
可是争论是针对间隔子的意义。这些未表达的DNA序列为什么存在于高等机体内,而不存在于细菌内呢?这些序列真的一点用途都没有,它们在那里就只待人们来把它们去掉,或者不直接地抑或非不直接地参与遗传信息表达的控制么?
间隔子:有害还是有益?
Francis Crick以前曾抛出一个假设,认为高等机体的基因原先是由连续的DNA链组成的(就像细菌中的情况一样),不过他又认为,这些基因在这些机体演化的某个既定发展阶段上可能遭受到一类来自外界的,无遗传学意义的DNA序列的“污染”,它们“非法地”潜入到原先那个基因内部。间隔子就是通过这一方法应运而生,它们分隔嵌锒基因里的表达子。此外,F. Crick还曾指出,切一连机理这时就应成为出现于高等机体里的一种保护方法,以便在信使RNA水平上重新建立起遗传信息的条理性,从而达到一目了然的目的,因为这一机理在DNA水平上被间隔子搞乱了。这一理论是根据下列事实建立起来的,多年来人们就已认识到细菌内存在着一些DNA部分(人们给它们起了一个绰号,叫做IS因子或“跳跃”基因),它们能侥幸地和非法地潜入到细菌染色体里面去。但细菌恰恰不具备任何的切一连机理,而且即便某个基因被这样一种“跳跃”基因潜入进去了,它也常常不能起功能性作用。
这一学说归根结底是以下列事实为前提的,间隔子在基因里的分布或少或多是任意性的。S. Tonegawa(Bale免疫学研究所)的结果指出,在免疫球蛋白实例中,间隔子的分布不是任意性的。恰恰相反,它们严格地被分隔在表达子中间,这些表达子“编码”各类蛋白质,每一种蛋白质均在免疫球蛋白抗体功能里面起到它们的作用。因此,S. Tonegawa就曾利用这一观察在英国“自然(Nature)”杂志上重新肯定了它的关于间隔子的意义和起源的见解。
根据他的看法,免疫球蛋白重链的不同表达子来自某个原始基因的一系列重复(也就是说,在染色体内部制造出了起始基因的互补性样板)。重复达到新型拷贝串列衔接的地步,间隔子则对应于衔接区。
S. Tonegawa和W. Gilbert(哈佛大学)甚至支持有关间隔子起源的还要更为普遍的一种解释:根据他们两人的看法,一种嵌锒基因的表达子首先不取决于任何重复而能存在,它们分散于染色体的基因库中,每个表达子各各控制不同的功能性蛋白质合成。尔后,一种移位机理将使两侧有间隔子的表达子自我插入到位于其它表达子两侧的间隔子中:就这样,两个表达子从此就被引到附近的位置,中间总保持有一个间隔子。可是,新的转录单位这时就可以产生出一种具有新的功能,跟从前受表达子位于远处时的控制的功能不同的蛋白质。因此,间隔子的意义就在于它在物种演化期间容许两个DNA序列顺利地发生融合,而又不打乱表达子的遗传信息。这样,它们就实际允许表达子的某种混合,从而便利于作为能编码新型蛋白质的遗传单位的遗传物质的富集,它们远不是多余的分子,它们一度曾加速高等机体的演化。
说真的,两种理论现在似乎已实现和解了。就像间隔子在它能允许表达子混合之前就必须先行问世的一样,F. Crick猜测,最初的间隔子诸如细菌里的插入因子,可能是出现于高等机体的祖先里。
F. Crick报道说,S. Tonegawa在一篇个人通讯里就这一点是跟他一致的。另一方面,他在美国“科学(Science)”杂志的文章中,发现S. Tonegawa的有关表达子混合在新的间隔子世代的作用的概念本身是合理的。
围绕一个法则的论战
可是,有关间隔子的目前功能还存在着另一个争论点,在这中间以F. Crick为一方,以W. Gilbert和S. Tonegawa为另一方,他们处于针锋相对的状态。后者曾经承认,“一基因——一蛋白质”的法则会由于嵌锒基因的出现而被打乱,并且被“一基因——多蛋白质”的一种新原理所代替。实际有可能从理论上考虑,在信使RNA形成之际的某个嵌锒基因的表达子仅仅是其中某一些才连接在一起,形成一个既定类型的蛋白质;而在其它情况下,捻接涉及同一个嵌锒基因的表达子的另一种选择,这会导致形成另一类型的蛋白质。换句话说,嵌锒基因可能就是经过多次选择而表达成为蛋白质的那些基因。这可能就是胚胎发育期间应用到细胞分化中的一种机理。看来在免疫球蛋白实例中存在的实际就是这一种,这就部分说明了脊椎动物里的抗体巨大多样性。看来这也存在于某个致癌病毒猿猴空泡病事(SV40)(寄生于高等机体的病毒,由于其遗传组合,常被看作是寄生性病毒的模式)。但F. Crick考虑,免疫球蛋白的实例将是个别的,而且猿猴空泡病毒的实例具体说明常在病毒里遇到的过程:用最小的方法做出最多的成绩的过程;他认为,多次选择的基因在高等机体里只会是例外。这就更加离奇了:假定这样一个基因是在物种演化过程中孕育起来的,他认为这个基因一定被分成为两个,每一个拷贝在编码某个蛋白质时都各有其特异性。
显然,目前还难于说明白谁是对的,各方面提出来的概念都是更广泛意义上的推测。但是人们的确看到了高等机体的嵌锒基因正在哺育某些新的概念,后者必然要遇到一些反抗。可是,Francis Cri-ok承认这些推测的促进作用,并且“公正地”承认嵌锒基因不是别的,只不过是前人见解的某种庸俗的引申。这可能就是他为什么没完没了地粉饰这场革命的发现,不惜用“小小的(mini-)”这个字头来衬托它。
〔La Becherche n°.103,896 ~ 898页,1979〕