酸雨正在四处蔓延
首先是在工业发达国家出现的酸雨,已经蔓延到发展中国家,逐渐演变为一个世界性问题。我们知道,水的酸度一般是用pH值来表示的,纯粹的水为pH7,天然的雨水因含有碳酸气(二氧化碳),所以呈微弱酸性,pH值在5.5 ~ 6之间。但是,现在在世界各地下的雨大量的却是pH3 ~ 5,这就是所谓的酸雨。
尤为严重的是在美国的东北部、加拿大以及斯堪的纳维亚等地。在那里,大片林木开始枯死,众多湖泊因pH值降至5以下而导致鱼群大批死亡。对此,加拿大归罪于在美国生成的氧化硫和氧化氮,斯堪的纳维亚则指责德、英、荷等国放出的氧化硫。
1981年年底,美国参议院有人作证说,迄今酸雨使美国经济遭受到很大的损害。其中农作物损失了10亿美元、林业17.5亿美元,建筑业20亿美元,渔业2.5亿美元。如果不及时采取措施,损失还将迅速加剧。
坐落在印度亚格拉的世界著名的泰吉马哈尔陵,是用光可鉴人的大理石建造的十七世纪古建筑,她那宏大雄壮的气势,使得世界各地的游客为之倾倒。可惜,这些大理石的光泽最近开始急速消失,印度政府为此伤透脑筋。同样,罗马的大理石古迹,大多亦已危如累卵,崩坍在即。
在日本,四日市大气污染最严重的时候,也曾下过pH2的酸雨。1974年和1975年的梅雨季节,关东一带下的雨是pH3 ~ 4。每场雨开始的蒙蒙细雨,使得数万人眼疼难忍,叫苦不迭。
氧化氮才是罪魁祸首
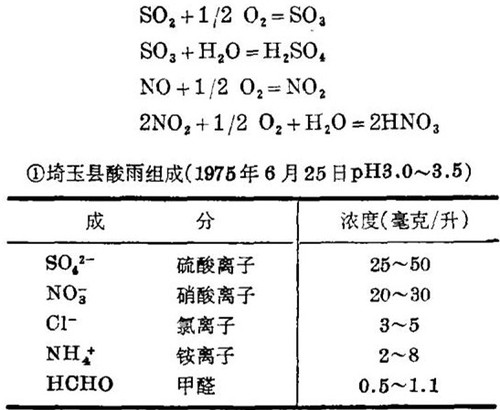
酸雨的主要酸性物质是硫酸和硝酸①。这些酸性物质大部分来自火力发电厂、工厂、汽车等排出的氧化硫SOx(SO2为主,少量的是SO3)和氧化氮NOx(主要是NO,NO2其次)。NOx即使在天然的情况下也能大量生成,但SOx则大部分是由于石油及煤的燃烧,自然生成的比较少。在潮湿的大气中,SO2和NO会逐渐氧化变成硫酸和硝酸。其化学反应式如下:
湿度和温度越高、这类反应就进行得越快。SO2和NO中的10 ~ 20%左右变成硫酸和硝酸所需时间少则几小时,多则几天。再加上烟囱高度和风速大小的因素,下酸雨的地方往往离开发生源50 ~ 2000公里。
—般认为,① 的雨中含有的硫酸和硝酸是由京滨、京叶工业地带的工厂及汽车等排出的气体,乘着和缓的南风飘然而至,并在高温高湿中生成的;雨中的盐酸主要是从垃圾焚烧炉、甲醛是从汽车废气中产生的;大量的氨则是自然界的产物。
为了弄清埼玉县熊谷地区的酸雨为什么会刺痛眼睛这一问题,我特地把各种各样的酸放入自己的眼睛,进行实验。在pH3的情况下,硫酸也好,硝酸也好,盐酸也好,放进去全没有刺激。把这些酸混合起来,或者每升加入10毫克左右的甲醛和氨等溶液,亦无异常感觉。可是在pH2.5时,不论哪一种酸对眼睛都有强烈刺激。我还对梅雨季节头里的蒙蒙细雨中的一个个颗粒进行了pH测定,发现有些颗粒的pH值是2 ~ 2.5。可能就是这些颗粒,在刺激着人的眼睛。可是,人们在进行pH值测定时,总是先把雨水集中在一个容器里,这样,酸度被大大稀释,pH值自然就大于3了。
从1950 ~ 1976年间,美国的SOx生成量从2200万吨上升到2700万吨,NOx 从800万吨猛增到2200万吨。其中约一半的NOx是从汽车里排出来的。鉴于目前世界上汽车与日俱增,产生酸雨的原因也开始由SOX逐渐转移到NOx上来。日本现行的措施是世界上最先进的,硬是把SOx和NOx限制在一年200万吨以下。
放宽限制的里根当局
只要减少SOx及NOx的排出量,就可以防止酸雨的生成。日本施行的减少SOx措施不仅体现在推广使用含硫少的燃料上,而且还建立了1200座排烟脱硫装置。这种装置能够净化废气,去除SOx①。在处理火力发电厂等排出的大量废气时,我们采取在吸收塔内喷降内含石灰石粉末水雾的方法吸收SO2。石灰石的主要成分是碳酸钙,它与SO2反应生成亚硫酸钙,然后把它用空气氧化而成硫酸钙,即石膏。这种石膏一年生产200万吨以上,可用于生产水泥和板状建筑材料。
然而,排烟脱硫装置耗资大,大型的一座就得投资50 ~ 100亿日元。为此,日本已经用掉数兆日元,从而使火力发电成本跃居世界第一。美国在卡特当政时期,曾决定向日本学习、全面实行排烟脱硫计划。但到了里根时期,却以脱硫费用过大,将削弱产业为理由,正一步步地放宽限制。
以汽车为例,日本通过改良柴油发动机,使用催化剂等手段,使NOx的排出量控制在1公里0.25克内。但里根当局即使是0.6克也嫌破费太大,考虑把限制放宽到1.2克,因遭到舆论界的反对,议会正在审议妥协方案。
日本眼下又建造了140座脱硝装置,这种装置能够从发电厂及工厂排出的废气中去除NOx。美国像这样的脱硝装置只在洛杉矶才有一座,而该地区NOx浓度却在东京和大阪的一倍以上。在欧洲,排烟脱硫装置仅西德有几座,荷兰有一座,而脱硝装置则一座也没有。实际上,只要各国都像日本那样采取得力措施,那么酸雨问题必将得到大大改善。
世界主要燃料正从石油转向煤。从SOx及NOx的排出量来看,煤要比石油多,所以重要的是加强措施。世界可开采的煤的储藏量为7000亿吨,若把它们全部烧完,将产生200亿吨的SOx和50亿吨的NOx。用于吸收这些SOx的石灰石全世界有的是。也正是由于泰吉马哈尔陵使用的大理石和石灰石同类,所以才与SOx发生着化学反应。
至于NOx,我们正在用氨来进行脱硝,使它变为氮(N2)。要去除50亿吨这么多的NOx,将在全世界用掉大量的氨,这将迅即造成世界性的氮肥不足、粮食减产的恶果。由此看来,我们在考虑NOx对策时,应该把中心放在用改善燃烧方法来减少NOx生成量上。让微量的SOx和NOx存在于大气中非但无害,反而对植物的生长有益,因此我们只要设法把它减少到无害程度就可以了。
关键在于柴油车的排气
日本采取的世界上最严格的防污染措施,起源于六十年代初期发生在四日市的哮喘症。人们普遍以为病因在于当时四日市建成的联合企业因采用含硫量高的重油而生成的SO2(亚硫酸气)。其实,虽然四日市下过pH2的严重酸雨,但相隔50 ~ 60公里以上地区的雨水酸度则是正常的pH5 ~ 6。从这些迹象分析,这不同于由SO2引起的酸雨。
只要查阅一下四日市的大气测定数据,就可知道当时市内各区SO2的平均浓度为0.02 ~ 0.1 ppm,并不算高。但S03(硫酸酐)却异乎寻常地高,有的地方甚至超过SO2。一般来说,如果仅仅是由燃烧重油排出的废气所生成的SO3,充其量才不过是SO2的3%左右。显然,这么多的SO3是从化工厂里跑出来的。
SO3一旦排出,立即与水蒸气结合,成为浓硫酸(70 ~ 100%)的微粒,即浓硫酸雾,其害处远远超过SO2。正是这种浓硫酸在市内到处游荡,才引起了哮喘,并溶于雨水生成酸雨。当时因为人们还不甚了解SO2及SO3的性质和作用,以至于把祸因错怪为SO2了。
四日市对SO2和SO3都实行了严格的管制,才算降服了污染。之后,虽然在全国加强了对SO2及NOx的限制,但把SO3给忽略了。日本大城市及工业地带的SO2和NOx浓度一般要低于欧美,但是,因大气污染而引起的公害病患者却比欧美多。不难看出,这是SO3在兴妖作怪。
目前特别成问题的是从汽车、卡车等柴油发动机中排出的有害气体。用于发动机的轻油一般含硫0.4%,是工厂、发电厂所用燃料含硫量(城市边缘平均为0.12%)的二倍以上,加上马路上放出的浓硫酸雾和烟尘,有害程度特别厉害。美国用于发动机的轻油含硫量是0.2%。加利福尼亚州决心把它减少到0.05%。在我国城市里跑的用柴油发动机的车辆,比美国多得多。降低轻油的含硫量,越显重要。
去除SO2和NOx对于防止欧美那样大面积酸雨固然重要,但因为日本3000米以上高空盛行西风,SO2和NOx被吹到了太平洋,所以除了梅雨季节,酸雨问题并不突出。现在麻烦的是从南朝鲜和中国吹来的SOx和NOx。最近,环境厅设立了“酸雨对策研究会”,以期进一步弄清事态。
[《科学朝日》,1982年12月号]