利用DNA微量注射法而获得的转基因动物是日趋发展的高科技。应用该技术繁殖鱼类已取得不同程度的成功。应用优化微量注射特别技术于鱼类并研究选择大量培养方法可生产出表达了最佳特性的基因转移鱼产品,进而促进鱼及后代的生长和抗病能力。
人工注入基因到动物体内是有效的转基因方法。自80年代初微量注射异种DNA来已产生了转基因的果蝇、海胆、蛙、鼠和农场哺乳动物猪、绵羊、牛。所举例子,DNA均注入了受精卵的原核内和胚胎中然后在玻璃缸或假孕子宫内继续发育。这些研究展示异基因增殖复制在随机点位结合并进入从头到尾呈串联排列的转基因动物染色体组内。如一种助长功能的异基因注入发育的胚胎,表达这种基因可望促成一些基因转移个体。在许多场合,异基因能通过生殖种系遗传到繁殖的下一代。这种繁殖和转基因动物的研究所获知识正引入发育机制和致癌基因基因调控机制及免疫系统内复杂的互相作用机制。利用这项技术可能治疗特殊的人类遗传疾病及生产重要的经济蛋白质而成的动物工程模型。
转基因动物也显示表现型变化。如转基因鼠表达人类和鼠类生长激素基因可以控制提高激素的生长水平,结果比控制的同科动物生长快。研究证明注入合意基因特性从而加快了鼠的生长,增强了抗病和耐寒能力,并稳定重要的饲养动物,代替和补充常规类似的遗传饲养。
鱼类的基因转移研究仅开展几年,然而研究进展是极鼓舞人心的,回顾旨在应用该技术解决水产科学和基础生物学中的问题。
基因转移的方法
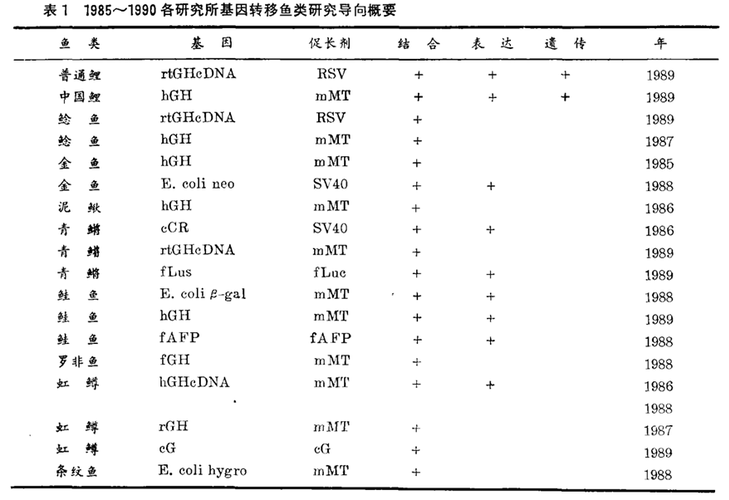
微量注射 1985年《科学》杂志介绍了微量注射进入鱼体的异基因包括人、鼠生长激素,鸡d-结晶蛋白、大肠杆菌b-半乳糖苷、大肠杆菌新霉素抗基因、大肠杆菌潮霉素、冬季比目鱼防冻蛋白和虹鳟cDNA生长激素(表1)。DNA克隆微量剂直接注入受精卵原核中。实验证明异基因注入基因转移的鼠、牛、猪、羊和兔的生殖种系内为最成功和有效的方法。虽然该方法需特殊的设备和熟练技术,但结果是极明确的且任何DNA克隆能被利用。原核微量注射包括以下基本步骤:_
· 几百复制的线性化克隆基因溶解于小容积内(<2 nl)并用玻璃超微吸管注入1细胞期的胚胎核中;
· 将胚胎重新移入假孕子宫内进一步发育;
· DNA从假定基因转移动物的活检组织中提取并适合对南方杂种弱点的分析,利用放射性同位素标记异基因作为探子;
· 进一步研究亲本一代(P1)基因转移个体。
相同的微量注射技术繁殖的许多基因转移鱼类已获成功。如,鲤、鲶鱼、金鱼、泥鳅、青鳉、罗非鱼、虹鳟、鲑鱼和条纹鱼。因大多数鱼种类原核型数据研究不容易具体化,DNA常注入细胞质代替。精、卵采自成熟的个体并放入干的容器中分离。精卵加水受精并缓慢搅拌门促?受精。卵膜在水中各时期的变化视不同鱼种而定。约106~109 DNA分子线性化,有20 nl或更少(表2)的剂量微量注射到受精几小时的卵中。微量注射后的卵在适当的孵化箱中孵化并每日清除死胚。
鱼类的体外受精发育,胚胎注射不要求复杂的特殊操作而哺乳动物类如玻璃状的胚胎培养和转移胚胎要进入母体内。
与微量注射DNA不同,逆转录病毒遗传物质是融入了感染率极高的细胞染色体组内。只有单个复制的前病毒DNA是插入在所给染色体点并重组原染色体组而不减少。通过病毒的功能异基因插入病毒基因组因而能转移到原染色体组中。总之,具特殊种类特性的逆转录病毒推动和发展了培育转基因鱼类的方法。
电激法 利用的是短暂电脉冲渗过细胞膜,因此允许完整的大分子包括DNA渗过。采用该方法对细菌、培养的哺乳动物细胞和植物胞质进行的基因转移已获成功。几个研究所试图利用这一方法将外源基因移入鱼胚没成功。
Liposomes采用反转脱水法精制磷脂成功地把它作为药物和蛋白质的传达媒介进入培养的哺乳动物细胞使包裹的异源DNA转移到哺乳动物细胞或植物胞质内。几个研究组试图用该方法将异种DNA转移进鱼胚却毫无结果。
利用高速微粒子弹轰击的方法可使异DNA射比胚胎核内注射伤害少(因为鱼类核型很难固定),这样注射的鱼胚胎成活率比哺乳动物胚胎高得多。依种类不同,鱼胚的成活率范围是35%~80%(表2)。虽然DNA注入细胞质,但DNA融合率相当高(10%~70%)。青鳉不采用细胞质注射,它适合异种DNA注入原核内。棘手的是许多鱼受精卵可能附粘在超微玻璃针上,解决这一难题有几种方法。
虹鳟和鲑鱼卵先进行超微手术,打开后插入微针。大西洋鲑、罗非鱼的界种DNA可通过微孔注入因为在受精间精子渗透的孔打开。粘性条纹鱼卵可用镊子操作除去,金鱼和青鳉粘卵膜用胰朊酶浸提。
基因转移的其它方法 虽然细胞质微量注射是一成功技术却是单调和耗时的繁殖而不适合大量基因的转移。因此进一步研制新方法迫在导入水稻或谷类嫁接胚胎细胞内。这种方法异DNA吸收了4 um球形钨粒子,外源DNA被粒子枪注入了植物细胞内,因为粒子能助长植物细胞壁,该技术可转移外源DNA穿过未动的粘卵。
转移生长激素基因促进生长
虹鳟生长激素(GH1)cDNA在大肠杆菌中表达出高水平。适用的蛋白腹腔注入1龄虹鳟为结果明显促进了生长——用重组GH注射四周后重量双倍增加(1 ug/g体重/周)。相同促进生长效果在接受了重组生长激素注射人的渗透冲击的2周龄虹鳟苗中也观察到。应用体外GH重组可促进培养的鱼体生长,利用这种基因转移技术产生的基因转移鱼类表明了高水平的GH是更有价值和效力的补充方法。这些鱼不只产生内生长激素通过这些产物和助长方法也将提高生长的特性传给了后代。
1985年朱(Zhu)等报道成功地将人类GH基因与老鼠金属硫堇助长基因融合并注入金鱼体内。金鱼F1(子一代)后代基因转移鱼类的生长为非转移种类的两倍而GH注射入虹鳟和蛙鱼也产生了一致的促进生长的生物综合效果。虽然Zhu等没提出强硬的证无目标融入鱼染色体组;(C)逐渐遗传到繁殖的下代(F1):(d)异基因已在繁殖的P1和F1中表达;(e)表达了异GH基因的增加且促使P1和F1基因转移鱼类生长率的提高。
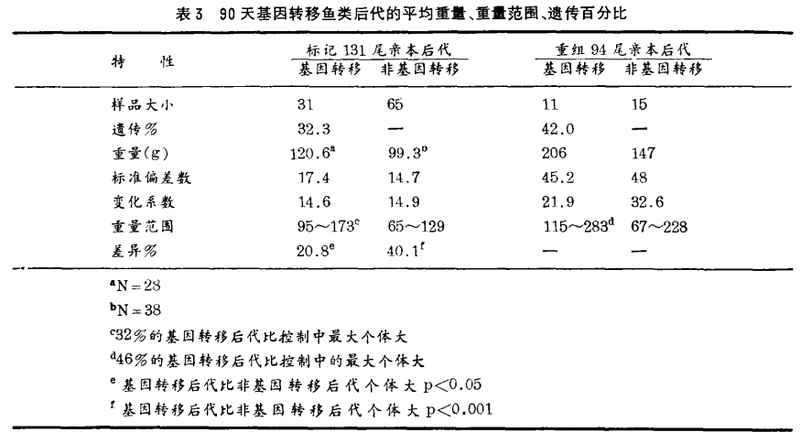
张(Zhang)等研究106分子线性重组质粒包含长期终止重复(LTR)鸟类劳斯肉瘤病毒(RSV)序列和将虹鳟的GH1cDNA微量注入普通鲤1—4期胚胎细胞中。DNA染色体组样品从胚胎发育来的个体胸鳍提取并用嫁接点和南方异种突点分析,利用RSVLTR和虹鳟GH1cDNA作为探子。注入微量剂的胚胎其存活、孵化率为35%,约10%的存活个体中发现已稳定与pRSVLTR-rtGH1cDNA序列融合。而虹鳟GH多肽表达也在许多遗传转移个体中检验到。虽然不少P1基因转移鱼大小有变异,平均比同科控制的鱼大20%。更进一步随机选择F1的后代(由P1基因转移雌鱼和非基因转移雄鱼杂交的)遗传和异基因片断。这些基因转移后代不仅比非基因转移的同类鱼生长快而且也比其父母生长快(表3)。基因转移实验包括人的GH基因结构成分得出的相似结果。中国鲫、鲤F1后代实质上比P1母父杂交的后代大,与利用的镜鲤相差无已。虽然转移、表达和异种GH基因遗传研究大有进展,一些基因转移鱼的生长结果明显快于同科非遗传鱼类,快速生长的基因转移鱼类的后代商品鱼仍处于发展阶段。今后研究发展的总目标是:(1)改进基因转移效果;(2)鉴定适合的助长剂以推动GH异源基因表达型:(3)确立生理学、营养学和环境遗传因素而充分显示转移个体的特性;(4)评估安全和环境效果。
转移抗凝蛋白基因增强鱼的耐寒力
人们发现鱼能在极地、温带和热带水域生活,这些地方的条件每天或季节有变化。为适应温热条件鱼类发展,产生了复杂的长期有效的生活习性、繁殖方式及生理机制。一些耐寒鱼有一系列特异的蛋白、抗凝蛋白(AFP)使血液免遭冻结。De Vries发现AFP基因在极地鱼类里周年表现,温带种类,像冬天的比目鱼才发现具AFPs。有这种蛋白的鱼就可在-2°C的水中生活。鲑鱼和其它鲑科鱼类没有相同或类似的适应战略故在这样低温水域不能存活。
南极鱼的AFPs由重复的丙氨酸-丙氨酸-苏氨酸组成含二糖类、半乳糖-n-乙酰半乳糖胺,糖苷通过葡糖苷键与苏氨酸联结。另一方面,冬季比目鱼AFPs是具丙氨酸-富含螺旋状蛋白而缺二糖类,这些机制通过AFPs键的超微-冰晶粒实现因而决定了血液较低的冰点,有几种鱼类的DNA序列译成了这类蛋白。最近Huang等介绍冬季比目鱼克隆AFP基因注入了虹鳟、翻车鱼和鲑的细胞系并通过检测AFPmRNA综合性观察到基因的表达型,表明AFP基因用来生产耐寒能力的鱼类将成为现实。
转移反义DNA序列防止疾病
在任何养殖业中,动物疾病证明是减少收入的主要原因并左右成功与失败,尤其在商业性养殖中。诊断和控制由细菌、真菌、病毒所导致的鱼病仍为目前主要的技术和经济难题。虽然抗菌素和化学药疗能有效用来控制分离的一些鱼病原体,但无普通实用的抗病毒药物或疫苗预防治疗鱼的病毒性疾病。因此,唯一有效的办法是总体上消灭产业中病毒对鱼的感染。功能性造血坏死病毒(IHNV)被鉴定是一病原体曾导致大批华盛顿州红大麻哈鱼死亡(1953年)。自那以后,这种疾病从阿拉斯加蔓延到加利福尼亚而最远扩散到了日本西部,近年已威胁到天然和人工培育的鲑和虹鳟类。IHN和其它病毒冲击了经济,近年来科学家正竭尽全力研制抗IHNV等疫苗。最近,LEong等研究了IHNV病毒粒子基因克隆和序列及一种INHV表面糖蛋白的eDNA,采用在带菌的杆状病毒中表达cDNA糖蛋白基因序列的方法,成功地生产出大量综合性生物疫苗,证明治疗感染了IHNV的虹鳟有效。另外,可预防IHNV和相关的病毒病。一种重组疫苗也研制成功可治疗狐菌类细菌性病原体病。
抗病毒疫苗应用有两种选择阶段其中包括发展免疫性鱼类。一种注入结合的DNA充当促进剂以保证抗病毒RNA序列表达,通过抑制病毒的复制而阻止病毒的感染。这一策略证明在鸟类逆转录病毒系统有效。另一种转移病毒膜蛋白基因进入有机体证明可防止病毒。足够的浓缩病毒膜蛋白必须通过寄主竞争到细胞表面病毒受体连接点而产生。
未来工程
自1985年来,基因转移鱼类研究生产取得了重要进展,进一步研究要求获得实验系统鱼类最佳优点并发展以商业养殖为目标的基因转移鱼类。
研制有效方法使转移基因进入大批的生产卵中而使鱼成为特别的标准实验模型。研制群体基因转移技术如利用抗病毒携带者,具DNA精子膜,电激法和高速粒子枪是未来主攻方向。研究快速生产为鉴定预测基因转移个体的早期生活是必要的。我所未来主要研究形态学和生物化学市场(如,体色)这将可能快速鉴定处于卵或幼苗段的基因转移个体,这样可排除非转移个体。在较短时间内,发展有效群体基因转移方法将同快速群体筛选匹配从而促进鉴别基因转移个体的病毒,胚胎阶段效果更佳。
采用微量注射转移异源基因序列进入胚胎结果常是随机融合基因序列进入原染色体组。结果,融合的异源基因打断了原基因基本的转录而导致畸胚或死亡。因此研制标准的异基因到达染色体组特殊面是重要的。也必须研究正常特殊组织和发育阶段异基因(在)适合水平的特殊表达技术。这方面,起源于胚胎学的细胞技术可能具很大的潜力。
为最大限度发展异源基因在基因转移动物中的潜力,研究基因转移鱼类的生理学、营养学、发育学、免疫学和繁殖在典型野外环境下的刺激反应是必要的。例如,重要的是研究基因转移鱼类的生长特性和鱼在典型充足饵料养殖下产生的GH升高水平及各种饲料条件变化下对自然环境中的季节变化的适应。当饲料被限制这些基因转移鱼类将饿死,或将它们放到野生群体中竞争?另一重要研究是池塘实验,必须走这一步以确定环境可能对转基因鱼类产生的制约因素。
[Trends in Biotechnology,1990年第8期]