研究表明,产能细胞器线粒体或在焦虑和抑郁的产生机制中至关重要。

压力和焦虑或许不仅取决于脑内的神经元,细胞内的线粒体也举足轻重
卡门 · 桑迪(Carmen Sandi)回忆起她最初受到的质疑。作为瑞士洛桑联邦理工学院的行为神经科学家,她有一种预感:在关键神经元环路的内部,一种超越脑细胞和突触连接的结构能够解释焦虑行为。她始于2013年的实验表明,与焦虑行为有关的神经元会发生一种现象:细胞的线粒体——被比作细胞发电站的细胞器——功能异常,它们产生的能量水平低得令人惊讶。
这一结果提示线粒体可能与生物面对压力时的一些症状有关。但这与学界持有的大脑以“突触为中心”的看法背道而驰。同事们难以相信桑迪在焦虑个体(至少是大鼠)上的结论——关键神经元内的线粒体有重要作用。
“每次我展示实验数据,他们都会说,‘这很有趣,但你弄错了’。”桑迪回忆道。
但在过去十几年中,还是不断有科学家加入她的研究,也有很多人开始思考线粒体可能不仅仅是生理健康的基础,也对心理健康至关重要。科学家开始关注线粒体是否会影响我们面对压力以及焦虑和抑郁等状态时的反应。
现如今许多证据还处在初级阶段,但已经指出了一个潜在的关联性。线粒体在应对压力时有重要作用,它不仅仅作为中介参与其中,也会在过程中受损。一些研究者认为压力反应甚至可以看作是一种全身线粒体的协同行为,与神经学过程相交互。
“我认为线粒体的作用被低估了,”纽约哥伦比亚大学欧文医疗中心的马丁 · 皮卡德(Martin Picard)说,他的实验室在该领域处于研究前沿,“它们是细胞中主要的执行细胞器。”如今科学家在探索这一细胞器的重要作用,以及在未来可能用于治疗的方法。
线粒体与心理健康

卡门 · 桑迪,瑞士洛桑联邦理工学院的行为神经科学家,她认为细胞产生能量的不足能够解释人类缺乏动机和有焦虑倾向的内心体验
线粒体是复杂(真核)细胞中的微小结构,能够产生大多数代谢过程中的化学燃料——三磷酸腺苷,即ATP。加拿大维多利亚大学负责研究的副校长丽萨 · 卡林丘克(Lisa Kalynchuk)说:“ATP就是能量,让生物的活细胞能够完成它们的功能。”这一细胞器是远古时代的入侵者,共生细菌的残留物,它们大约在20亿年前将自己整合入宿主细胞并专注于产能。线粒体仍然保留了一小部分自身的DNA——大约37个基因——比任何活细菌的遗传物质都要少。
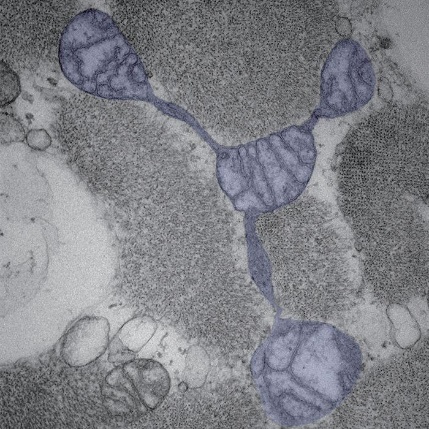
线粒体可以改变形状和大小,其中一些形成连接以分享信息
线粒体和疾病间的关系于1975年被首次阐明,耶鲁大学的道格拉斯 · 华莱士(Douglas Wallace)和同事们描述了线粒体DNA与一种遗传病的关联。20世纪90年代,研究者发现线粒体DNA变异会产生各种影响。每5 000人就会有1人患某种线粒体遗传病,可能会导致包括糖尿病、视力和听力障碍、学习困难以及其他一些问题。近十年来,科学家才开始认真探索线粒体对心理健康的影响,尤其是压力、焦虑和抑郁问题。
桑迪的工作源于对线粒体可能会改变特定大脑通路运作的预判。人脑会消耗约20%摄入的氧气,尽管脑在质量上只占了2%的体重。桑迪猜想,关键神经环路中细胞产能不足可以解释焦虑症患者总体动机和自尊的不足。
桑迪通过将大鼠置于竞争环境中来模拟社会阶层,她发现焦虑情绪更少的动物会取得更具统治力的地位。进一步研究显示,这些动物的伏隔核——脑中对动机行为和努力行为至关重要的区域——线粒体功能更好。
许多实验室的其他研究揭示了压力和线粒体间更深远的关系。2018年皮卡德和于今年早些时候去世的压力研究先驱布鲁斯 · 麦克尤恩(Bruce McEwen)共同发表了一篇荟萃分析,涉及23个有关线粒体和焦虑的研究,其中19个展示了“心理压力对线粒体显著的负面作用”,另外4篇提到了线粒体应对压力时大小或功能会发生改变。
柏林自然博物馆的安可 · 霍夫曼(Anke Hoffmann)和慕尼黑马克斯 · 普朗克精神病学研究所的迪特马 · 斯宾格勒(Dietmar Spengler)在2018年的一篇综述中总结了一些研究证据,有关线粒体能够调控脑面对早期生活压力时在结构和功能上的反应,线粒体作为“一种编码过程中的亚细胞结构”而发挥作用。线粒体功能和心理健康间联系的实验证据仍然是假设性的,且具有一定的局限性,但足以说服科学家开展进一步的研究。

马丁·皮卡德,哥伦比亚大学欧文医疗中心的研究者,他的实验室研究心理生物学现象中线粒体所起到的作用
线粒体间的交互对话
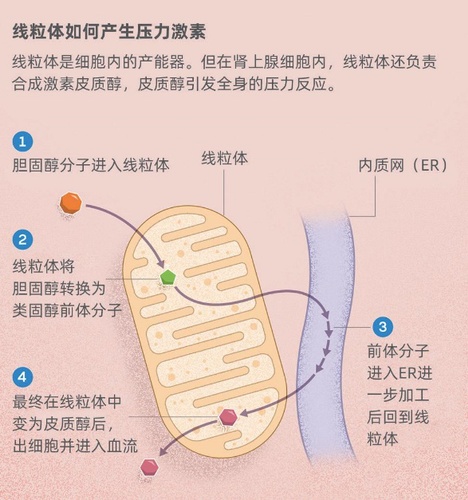
线粒体在压力下会发生怎样的变化依旧是个未解之谜。皮卡德的猜测是一切开端于压力反应被触发后,肾上腺细胞开始产生皮质醇。在这类细胞中,线粒体能够合成激素(在另一个细胞器内质网的帮助下),将胆固醇转化为皮质醇。皮质醇接着随血液遍布全身。特异的受体将皮质醇运输进细胞核,并最终激活大约1 000个基因以启动“战斗或逃跑”反应。但这些受体也会运载一些皮质醇进入细胞内的线粒体,并于线粒体DNA交互,使线粒体产能效率增高。
实际上可以说,肾上腺细胞内的线粒体产生压力激素,并进入全身的其他线粒体,带来整体性的压力反应。皮卡德评价道:“它产生了一种不同器官内线粒体间美丽的对话,而这还未被充分研究讨论。”
当线粒体对这些信号产生反应并做出调整时,它们改变会改变自身的形状,从豆状逐渐拉长成为面条样结构,如此分裂开来或是与其他的线粒体融合在一起。而干扰这一融合或分裂的过程会造成细胞损伤甚至死亡。皮卡德将这种干扰行为比作一种社交隔离——当线粒体无法相互交流时,它们的功能会下降。
研究压力如何影响脑细胞中的线粒体会牺牲一些动物——很多实验自然无法在人类身上进行。不过少数涉及人类的研究仍然暗示了一种关联性。
2019年发表于《心理神经内分泌学》(Psychoneuroendocrinology)杂志上的研究,主要作者皮卡德实验室的博士后卡洛琳 · 特朗福(Caroline Trumpff)、合作者匹兹堡大学的安娜 · 马斯兰(Anna Marsland)和布雷特 · 考夫曼(Brett Kaufman)在小样本的健康中年人中发现,急性心理压力和线粒体DNA短片段在细胞外的快速增多有一定关联性。通常情况下,这些线粒体DNA短片段会在与受伤或疾病相关的损伤性事件中释放出来。而这一效应在男性中更为显著。
这一压力相关的线粒体损伤的发生机制仍在研究中。桑迪介绍说,可能的解释是线粒体面对压力时的过分活跃会产生更多的活性氧分子,而这类物质对细胞有一定毒性。
科学家认同ATP参与了这一过程。皮卡德说:“机体对外界保持敏感,并启动内源性反应的能力,全都是能量驱动的。”研究表明遭受过度压力的动物会出现ATP产量被抑制的现象,这会对许多生理过程产生影响,尤其是细胞分裂过程。海马体与此的关联性很大,这一结构对记忆编码、学习、情感以及压力产生至关重要,也是脑中少数即使是成年哺乳动物,也有证据表明有新神经元不断产生的区域。
尽管线粒体在机体内广泛存在,不同组织甚至同一个细胞中线粒体结构和功能的差异性,让线粒体受到的损伤在特定的脑环路中会产生不同的表现,德国海因里希 · 海涅大学的卡门 · 梅纳霍(Carmen Menacho)和亚力山卓 · 普利吉欧涅(Alessandro Prigione)在6月发表于《国际生物化学和细胞生物学期刊》(International Journal of Biochemistry and Cell Biology)的一篇综述中讨论了这一问题。研究者发现线粒体通常会锚定于神经元中的特定部位,如靠近突触的位置,这显然有利于其功能。线粒体功能的实现可能也与脑中非神经元的胶质细胞有关,譬如通过髓鞘包绕神经元的少突胶质细胞和支持营养神经元的星形胶质细胞。神经元有时会将受损的线粒体运输给星形胶质细胞,而星形胶质细胞则会用健康的线粒体与之进行交换,如此减少细胞受到的损伤。如果压力干扰了譬如伏隔核这些脑区内的任何上述过程,那么就可能会对焦虑症产生影响。
探寻干预措施
卡林丘克提到,精神病学如今需要新的药物,那么以线粒体为目标的干预手段或能帮助受到压力、抑郁和焦虑困扰的人们。卡林丘克的实验室正研究一种细胞外大分子蛋白Reelin的抗抑郁潜能,Reelin能够为细胞迁移提供支架,并促进细胞间交流。压力会降低实验动物体内Reelin的水平,而这一现象似乎是因为线粒体的反应。2020年1月发表的早期结果显示,Reelin在雄性大鼠中有可观的作用,而实验小组希望进一步探索其在雌性大鼠中的作用。
桑迪的实验室在2017年的研究证明抗焦虑药物地西泮能够提高大鼠线粒体的功能。她和同事们在2019年1月发现一种促线粒体补剂(乙酰左旋肉碱)能够保护与人类抑郁行为相似的易感性小鼠。她如今正与制药公司合作进行临床前研究,探索能够促进线粒体输出的疗法,并收集与线粒体功能有关的代谢信息。
而皮卡德则对开发针对线粒体的药物持怀疑态度。他认为,基于线粒体功能的行为干预,譬如运动可能是有效的,运动或许是“你能为线粒体做的最好的事情”。
压力是相当复杂的一种现象,无法通过单因素或简单的一条通路去解释。杜克大学分子生理学研究所的马修 · 赫斯契(Matthew Hirschey)认为皮质醇是线粒体和压力间关系的主要驱动力,但也强调事实并非这般简单。“很显然,线粒体对神经功能的正常运作很重要——神经元是一种相当活跃的细胞,需要大量的能量来产生动作电位,因此线粒体至关重要,”赫斯契在一封邮件中写道,“但外界的压力源是否以及如何影响神经元内的线粒体功能仍是一个未知数。”
对他而言,线粒体更像是有关焦虑和压力生理学巨大拼图中的一个碎片。但这一碎片正不断吸引着研究者们,在这条道路上不断开拓新的天地。
资料来源 quantamagazine.org