近期的研究发现了可以通过级联反应缓解心脏疾病的分子机制。

斑块内部的胆固醇晶体――一种导致心血管疾病的组织
第二次世界大战结束后,美国与心脏相关疾病的发病数字直线上升。当时,人们对导致心脏疾病的原因还不甚了解。鉴于此,1948年,美国卫生署开展了一项具有里程碑意义的研究。5 000名马萨诸塞州弗雷明汉市的市民参与了这个项目的研究调查。弗雷明汉研究确认了多项容易导致心脏疾病的要素:吸烟、高胆固醇、高血压、糖尿病、肥胖以及缺乏运动。该研究也同样发现了一些有助于降低发生心脏疾病风险的因素。
在近几十年的研究中,研究人员开始尝试解开潜藏在这些致病风险中的分子路径。他们发现即使是一些看起来很直接简单的关联,例如高胆固醇和心脏病的联系,都比人们以往了解的情况要复杂得多,甚至有些研究者们已经开始对这些最基本的假设产生了质疑。
心脏疾病是一个总称,它包括各种各样的疾病。不过迄今为止,最常见的是冠状动脉心脏疾病。发病时,脂肪斑块沉着在心脏动脉内,这个过程被称为动脉粥样硬化。脂肪斑块会阻塞血液流动,斑块破裂还将造成更严重的问题:碎片混入血流,结成血块,阻断血液向心脏流动,导致心脏病发作。如果血块流向大脑,则会引起中风。
胆固醇是脂肪斑块的主要成分。“人体本身不能分解胆固醇,因此只能储存它或将其排出体外,还有一种方式就是将胆固醇转化为别的物质,例如激素。”哈佛大学公共健康学院预防心血管疾病的专家弗兰克·萨克斯(Frank Sacks)说。“因此,如果胆固醇进入了动脉血管,就出不来了,只能卡在那儿。”脂蛋白(脂肪和蛋白质复合物)是将胆固醇带入人体的载体。人们通常将过剩的低密度脂蛋白(low-density lipoprotein,LDL)称为“坏胆固醇”,它会沉积在动脉血管壁,加速形成动脉粥样硬化斑块,增加心脏病和中风发生的风险。
高密度脂蛋白的多重角色
高密度脂蛋白(High-density lipoprotein,HDL)比低密度脂蛋白的分子大,它能够清理动脉血管壁上的胆固醇斑块,将它们运载到肝脏后排出体外。流行病学的长期研究结果显示,血液中高密度脂蛋白含量高的人群患有心脏病的几率也较低。不过近期越来越多研究发现,高密度脂蛋白并非有百利而无一害。“只要你的低密度脂蛋白降低了,得心脏病的可能就也会降低。”萨克斯说。但是提高高密度脂蛋白却不一定完全有益。“我们发现高密度脂蛋白具有一些保护性的特性,但还没有完全确认这些特性是什么。”
不确定的部分原因在于,高密度脂蛋白包含不同大小和成分的分子。萨克斯和他的同事们推测,某些高密度脂蛋白会比其他同类更具有保护性。他们曾在一些脂蛋白的表面上发现了一些微小的载脂蛋白C-III。研究显示,载脂蛋白C-III和低密度脂蛋白在一起,会加剧动脉中的斑块形成。于是萨克斯开始考虑它遇上高密度脂蛋白的话会产生什么效果。
以此设想为基础,萨克斯的团队测试了两个大型流行病学研究中收集的血液样本。这两个研究分别是:“护士健康研究”,样本来自122 000位女性护士;“健康专业人士追踪研究”,研究对象是52 000位男性。不出所料,萨克斯发现高密度脂蛋白具有保护性,该指标较高的人群得心脏病的几率也较低。然而,当他将研究聚焦到带有载脂蛋白C-III的高密度脂蛋白(这种类型的高密度脂蛋白约占所有高密度脂蛋白总数的10%-15%)时,两组研究样本都分别显示出了逆转性的结果。研究人员将两组样本合并分析后,这种特征表现得更为显著。高密度脂蛋白带有载脂蛋白C-III后,“其实预示着更高的心脏病发病率,而不是降低这一风险。”萨克斯说。研究组将这种有害的高密度脂蛋白排除后,其余的高密度脂蛋白体现出了更强的健康保护性。
如果高密度脂蛋白能直接参与抵抗心脏病,那些体内带有能提高高密度脂蛋白产量的基因变异的个人得心脏病的几率应该会更少。事实上,减少低密度脂蛋白的基因变异的确能降低心脏病的风险。但是该原理并非直接逆转就能套用在高密度脂蛋白上。有研究者监测了能增加高密度脂蛋白胆固醇水平的基因变异效果,结果发现有这种基因变异的人群的心脏病发病率并没有降低。
种种研究表明,“我们仍需加强对高密度脂蛋白生物性的研究,要认识到这是一种很复杂的分子,这样才能确保我们能研发出最佳的治疗策略。”美国国家心、肺、血液研究所主任加里·吉本斯(Gary Gibbons)说。
发炎的心脏
导致动脉粥样硬化的机制和预防其发生的机制都相当复杂。举其中一例来说,过去30年的研究显示,炎症在发病中起到了一种中介作用。
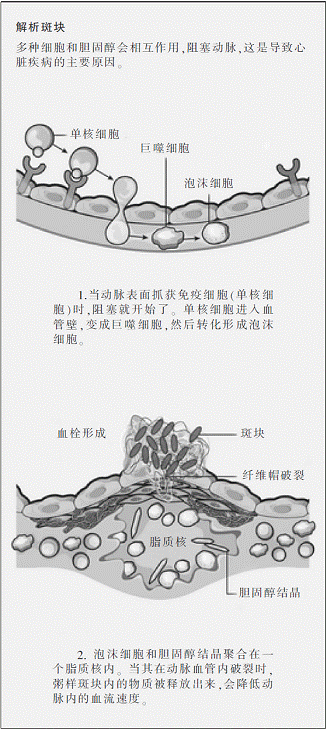
20世纪80年代,科学家们在脂肪斑块中发现了巨噬细胞,这是一种在炎症中能发挥作用的免疫细胞。现在,研究人员怀疑巨噬细胞会在斑块中出现是一系列事件导致的结果。动脉血管壁中的低密度脂蛋白提高了血管中排列的内皮细胞的数量,内皮细胞变化出粘性分子,堵截住血液中的单核细胞,也就是巨噬细胞的前身。与此同时,内皮细胞和平滑肌细胞开始分泌化学物质吸引单核细胞。这些被吸引来的单核细胞进入动脉血管壁,发育成熟变成巨噬细胞,它们将吞噬掉低密度脂蛋白胆固醇并急剧变大。“如果你的动脉血管壁里没有载有胆固醇的巨噬细胞,就不会有动脉粥样硬化斑块,这是斑块里最主要的细胞类型。”内分泌学家、俄亥俄州克利夫兰医学中心预防心脏病学和心脏康复学带头人史丹利·哈森(Stanley Hazen)解释说。由于它们的内部散布了许多胆固醇脂肪团,病理学家称其为泡沫细胞。泡沫细胞是动脉粥样硬化斑块的标志,它们和其他的免疫细胞生成化学信号,推动平滑肌细胞向斑块顶部移动,并形成一个坚实的帽子。在泡沫细胞积聚的过程中,有一部分会死去。这个帽子将这一团有生有死的泡沫细胞保护起来,免受血流的直接冲击。
炎症似乎会加剧斑块破裂的风险,这可能会激发潜在的致命性血栓的形成。胶原蛋白和其他一些物质能确保斑块纤维帽的稳固性。但斑块内的炎症介质会抑制胶原蛋白合成,并促进生成能够分解胶原蛋白的酶,导致纤维帽削弱、变薄,布里格姆医学中心和波士顿女子医院心血管主任彼得·利比(Peter Libby)说。利比的实验室和其他的研究团队的研究也显示,炎症介质会促进斑块中的巨噬细胞生成大量组织凝血活酶,加剧结块的形成。利比告诉记者:“所以说,炎症不仅仅参与了动脉粥样硬化的第一步,也与其最终并发症密切相关。”
利比最近又为这个故事加入了一段插曲。利比和他的同事们用在先天就较容易在动脉生成斑块的老鼠做实验,发现心脏病会提高骨髓中干细胞的释放量,并进一步加剧动脉粥样硬化。干细胞迁移到脾脏后,就变成了单核细胞。研究人员认为心脏病发作时产生的紧张和疼痛会引发交感神经系统加速释放干细胞,因此如果干扰这个连锁反应,就有可能预防心脏病的再次发生。研究组还在死于心脏病的患者的脾脏内发现了大量的干细胞,这表明上述原理在人体中的作用机制可能基本相同。
微生物的影响
与动脉粥样硬化发展相关的某些因素是全新且出人意料的。几年前,哈森曾无意中发现了一种令人惊异的机制路径,他当时在研究动脉粥样硬化相关的新陈代谢问题。哈森确认了一组“与心血管疾病风险显著相关”的化合物,其中一些是只能由细菌制造的代谢物。“我们一发现该路径中可能有细菌的参与,就开始检查肠道。”哈森说。他将视点聚焦到一种化合物上:三甲胺N-氧化物(TMAO)。
肠道微生物不直接产生TMAO。它们会将磷脂酰胆碱(一种在肉类和蛋类等动物产品中常见的成分)转化为一种名为三甲胺的恶臭气体,这种气体会再次被肝脏转化为TMAO。哈森的研究小组给老鼠注入TMAO后发现,“仅这一种物质本身就足以加速动脉粥样硬化。”当具备TMAO制造的微生物时,甚至三甲胺的前导物都能加速动脉硬化。不过研究人员发现,用抗生素杀灭老鼠肠道内的细菌就可以预防这种状况发生。
TMAO促进动脉粥样硬化的原因是多方面的。哈森和他的同事们发现该代谢物会提高巨噬细胞表面与低密度脂蛋白联接的受体的数量,导致巨噬细胞更倾向于吞噬胆固醇。“这条路径机制正位于胆固醇新陈代谢同炎症的关联处,”哈森说,“在动脉血管壁内,它对二者都有影响。”
如果微生物是问题的一部分,那么抗生素是否可以成为解决问题的一种手段?哈森指出,大量的随机对照试验测试了抗生素能否防止心脏病,但是还没有一个方法特别富有成效。问题可能在于药物测试并不能消灭生成TMAO的有机物,微生物可以迅速产生抗药性。“我们现在所做的老鼠实验都不是单抗生素的,而是用包含五种不同抗生素的鸡尾酒疗法。”哈森说道。但是他并不提倡使用抗生素鸡尾酒疗法预防心脏病。相反,他设想用益生菌,即有益的微生物改善微生物群落的健康,或使用药物以杀死细菌的方式中断致病路径。
自1940年代弗雷明汉心脏研究以来,对于该领域的研究工作已发生了很大的变化。科学家们对引起心脏疾病的原因有了更深的认识,心脏疾病的死亡率也有了大幅下降 。“心脏病学不可能有短期的革命,” 国家心、肺、血液研究所心血管研究部门主任迈克尔·劳尔(Michael Lauer)说,“这是现代医学的一项伟大成功。”但是,对于我们的心脏背叛我们的精确方式,尚未被完全揭示。
资料来源 Nature
责任编辑 彦 隐