
寻找生物标记――能对阿尔茨海默氏症的侵入发出警告信号的标记物――的工作一直在进行着。而开展这项研究的目的旨在赢得对这一疾病治疗的主动权,探索阿尔茨海默氏症防治的新模式
在过去的六年里,每周都有一箱又一箱的血液、脑脊液(CSF)和尿液样品运达位于费城的宾夕法尼亚大学的一个实验室。在那里,研究人员分别对这些样品进行记录、分类,并贴上标签,然后储存在七个巨大的冰柜中。
大约1.4万份样品被保存在16万个试管中,“每一个试管都非常珍贵”,宾夕法尼亚大学阿尔茨海默氏症研究中心主任约翰·特罗扬诺夫斯基(John Trojanowski)说,“万一发生断电,我们有备用的冰箱和报警系统。”
有很好的理由来解释这些防范措施。这些样本都有详细的病史、认知和临床措施以及高分辨率大脑图像的记录,至少,它们应在“整个阿尔茨海默氏症的研究中注解最为详尽的生物样品”之列。同是阿尔茨海默氏症神经影像学计划(ADNI)负责人之一的特罗扬诺夫斯基这样宣称。
目前,对阿尔茨海默氏症的决定性诊断需要对大脑进行尸检。然而对一些依然活着的患者,是否能通过其他诊断方法来分析影响患者行为和记忆力的变化?为此,医生们非常渴望能找到这样的一种标记物――可以确切地知道某某患了阿尔茨海默氏症,某某正处在该病症的哪一阶段。
当然,类似这样的标记物在临床诊断上非常有用,同时也能帮助研究人员测试那些可减缓病症的药物。当前流行的关于阿尔茨海默氏症的假说是,β-淀粉样蛋白沉积导致了脑细胞间不溶性淀粉样斑块的形成,这些斑块涉及到脑细胞的功能障碍和死亡。
“制药公司一直在研制抑制或减缓淀粉样蛋白的药物,他们也需要一些措施来监控这些疗法的效果,”ADNI成员、加州大学旧金山分校的放射学和精神病学教授迈克尔·维纳(Michael Weiner)说,“在这些过程中,影像和生物标记物显然是不可或缺的重要手段之一。”
目标:建立全球网络
2004年创建的ADNI是研究阿尔茨海默氏症规模最大、运行时间最长的计划之一――其目标是发现能有助于确定患者疾病是如何发展的生物标记物,以及测试患者对治疗的反应进展。目前确认了几个由小型研究发现的敏感标记物。
ADNI投资1.6亿美元,由美国国立卫生研究院(NIH)和包括默克、阿斯利康、辉
瑞和葛兰素史克在内的20个世界最大的制药公司,以及阿尔茨海默氏症学会和阿尔茨海默氏症药物发现基金会(ADDF)共同资助。维纳说:“这是NIH参与的最大的与私企合作的研究计划。”
迄今为止,ADNI分别在美国和加拿大的59个中心招募了1000名志愿者;欧洲、日本、澳大利亚和其他地区的合作中心也已经建立。“我们的目标是建立一个世界范围的网络,在这个网络内使用相似的研究方法,并能分享数据,”维纳说,“这样的话,进行国际间的治疗试验更加容易,也让我们能从中了解到各个国家间的区别。”
在寻找阿尔茨海默氏症的生物标记物过程中,ADNI是一个最全面的计划,但绝不是唯一的。目前,数十支研究团队正在分析大脑图像、DNA序列变化和基因、蛋白质以及免疫分子表达的模式。在不同情形下,其目标是鉴定那些可测量的差异――这些差异有助于阿尔茨海默氏症的诊断或反映这一疾病的进展。
切入:从MRI-PET入手
维纳说,ADNI的创建是缘于他的一个想法,即通过一项多位点研究课题来比较不同的大脑成像技术。例如,利用磁共振成像(MRI)和正电子发射断层扫描(PET)技术,以检测患者脑部结构变化和与阿尔茨海默氏症有关的代谢。初始与几家制药公司接触后,由于这项研究花费太大,任何公司都无法单独完成而未果。
之后,维纳与美国国家老龄问题研究所(NIA)负责痴呆研究的尼尔·巴克霍尔茨(Neil Buckholtz)进行了沟通。巧合地是,巴克霍尔茨也一直在思索类似的想法,为此,他们开始了一系列深入的讨论,这些讨论引发了一年后ADNI的建立。
在最初招募的800名志愿者中,200名患有阿尔茨海默氏症;400名有轻度认知能力损伤(MCI),MCI存有发展为阿尔茨海默氏症的较高风险;还有200名年龄相仿的健康对照组(包括维纳在内)。在花了约一年时间对操作和技术进行标准化之后,研究小组开始用PET技术和MRI技术,分别对志愿者大脑的代谢活动与特异性大脑区域体积进行测试。为了便于测试,研究人员利用放射性18-氟-2-脱氧葡萄糖(FDG)作为示踪剂,这种类型的葡萄糖与普通葡萄糖的化学性质相似,可在人体中产生有标记的代谢物,并且存留时间较长。
在测试的同时,研究人员对血液和CSF中各种化学成分的水平,包括β-淀粉样蛋白、tau蛋白、硫脂类(神经细胞膜成分)、异前列烷(氧化应激标记物)和同型半胱氨酸(一种氨基酸)也一一作了记录。研究发现,一些物质的变化与阿尔茨海默氏症有关联。维纳说:“ADNI的主要目的是证实在一些小型研究中做出的发现,并展示这些结果确实是可复制的且在临床上是有用的。”
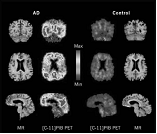
匹兹堡化合物B(PiB)在人类大脑的正电子发射断层扫描图像(PET)中照亮了淀粉样斑块


完善:新颖PET技术
随着这些分析数据的出现,一些测量值开始看似非常有希望,而另一些则半途而废。例如,CSF中硫脂类、异前列烷和同型半胱氨酸的水平被证明与阿尔茨海默氏症患病风险和疾病发展无关联。另一种潜在的标记物――血浆中同型半胱氨酸的水平――有助于区分MCI组和对照组,但不能区分MCI和阿尔茨海默氏症组。
PET:一种检测生物标记物的技术
最后,研究人员在CSF中鉴定出两个敏感的生物标记,以检测阿尔茨海默氏症和预测MCI向阿尔茨海默氏症的转变:一个是tau蛋白总水平;另一个是β-淀粉样蛋白水平,这是一种来自淀粉样前体蛋白质的具有42个氨基酸的多肽。表明对照组中功能下降的最好的CSF标记物是P-tau,它是带有额外磷酸基团的tau蛋白。
成像技术有助于鉴定大脑中与认知能力下降有关的变化。对进行期阿尔茨海默氏症患者施行MRI扫描,可揭示其颞叶和海马区缩小以及脑室扩大。海马是大脑中用于储存记忆和空间导航的区域,脑室是大脑容纳CSF的腔。FDG-PET研究显示,认知能力下降与大脑新陈代谢活动降低最密切相关。
ADNI开始不久,宾夕法尼亚州匹兹堡大学的研究人员开发出一种新颖的PET技术――他们使用一种称做匹兹堡化合物B(PiB)的放射性标记物,检测患者大脑中的淀粉样蛋白斑块。将这一技术结合CSF的测试,参与ADNI的研究人员现在能够确认随着大脑中聚合的β-淀粉样蛋白水平增加、CSF中可溶性β-淀粉样蛋白的减少。这不仅把PiB-PET确定为一种检测生物标记物的技术,还进一步确定了CSF中β-淀粉样蛋白的测量值可作为大脑病理学的可靠标记物。
“我认为,现在谈论这些经过验证的预测疾病或进展的生物标记物,还为时尚早,不过它的确朝着那一方向前进。”位于明尼苏达州罗切斯特市的梅奥诊所的罗纳德·彼得森(Ronald Petersen)说,目前他领导着ADNI的临床核心部门。尽管彼得森行事谨慎,但制药公司已经在临床试验中使用ADNI的测量方法。同时,ADNI在分布全球的各个中心继续对生物标记物进行确认或完善。

通过匹兹堡化合物B(PiB)放射性标记物,以检测患者大脑中淀粉样蛋白斑块
范围:从健康群体开始
瑞典哥德堡大学临床神经化学家卡伊·布伦诺(Kaj Blennow)教授,也是欧洲ADNI的成员。他认为尽管生物标记物使用时足够稳定,但目前还没有可靠的药物来测试这些标记物。“在药物开发中我们需要生物标记物,”他说,“但同时,我们也需要一种获准的、能影响(β-淀粉样蛋白)病理学或神经退行性的药物,便于验证这些生物标记物。”
在验证或使生物标记物标准化的目标上,ADNI可能已经开始着手进行了,但它的范围已远超出(预期)。维纳说:“ADNI已揭示,人们在患痴呆前的很长一段时间里,阿尔茨海默氏症的病理学就存在于大脑中。”这一研究表明,年龄在70岁及以上的表面看似健康的人,如果其大脑中存在β-淀粉样蛋白,则可能有发展为痴呆的更高风险。
的确,新的诊断阿尔茨海默氏症的NIH指导方针,已将这一疾病的定义扩充为包括MCI和症状发生前阶段。即便在早期阶段,β-淀粉样蛋白的存在可解释抗β-淀粉样蛋白疫苗实验失败的原因。布伦诺说,这些实验都是在那些患有发展较为迅速的阿尔茨海默氏症病人中开展的。“当你有如此之多的病理学,可能药物就不那么有效了,因此需要更早一些进行实验。”
不论原因是什么,需要更长期的研究跟踪健康人群,直到其中部分人阿尔茨海默氏症症状的出现。有NIH提供的未来六年资金保障,而这恰恰是ADNI计划要做的。ADNI项目团队已经招募了200名具有早期MCI的新参与者。截至目前,彼得森说:“他们正在缩减正常的对照组和后来的MCI测试者之间的人数。这真的是在排队,有点像我们盼望和希望的那样。”
测试:旨在简单有效
如果病理学在受试人群认知能力下降前存在的话,那么逻辑上的下一个步骤将是对老年人进行常规扫描以鉴定出这一疾病的指示标记,但这说起来容易做起来难。MRI非常昂贵,PET比MRI更昂贵且不易得到。布伦诺说:“只能在大型专业医院或研究机构中有PET仪器。”
腰椎穿刺通常是获得CSF的常用方法,但这仍比采血更具攻击性,并且还存在感染和损伤脊髓的风险。奥地利因斯布鲁克大学精神病学教授克里斯蒂安·哈姆佩尔(Christian Humpel)说:“我们不能对健康人或MCI患者进行腰椎穿刺,这是不道德的。”
理想的生物标记物将会在一个简单的血液测试中暴露出来,这一新标记物是人们经常建议并能满足的。过去几年中,提出的候选标记物包括丛生蛋白、羰基蛋白、血管紧张素转化酶、脂质过氧化产物和基因表达模式。哈姆佩尔认为,理想的标记物或许不久就会出现,或许它根本不存在。“我们或许不得不使用综合生物标记物。”
哈姆佩尔目前尚未发表他在血液单核细胞中发现的两个潜在的生物标识物(一种免疫分子和一种肿瘤抑制蛋白)的证据。血液单核细胞也是一种免疫细胞。他说,如果其他团队复制出他的这一发现,这些标记物就可能会在临床上获得重大应用。
与哈姆佩尔一样,斯坦福大学的神经学教授托尼·威斯-科雷(Tony Wyss-Coray)也认为综合生物标记物可能工作效力最佳。2007年他的团队提出了一套18种血浆蛋白作为标记物,并在实验中对阿尔茨海默氏症患者和对照组同时测试过。但是,这一方法没有产生可重现的结果。
“没能重现的一个原因是你使用了不同的工具,”威斯-科雷解释说。他的团队使用了抗体阵列芯片技术,这种技术在识别和结合蛋白质方面具有高度的差异性。如果所有的研究人员使用完全相同的阵列试剂盒和血浆制备技术,他们应该会得到相同的结果。不幸的是,威斯-科雷团队使用的试剂盒不再有效了。
创新:探索反向研究
对许多有前景的生物标记物研究来说,缺乏再现性听似是“丧钟”之声,它强调了ADNI在使标记物标准化方面付出的努力的重要性。对佛罗里达州斯克里普斯研究所的化学和癌症生物学教授托马斯·柯达德克(Thomas Kodadek)来说,这似乎在暗示需要一种不同的方法。
柯达德克团队决定从反向研究入手而不再使用抗体阵列来寻找血液中的蛋白――他们使用了1.5万种合成蛋白在寻找血液中的抗体。抗体是机体免疫系统产生的,能对外源分子(在某些情况下也对机体自身的一些分子)或抗原做出反应。“研究抗体比研究抗原更不易尝试,”柯达德克说,“抗体在疾病没发生前是不存在的,但在疾病存在时抗体则成百万倍地增加。”
柯达德克采用的方法,假定了阿尔茨海默氏症病理学包括一种免疫反应。尽管这一想法并不被所有研究人员认同,但这个看似冒险的假设似乎已见成效。他的团队发现了两种抗体――这些抗体在16名阿尔茨海默氏症患者中的14人高效表达,在16名对照受测者中只有2人高效表达。由于对照组年龄相当,这两个较高抗体水平的人可能有临床前期的疾病。
柯达德克说,用大致相同的方法进行试验后发现,淀粉样蛋白在认知症状下降前即已出现。随后他将该研究范围扩展到200人。“获得的结果非常出色,”他说,“有迹象表明我们的测试能检测到阿尔茨海默氏症的早期阶段。”
柯达德克计划在来自ADNI的血液样品中测试这些抗体是否也会扩增,以及能否利用其所有的图像和其他数据。其实,柯达德克并不孤单,因为有这样想法的人并不只是他一人。一些想使用样品但未能得到满足的研究人员开始对ADNI流露出不满,但ADNI不能向所有的人给出承诺。毕竟,16万个试管的样品听起来很多,但如果每一个新的候选生物标记物都要测试的话,这些样品将会急速减少。
资料来源 Nature
责任编辑 则 鸣
――――――――
本文作者露丝·威廉姆斯(Ruth Williams),纽约市布鲁克林区一科普作家。


![]()
![]()

