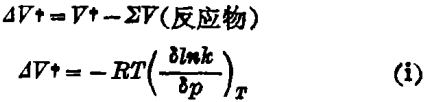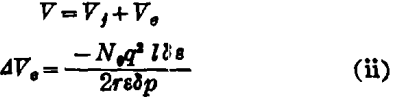高压液相化学直至最近它的发展还是不充分的,而且认为不安全。现在合成化学家们正在注意探索这些反应。目前已经出现了在20千巴(2000 MPa)压力下能够盛装20 ~ 25毫升液体的简易设备。在日本已经安装了一套在高达100千巴压力下能够处理1000毫升液体的国家级装置。看来今后人们很可能将对这类反应进行工业性的探索。
用加压的方法来促使发生化学反应已不是新鲜的事:工业上很多重要的化学工艺过程只有在高压下才能进行;众所周知的例子是哈伯(Haber)的氨合成和乙烯和丙烯的高压聚合。在这些气相反应中,采用高压可以增加反应物的浓度,从而获得较高的反应速率和比较有利的平衡点。这些表观的效应与所加的压力或多或少成线性关系。然而溶液反应的情况就大不一样,溶液反应的速率与所加的压力成对数关系。在一些有利的反应中,可以利用这种关系来大大提高反应速率。这种效应是由反应机制而不是化学计量学所决定的。
溶液中某一溶质所占的空间体积,通常用它的偏克分子体积V来量度。后者的物理意义是:将1克分子溶质溶解在大量溶剂中所引起的体积变化。增加压力有利于体积较小的那些产物的平衡移动。这种作用,可能与反应速率过程的活化平衡有关[埃文斯 - 波兰尼(Evans-Polanyi)原理]。这里对原始反应物的偏克分子体积(∑V),及其过渡态的偏克分子体积(V?)必须同时考虑。两者之差,即活化体积,?V?是决定反应速率与压力影响关系的一个物理量:
方程(ⅰ)表示当?V?为负值时(由于过渡态的偏克分子体积小于反应物的体积),增加压力可以提高反应速率。这种情况的逆关系也是成立的。压力仅在kbar范围(1千巴=103 atm)内才能引起反应速率的有效变化。对于物理 - 有机化学研究,压力加到1 kbar通常就已足够;但对制备化学研究,压力一般要加到10或甚至20千巴才行。从原刻上说,若要充分利用速率常数与压力之间的对数关系,所用的压力要尽可能高。?V?值的典型值范围为+20到-60厘米3克分子-1。这些数值与一定的结构变化有类,其中最重要的变化有以下两类:
A. 两种反应物的分子缔合形成一种加合物。这种情况引起体积减少,?V?为负值,因此增加压力可使反应加速。反之,如某一分子解离成几个小分子,致使体积增加,加大压力就抑制反应的进行。
B. 溶剂化(亦即与某种溶剂发生缔合)程度的增加,引起体积减少,当有离子电荷存在时,这种减少特别明显。对有离子生成的反应,或者那些过渡态有很大偶极矩的反应,活化体积很负。负的程度明显取决于溶剂的性质,介质极性越小,负值越大。这是由于电场的影响。在电场的作用下,与邻近某一电荷为q的离子相结合的溶剂会被拉开,介质的介电常数越小,离电荷中心拉开的距离就越大。这种“电致伸缩”效应可用德鲁特 - 能斯特(Drude-Nernst)方程(ⅱ)表示:
式中Ve是由电致伸缩引起的体积变化,Vj是溶质的固有范特沃尔体积,q2项表明随过渡态电荷增加,反皮速率将明显增大。与此相反,溶剂化程度减弱电荷中和,使体积增加,?V?为正值,增加压力就对反应起抑制作用。
环加成反应
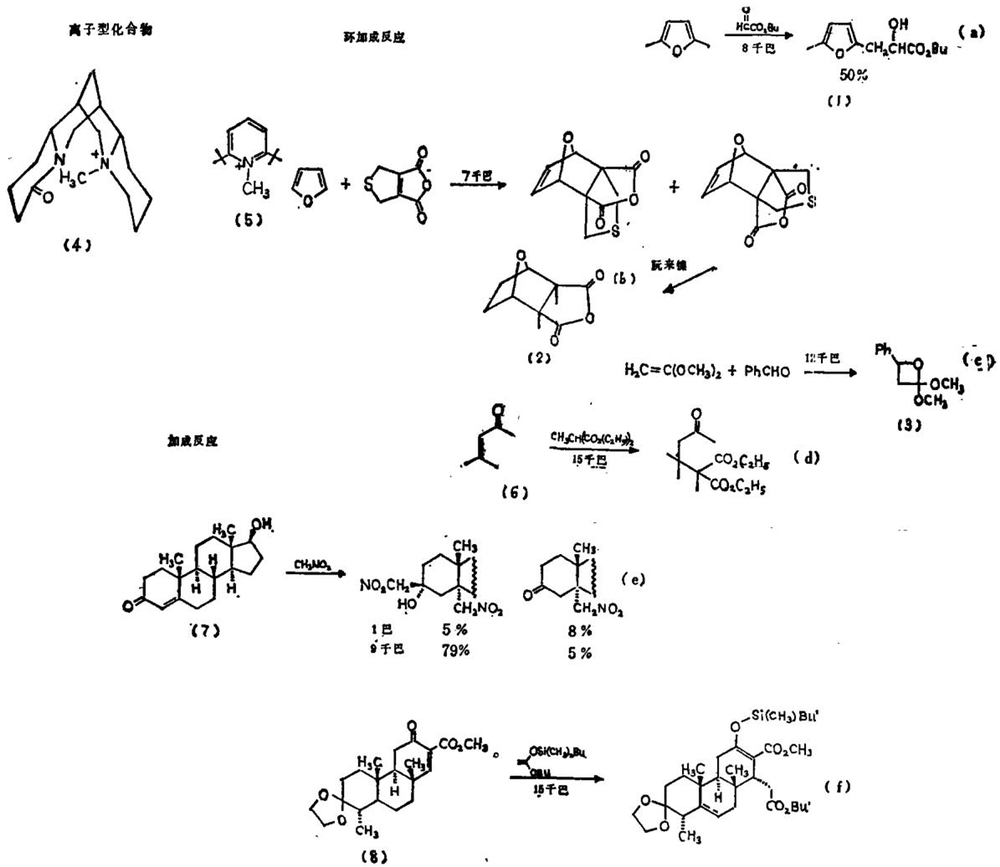
人们对高压下的狄尔斯 - 阿德尔(Diels-Alder)反应已作过广泛的研究。在这类反应中,呋喃及其衍生物很受注意。呋喃(C?H?O),2 - 甲基呋喃和2,5 – 二甲基呋喃,在高压下都能与各种单活化的亲二烯体生成环加合物。而在1 bar压力下这些反应均不能生成任何加合物。2,5 - 甲基呋喃与某些选定的羰基化合物在高压条件下进行反应,可以生成类型(1)的加合物[方程(a)]。这种产物可能是通过烯化反应形成的。
在一个实例中,呋喃与亲二烯体反应生成一种热不稳定的变形(strained)氧化二环[2.2.1]庚烷结构。这种反应容易向反方向进行。用增加压力,不用加热的方法来进行反应,往往有可能将加合物分离出来。但这些加合物在它们生成所必需的1巴压力反应条件下是要分解的。提高温度,会同时增加正向和逆向反应的速率,而增加压力只会加速正向反应的进行。另外,加合物的分解反应通常会引起体积增加,所以高压可以阻止这些反应的进行。
加压还可以克服空间位阻。例如,利用高压环加成法作为关键一步已经制得了多克量的斑螫素(2),方程(b)。加压对分子内的变化的有利效应要比分子间的反应略为小一些。但尽管如此,2 -(5 - 庚酮 – 6 - 烯炔)- 5 - 甲基呋喃,经过高压反应仍可转化成内桥式(endo)和外挂式(exo)加合物。值得注意的是,外挂式加合物在动力学上是有利的异构体。然而上述反应在常压下就无法进行,即使在各种路易斯酸存在下也是如此。
另外还有好几种有其它二烯类化合物参加的环加成反应,这些反应都是在高压下进行的,而且都很有用:
1. 噻吩(C?H?S)与呋喃相比较具有较高的共振稳定能,因此比较难于形成加成产物。不过,有一个报导噻吩与马来酐反应的例子:反应在100℃和15 kbar压力下进行3个小时,得到的产物几乎有50%是外挂式加合物。
2. N - 取代的吡咯(C?H5N)在高压下能生成环加合物,而在1 bar压力和回流的条件下,则主要生成α - 取代产物。
3. 磷酸(phospholes)在高压下,可以作为4π组元与炔属酯发生反应。
4. 被手性含酯取代物所取代的丁二烯可以同P - 苯醌发生反应生成环加合物。后者的对映体测量值超过50%。对>甲氧基丁二烯和(R)- 甘油醛丙酮化物反应中的不对称诱导作用作了进一步的研究,发现这种作用与温度和压力有关。在1 bar压力下,反应不发生;但在高压下能发生反应,而且收率很高。
5. 用加压方法亦可以明显促进[2π+2π]的环加成反应,因为所发生的那种反应主要是通过一种偶极过渡态进行的。这种情况有可能为合成四元环,如氧杂环丁烷(3)(方程c)提供一种有价值的方法。
成离子反应
有些化学反应所形成的过渡态的极性比初始态高,用加压的方法可以促进这类反应的进行。利用这—原理,可以来合成一些新的手性穴状配体。具体的方法是:先在高g下用2,2'-二碘二乙醚来处理某一单坏前体,然后常压条件下,用三苯基膦进行脱甲基化。
空间取代基较多的叔氮原子中心,在加压条件下可以进行季铵化,得到如(4)和(5)的那些盐类。这两种盐在lbar压力条件下都是无法生成的。另外,不活泼的烷基双二卤化物可参与旻希特金(Menschutkin)反应,例如二氯甲烷与叔胺在高压下反应生成亚甲基双铵盐。有人在曼尼期(Marnnich)反应中用二氯甲烷作为C1单元。另一些作者,利用某种仲胺和高度支链的酮,在9 kbar压力下制得了一组曼尼期碱。
还有作者,在室温和高压条件下制得了鳞盐[用于制备维梯希(Wittig)试剂],产率达94%。维梯希反应也是受压力加速的。利用这类反应可以合成三或四取代的链烯。
加成反应
人们对各种空间受阻的卜不饱和酮的迈查尔(Michael)加成反应也已作了研究,例如方程(d)中的结构(b)和方程(e)中的结构(7)。在高压下反应可以获得中等的收率。然而在加热或路易斯酸催化的条件下,这些反应的收率都很低。利用这类反应使莱基氧化物进行迈查尔加成反应,然后在15千巴压力下进行醛醇环化,还可以制备二环酮。
利用高压取得成功的一个令人瞩目的例子,是将烯酮乙缩醛加成为抗肿瘤药二化合物鸦胆丁(8)(方程f)的前体。这一加成反应在1巴压力下不能进行,甚至在155℃温度下也只能得到10%的产品。用路易斯酸催化会引起酮缩醇官能团的大量分解。然而用施加15 kbar压力的方法,在20℃下反应24小时,无需催化剂,即可分离得到91%的产物。从高压反应中回收得到的原料酮为总量的9%,而从高温,1巴压力下反应中回收的量只有10%(对应于80%的原料损失)。所以高压下的反应显著“完全”,这方面的例子是不难找的。
甲硅烷基烯酮乙缩醛在高压和中性条件下,能与醛或酮发生醇醛反应。这样,现在就有可能使那些对酸或碱敏感的分子进行这类反应。另外,现在有人利用加压的有机锡烷,在缓和的条件下使醛类烯醛化,获得了不同程度的成功。
目前所发现的对高压最敏感的反应之一是丙烯腈被醛和酮的取代反应。在lbar压力下,只有最活泼的醛能发生加成反应。实际上,乙醛的反应时间需要好几天。然而在5 kbar或稍低的压力下,在几分钟内就可以获得定量的收率。
醇类在高压条件下,可以用酰化或甲硅烷基化剂进行保护。当空间取代基较多或不稳定的醇,严重限制了那些原料分解不明显的加热反应的适用范围时,上述方法就特别有用。四硫代富瓦烯能与四氰基喹啉并二甲烷生成一种络合物,这种物质从有机性质上考虑,具有高度的导电性能。现在利用高压加成的方法,使二硫化碳或二硒化碳与各种炔烃进行加成反应,已有可能一步合成一组四硫代和四硒代的富烯化合物。另外现在也发现,二硫化碳加压至5 Kbar压力,在100℃温度下反应20小时,可以几乎定量地单独聚合成一种导电性材料。
聚合反应
加压有助于聚合反应的链增长。乙烯基单体在弱碱存在下,用加压的方法可以聚合成一种高分子量的物质。丙烯腈在高压下可单独聚合。二硫化碳在诏似的条件下也可以形成聚合物。苯乙烯与异氰酸苯酯只有在高压条件下,才能生成聚酰胺。看来今后很可能用高压的方法不仅是来制造新材料,而且还将用来制造较高分子量的聚合物。
上面我们叙述了如何用高压的方法来扩展许多重要反应的适用范围。高压反应过程所用的设备虽然成本较高,但由于生产快速,装置的尺寸也比较小,所以总的生产成本还是比普通的热反应方法要低,从另一方面考虑,高压设备的安全问题是一件麻烦事情,这是从气相反应工艺中得出的观点。不过应该记住,被压缩液体所含的潜能仅为同量压缩气体的百分之一左右,因此破坏性程度也成比例减小。所以这两类反应的安全规则应该有所区别。
[Chemistry in Britain,1987年第1期]