(上海市科委总师室)
人们通过重组DAN技术(通称基因工程技术),将天然存在于人体内起着各种生理功能的含量很少以至微量的肽、蛋白质,糖肽通过能编码这些物质的外源基因导入微生物或哺乳动物细胞达到表达,经高技术含量的加工过程获得近百种生物技术药物。截至1992年已有近50种生物药物进入不同阶段的临床试验或进入市场销售。美国制药业协会(现更名美国药品研究与制造商协会)1993年调查表明,有143种生物药物和疫苗正在进行临床试验,等待FDA批准。自1981年以来,美国FDA共批准了红细胞生成素(EPO)、组织型血纤维蛋白溶酶原激活剂(tPA)、人胰岛素、人生长激素、血液因子、集落刺激因子类、干扰素类、白细胞介素类各种生长因子等治疗剂和乙肝疫苗,总计16种产品上市,1994年销售额达到50.80亿美元。预计以年平均增长率12%计,至2004年可达到158亿美元。
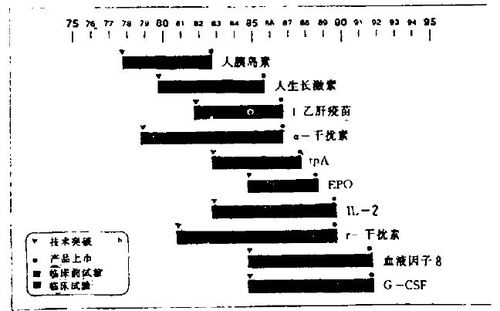
通常,一个生物药物,从技术突破(即获得基因克隆)到投放市场大体经历5~10年不等,对临床指征比较明确的,例如,人胰岛素、组织型血纤维蛋白溶酶原激活剂、红细胞生成素等,获得FDA批准上市较快大约5~6年不等,对临床指征针对性广泛,明确性稍差,则历时7~10年方获批准,上市较为缓慢(见下图)。
10种上市生物药物开发的时间进程
上述生物技术药物,均有不同生理功能,干扰素是伊萨克斯(Issacs)和林德曼(Lindermann)于1957年发现的,是多功能免疫调节因子,对免疫反应也有重要的调节作用。过去生产1克α-IFN约需30万升人血中的白细胞,而现在用大肠杆菌工程菌发酵生产,一个中等规模的实验室一天即可生产1~2克,而且生物活性极高,1毫克纯化的制品约含1亿以上国际单位。白细胞介素-2也是免疫系统的重要因子,它不仅在特异性免疫反应的调节上起重要作用,还具抗癌作用,因而是倍受重视的细胞因子,用IL-2在体外激活脾细胞所产生的LAK细胞和IL-2联合使用,对各种同源动物肿瘤有强大的抗转移作用。所谓集落刺激因子,是指在软琼脂中要依赖某种物质才能生长的粒细胞和单核细胞的骨髓祖细胞克隆与分化,这种物质通称“集落刺激因子(Colony Stimulating Factors,CSFs),人体中至少存在4种不同的CSF,其中2种特异性较高:粒细胞(G)-CSF,主要刺激中性粒细胞在体外增殖和成熟;巨噬细胞(M)-CSF,主要刺激产生巨噬细胞;多功能(multi)-CSF,亦称白细胞介素3(LI-3)能刺激多种不同的造血细胞。这些“因子”对造血机能障碍、发育不良或过度增生引起的疾病,或因癌症患者的放疗或化疗,艾滋病患者接受较大剂量抗病毒药物后所引起的骨髓严重抑制致使白细胞计数下降,均有治疗作用。CSF还对正常机体以及骨髓抑制的人有调节血细胞生成的功能。人体内估计有50000种蛋白质,起着不同生理作用,一旦通过类似阿波罗登月计划那样富有挑战性的“人基因组计划”的庞大工程,通过“作图(Map-ping)”对30亿个碱基对全部解码(decoding),就会对遗传病的诊断与治疗;对疾病的诊治会有根本的进步,哪怕1/50蛋白质数量的机率也有1000种药物在未来的世纪中诞生,成为贡献于人类征服疾病的武器。
生物技术药物在生物体内的表达和产物的分离纯化
生物技术药物是用重组DNA技术构建目的产物基因并插入细菌、酵母、哺乳动物细胞,昆虫细胞等四个表达系统来实现的。表一从六个方面比较了各自的优缺点并简述如下:
细菌表达系统:一般都采用大肠杆菌,表达水平高,约为细菌胞内蛋白质的10~40%;表达产物不具天然蛋白质构型,对含糖基的蛋白质来说,细菌缺失糖基化能力,表达的产物不含糖基;表达产物大都积聚在细菌的包涵体(个别的因构建上的特点可分泌在细菌体外),要将细胞分离与破碎,分离纯化,并经过蛋白质“复性”加工,而成为具生物活性的产品。
酵母表达系统:一般采用啤酒酵母或毕氏酵母,表达水平介于细菌与哺乳动物细胞之间,表达产物接近天然的蛋白质构型,但糖基化结构及数量有一定差异,多数分泌在细胞体外的培养液内,分离纯化也较简易,无需进行“复性”加工,是值得提倡的表达系统。
哺乳动物细胞表达系统:常用中国仓鼠卵巢细胞为表达系统,表达水平仅为细菌表达量的5%,但其表达产物更接近天然的蛋白质构型,有正确的糖基化结构与数量,通常分泌在细胞体外的培养液内,分离纯化相对简易,无需进行“复性”加工,即可成为具有较高生物活性的产品。
昆虫细胞多角病毒表达系统:具有介于哺乳动物细胞与细菌表达系统的优点,表达水平1~500毫克/升不等,具有良好翻译后修饰功能(细菌除外,酵母及哺乳细胞均具备),表达产物接近天然的蛋白质构型,但糖基化的结构及数量稍有差异,产物的抗原性、免疫原性及功能接近天然蛋白。目前用此表达系统作为生物技术药物生产仍有待工艺上的深入研究与完善。
*感谢复旦大学生命科学学院院长李育阳教授提供此数据
从产品的品质上评价“细菌”与“哺乳动物细胞”两种表达系统的例子是“粒细胞-集落刺激因子”的稳定性及血清中药物浓度的差异,其原因与该产品的糖基结构与数量有关:细菌无糖基化功能,因而其产品不含糖基,故pH8时残留生物活性为10%,pH7时为40%,37℃ 8小时后血浓度为28%;哺乳动物细胞具备糖基化功能,其产品含糖基,pH8时残留生物活性为80%,pH7为92%,37℃8小时后血浓度为80%。二种系统的表达产物有明显的差别。
从工艺上与产物品质上对表达系统的选择。不含糖基的生物技术药物都采用大肠杆菌为表达系统,具有培养基成本相对较低,培养条件易控制并污染机率低,培养周期短等优点,但难点不仅在于分离纯化工艺比较复杂,更因存在“复性”工艺以及要除去细菌本身产生的“内毒素”(致热物质),会使产品质量波动。但因基因工程工作者对大肠杆菌的背景了解甚多,构建表达系统的经验丰富,材料也多,一直将其作为首选的表达系统。其他三个系统的情况是:哺乳动物表达系统的表达水平低;构建经验不多,材料相对较少;培养条件苛刻,目前要解决许多工艺问题才能进入生物反应器进行大规模培养,培养成本昂贵,其中有些材料依赖进口解决;酵母系统是值得提倡的,但要作为首选系统,需进一步深入了解它的遗传背景,以获得更多的构建材料与手段,这将成为今后的研究课题。昆虫多角病毒表达系统虽然已在实验室规模下完成了诊断试剂的研制,在1987年突破FDA的法规障碍,首先批准了由该表达系统制造的Vaxsyn公司研究的gp160艾滋病疫苗并于1993年进入第三期临床试验。但是,在大规模昆虫细胞培养上尚存在着如下问题:温度引起表达产物的多寡差异十分明显,培养时要严格控制二氧化碳水平,以及如何正确选择多角病毒中的有关品种作为载体的问题。因此,与酵母相比,更要进行更多的遗传背景与构建手段的研究,才能使之成为成熟的“表达系统”。
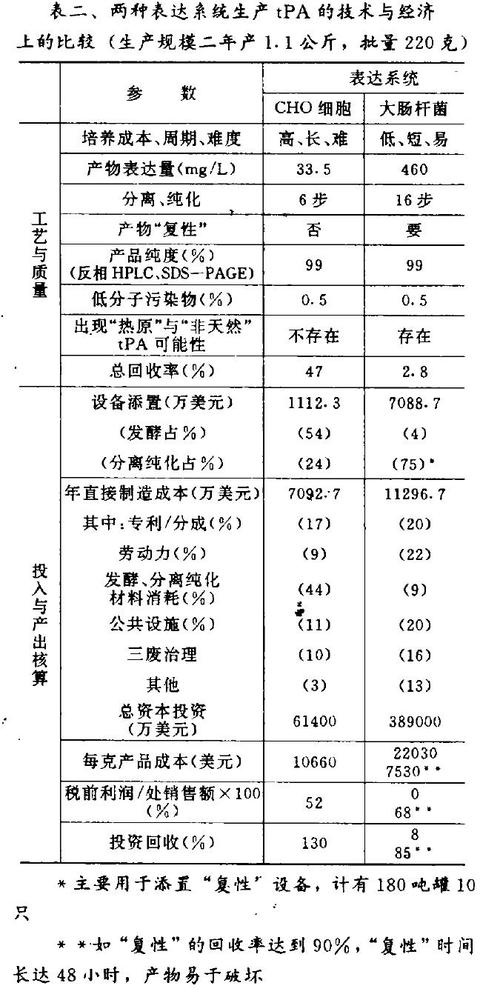
哺乳动物细胞与细菌两种表达系统生产组织型血纤维蛋白溶酶原激活剂(tPA)的案例
Rajiv V. Datar等以tPA为例从经济角度分析两个表达系统的结论对生物技术药物研制与产品化工作者在决策时无疑是值得参考的。就两个表达系统对产品的性质及分离纯化的工艺,从生产规模上比较了经济上的可行性(表二)。tPA是抗血栓药物用于急性心肌梗塞,1987年来一直由美国Genetech公司独家生产,1994年销售额2.6亿美元。它是高度专一的丝氨酸蛋白酶类物质,能使血纤维蛋白溶酶原转化为血纤维蛋白溶酶,然后作用于纤维蛋白达到“溶血栓”的作用,每一剂量售价2200美元。因而生产成本的高低与产品的质量决定着市场的占有率。
表列数据表明:两个表达系统尽管其产品质量都能符合FDA的“Point to Consider”的要求,但其生产经济效益有明显差异,其最显著点是大肠杆菌表达系统的分离纯化率低,并增加了“复性”的步骤而致设备、材料、劳动力的消费均远远超过哺乳动物细胞表达系统。若能解决关键的“复性”技术,提高“复性”收率,采用大肠杆菌表达系统亦有其优势。
韩国开展生物技术的概述
韩国是国民经济发展很快的国家。国民丰产总值由1962年的人均80美元发展到1989年的5000美元。政府于1984年通过“推进遗传工程”法案,各部设立生物技术R&D基金,建立遗传工程研究所。分管生物技术的政府部门是科技部,主要职能是推动大学与研究所开展生物技术基础研究,并将其成果推向产业界。
农牧渔业部的职能是应用生物技术培育动、植物良种。工业界担负60%的R&D。
政府对有关生物技术R&D的经费预算由韩国科技研究院、遗传工程研究学会,应用遗传学研究委员会编制。
遗传工程中心是一个基础研究所,有专职研究人员187人,其中70人有Ph. D学位。目前已迁入耗资1200万美元新建的中心,在韩国中部大德科学城。中心的R&D部有分子生物学、分子遗传学、蛋白质化学、细胞生物学、微生物工艺学、微生物资源、微生物生态、应用微生物,微生物遗传,生物调控、营养与生理、酶工程生化过程工程、食品工艺、食品生化、食品资源系统等构成;另有基因库、生物试剂、生物活性评价、中试工场等构成技术服务部。主要研究项目有:乙肝疫苗、细胞因子(如干扰素,白细胞介素等)、激素(如人或牛生长激素)、基因合成、新载体的开发、单克隆抗体的生产等。
1994年8月,韩国政府把生物技术列为尖端产业,预计到2000年的产值将从1993年的营业额1800亿韩元的基础上增长22倍,达到4万亿韩元。其中,药品将达到1.5万亿,食品达到1万亿,化学产品0.6万亿,环境治理产业达到0.4万亿韩元,其他(农药、生物工程仪器等)达到0.5万亿韩元。
为了缩小韩国同发达国家间在生物技术水平的差距,商工资源部决定从1995年开始增加研究开发资金,要求计划院从重型机械研究费中拨出第一笔(45亿韩元)用以生物技术研究。此外,还将重点支持基因工程产业化技术、微生物利用技术、新物质利用技术和生物工程技术等四个领域。