近一段时间,国际科学共同体关注的一个话题是纪念“人类抗癌之战40年”,全球最知名的两本科学刊物――英国的《自然》和美国的《科学》在3月底4月初先后刊登与癌症有关的专题报道,《自然》的专题重在讲癌症的预防,《科学》则比较全面,除了刊发社论,还约请了一批当今活跃在癌症基础研究和临床治疗一线的研究专家和医生评价介绍了人类与癌症最新这一轮为期40年的较量后,人们对癌症的认识及由这样一些认识带来的在药物和临床治疗上可能带来的新进展。本期本刊将和您一起关注癌症防治这个话题。
当代的癌症研究者需要从一种更清晰的生物学视角来寻求这些问题的答案,而这可能是未来癌症研究领域面临的最大挑战。
抗癌之战 有喜有忧
1971年,当时的美国总统尼克松在致国会的国情咨文中首次正式提出:“美国人医治这种该死的疾病(癌症)的时间成熟了,我们应该集中像研究核裂变以及登陆月球所付出的力量一样来做这件事,让我们的人民都为实现这个目标而奋斗”。同年12月,尼克松签署了《国家癌症法案》,宣布实施国家癌症行动计划。该项法案的核心内容是扩大国家癌症研究所(NCI)的规模、职责和范围,规定该研究所的所长由总统而非国立卫生研究院(NIH)任命,给予国家癌症研究所以相对的独立,同时大大增加了对癌症研究经费的支持,NCI的经费几乎在一夜之间上涨23%,达到2.3亿元。自从那时以来,NCI的经费持续攀升,每年超50亿美元,即使近年来通货膨胀仍有增无减。自1971年以来,NCI已经在癌症科学研究、癌症治疗和预防方面斥资900亿美元。
尽管人类同癌症的抗衡已有久远的历史,但是以国家立法的形式并投入巨资来做这件事,而且是科学实力最强的国家来推动,这在既往的人类文明史上并不多见,这也是1971年美国通过的癌症法案在人类抗癌史上具有重要意义的原因。
埃森巴赫(左)2003年设定的目标,即到2015年有望结束癌症带来的痛苦的愿望没有实现;艾尔伯茨:当癌症发现时,肿瘤已发展到含有数10亿以上的癌细胞。

但是平心而论,尽管美国自上世纪90年代以来在癌症得发病率和死亡率都在缓慢下降,7种主要癌症的死亡率也已有明显的下降(见表),但总体而言,这场抗癌之战并未取得预想的成功,人们研究的越多、越深入,发现牵扯到的问题越多,加上从研究成果到临床应用还有很长一段路要走,因此围绕这场与癌之战得失之争的争论一直没有停息过。1986年,生物统计学家约翰·贝勒在《新英格兰医学杂志》上发文提出,15年来癌症的发生率和死亡率基本上没有什么变化,美国正在失去这场针对癌症的战争,由此引发了持续多年的争论。2003年,受人类基因组计划完成后的乐观情绪影响,NCI所长安德鲁·冯·埃森巴赫设定了一个目标,称2015年有望结束癌症带来的痛苦和死亡。而这一设定目标引起了更大争议,因为针对癌症的计划虽然已挽救了大量的生命,但是有些癌症,如胰腺癌、脑癌、肝癌等并仍没有改善。
2009年8月,爱德华·肯尼迪参议员死于恶性神经胶质瘤――一种难以治愈的脑肿瘤――再次刺激了美国和国际社会关注恶性肿瘤对人类生命的巨大威胁。目前仅美国一年就要新增150万癌症患者,并每年夺走50万人的生命,差不多四分之一的人们最终都会因肿瘤而死亡。来自中国最大城市上海的最新统计显示,每100个上海人就有1人患癌症,上海癌症的总体发病率和死亡率已达到国际中等水平。
可能是受目前癌症发病率和死亡率仍居高不下的影响,此次纪念美国国家癌症行动计划实施40周年的报道少见到乐观、庆祝、成功等词语,至多是审慎地乐观,更多的是找问题、找不足。对于科学家而言,预防和治疗癌症这种疾病是一种巨大的挑战。《科学》杂志的社评说,40年前困扰研究者们的问题,如“染色体的变异缘于癌细胞吗”、“肿瘤细胞是必须从体内消除的外来入侵者吗”、“病毒在癌症中扮演了什么角色”等问题,除了病毒与癌症的关系大致搞清楚以外,其余依然困扰着今天的癌症研究者。《科学》的社论认为,当代的癌症研究者需要从一种更清晰的生物学视角来寻求这些问题的答案,而这可能是未来癌症研究领域的最大挑战。
癌症为何难以制服?
为何治疗这种疾病的任务如此复杂?《科学》杂志现任主编布鲁斯·艾尔伯茨解释说,因为到大多数癌症被检测出的时候,一个肿瘤已经发展到含有十亿以上的癌细胞。整个过程中,这些坏细胞会经多种方式乔装改变,设法逃脱人体生长控制系统的监管(这种生长控制系统使得构成人体的约80万亿个细胞处于一种可控状态),破坏细胞的自杀机制并进化出一种能对付人体免疫系统监管的耐受性。
癌细胞会不断地变化,其变异能力和改变基因的能力之强,使得任何一种单一的疗法几乎没有可能将其一网打尽,哪怕只有很少量的癌细胞只要存活下来就能不断增生,并最终扩展到可以再次为害的地步。这也是一些强有力的新疗法不断失败的原因。艾尔伯茨建议,为了有效灭杀癌细胞,应同时使用两种以上的药物。因为肿瘤很难应对两种以上针对癌细胞的不同路径的药物。另外一项既棘手又迫切的任务是能开发出一系列既能有效杀死特定的肿瘤细胞,又不伤及大量的正常细胞的药物。
DNA双螺旋模型的提出者詹姆斯·沃森认为,随着我们对导致疾病的分子机理的认识的深化,现在是发动一次真正意义上的对癌之战的时候了。艾尔伯茨认同沃森的这一说法,但他同时认为要确保这一计划的成功需扩大“癌症研究”的资助范围,其范围应远远超过癌细胞的工作本身。包括NCI应该拓宽对癌症研究的视野,要意识到对癌症治疗具有更深远意义的发现更多来自于模式生物的基础研究,而不仅仅是来自于对高度复杂的人体肿瘤的研究。而在肿瘤治疗方面,转化医学需要得到更多的重视。

重新定义癌症研究
面对久攻不下的癌症疾患,近年来癌症研究领域出现了与癌共存、带瘤生存的观点,一些研究者提出要重新定义癌症研究,要从生物学本质上加深对肿瘤机理的了解,例如《科学》杂志主编艾尔伯茨在2009年就提出,癌症是细胞生物学的一种疾病。我们人体是约80万亿细胞的集合体,任何一个细胞一旦其行为自私并且增殖失控就可能导致癌症。人体功能的正常发挥是由于每一个细胞都会接受来自近邻细胞的信号――告诉它该如何行为。绝大多数情况下,这些信号都是让细胞处于不需要分裂的休眠状态,但有时在人体受到创伤的情况下,信号就会指令细胞增殖和分裂,以产生康复所需要的新细胞。
之所以细胞会确切地知道下一步该怎么做,是因为每个细胞的DNA里都有一个基于指令的特定程序。但是随着人的老化,DNA指令的小错误会累积增多。当这种指令错误的量达到足够多――如达到10~20%,远远超过人体的自纠错能力时,肿瘤才会发生。此外,DNA序列维修时的缺陷也会诱导正常细胞向癌细胞转化,其突变率比正常细胞高出几百倍。这一缺陷主要会在早期诱发肿瘤的增生,高事故率是使得这些细胞摆脱人体多重自动纠错系统监管的要素。
人的细胞里至少有150种不同的蛋白质在帮助完成DNA修复,并由此形成了许多不同且重叠的修复通道。遗传学家和分子生物学家需要揭示这些修复通道的每一个发生改变后会带来什么,不仅是人体细胞,而且包括诸如细菌、酵母、蠕虫、果蝇、鱼和老鼠等各种模式生物;生化学家和化学家需要筛选可做药物开发的抑制剂;基因组和蛋白质组技术专家需要设计廉价的检验方法来检测导致高突变率的特定缺陷的检测方法。这样,抑制剂和能特定封堵缺陷通道的药物就能用于杀死癌细胞,而在现有的资助结构中,这些都未被视为重点。
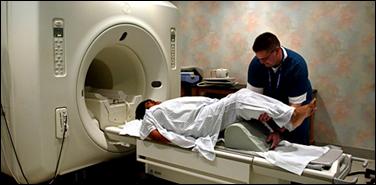
图为乳腺癌术前进行的MRI检查