肥胖已成为发达国家一个严重的健康问题,在发展中国家也日渐增多。它会引发人们患糖尿病、心脏病、脂肪肝及癌症的风险;掌握肥胖症生物学机理的有关知识将有助于人们的预防和治疗

肥胖的定义与环境因素
肥胖的定义为体内脂肪过多。过去是通过测定一个人在水里的重量并计算浮力来估算体内脂肪数量,这种方法比较麻烦。如今,人们常用的是身高体重指数(BMI)。不过,BMI――即以体重除以身高――虽然可以用来测定特定群体在某一时期的体重状况,但是对于个体却常常并不可靠――无法分辩脂肪和肌肉质量,而且身高的这一变量,取决于人口组成的变化和个人经验的判断。最近出现了一些直接测定脂肪的方法,譬如,通过排气量测定肌肉密度等,相比较BMI,这些方法更加可靠。
肥胖症是一个全球性问题。据保险统计表显示,对于白种人来说, BMI值为25(即超重)的人群,患有肥胖引发的医疗并发症或遭遇死亡的风险明显增加;如果BMI值超过30(即肥胖),则风险急剧上升。在美国,约有三分之一的人BMI值超过30,半数人口BMI值超过25,而每年用于治疗肥胖症的花费就超过600亿美元,其中很大部分用在了Ⅱ型糖尿病上。如今,中国、印度和其他国家的肥胖现象也日趋严重,而且随着国家的日益富裕,问题可能会进一步加剧。与白种人相比,同样面临糖尿病及其他新陈代谢疾病风险,亚洲人的BMI值显得更低,这更加显示了肥胖给亚洲人的健康所带来的不良后果。
生活方式或环境可能是引发肥胖的一种因素,但不是绝对的。就美国而言,绝大多数人都摄入过多的热量,但也仅仅只有半数的美国人超重。关键的问题是:同样摄入热量,有些人比其他人吸收得更多,从而变得肥胖。
人们往往认为,食物的摄入是一种自主的、有意识的行为。但有证据表明,人体能量摄取与输出之间的平衡很大程度上是由一个强大的、无意识的生物系统控制的。在不同的环境条件下,维持能量平衡的生物系统会合理地分配相应的脂肪总量。对捕猎采集者而言,脂肪太少易于挨饿;相反,脂肪太多又会增加捕猎的风险。因此,对群体而言,不管遗传变性是趋于苗条还是趋于肥胖,都可能是有益的,就看环境状况如何。这也许可以解释为什么长期营养不良的人,一旦无节制的摄入热量,往往会变得肥胖。
根据热力学定律,食物摄入与能量消耗保持平衡,体重可以得到控制。然而,负责平衡脂肪的生物系统会通过调节无意识的饮食驱动等方式来阻止体重的变化,不管是变轻或是变重。实际上,减少热量摄入或增加能量消耗,减肥者是可以在短时期内减轻体重。与此同时,生物学因素也将发挥作用,使人产生强大的、无意识的饮食冲动,直到又恢复到原有的体重。这里所面临的一个挑战性的问题是,调节饮食驱动的神经回路与反映人们减肥或增肥意愿的神经回路之间是如何互动的。
生物学因素控制肥胖生成
根据遗传理论发现,肥胖的遗传可能性,即源于遗传因素的几率在70%——80%之间,超过了其他大多数被广泛认可的生物学特质,如糖尿病、心脏病和癌症;而唯一高于肥胖的遗传几率的只有身高。遗传基因对肥胖的影响也可以从有关收养家庭的案例得到证明,跟收养儿童体重关系更为密切的不是养父母,而是他们的亲生父母。尽管如此,仍没有任何证据表明,肥胖完全归因于遗传基因,因为食不裹腹者是不可能变得肥胖。如此看来,也许是环境――主要指无节制地摄入热量――为肥胖基因携带者从可能肥胖发展成现实肥胖提供了条件。
基因突变也会引发肥胖,它们与其他基因共同构成了调节能量平衡的系统,编码瘦素(脂肪组织产生的一种荷尔蒙,它会影响很多生理系统,包括控制食物摄入和能量消耗的脑中枢)的ob基因就是其中之一。身体脂肪的瘦素水平上下波动,则导致食物摄入的减少或增加。以老鼠为例,如果ob基因发生突变,老鼠体内不再产生瘦素,体重会增加3倍,而脂肪增加5倍。
对人类来说,如果ob基因或作为瘦素受体的基因发生突变,同样也会发胖。瘦素受体位于下丘脑和脑部的一些外围组织里。下丘脑受伤之所以会引起肥胖,部分原因在于表达瘦素受体的神经元受到了损害。在下丘脑中,表达神经肽前体POMC的是一种由瘦素激活的神经元,如果它们或者它们的受体MC4发生突变,也会引起肥胖。
当然并非只有基因突变才会引起肥胖。大约有5%——10%的病态肥胖(BMI值大于或等于40)源于上述基因的突变,以及大脑回路中包括编码神经肽BDNF在内的其他功能基因的突变。不过,对于其他大多数人来说,体重的变化往往源于部分基因的组合以及与环境的互动。
根据全基因组关联研究,已经确认了几种可能影响体重的基因,其中就有FTO基因。尽管对该基因的功能尚未认识,但其内部DNA序列的变化足以导致3——5公斤体重的差异。像FTO这样已经发现可以引起肥胖的基因在总体人群中并不怎么起眼,因此尚不清楚它们是如何引发肥胖的。抑或是通过不同单基因的突变,或是通过多种基因潜在的复合影响,或者两种情形都存在。
瘦素能长期维持稳定的能量储存,而另一种系统则使血液中的养分在短时期内维持相对稳定的水平。该系统由血源性和神经性信号组成,控制着人体的饥饿感和饱腹感。其中,血源性信号既包括代谢物――如葡萄糖,也许会有氨基酸和脂肪酸,也包括消化系统荷尔蒙――如胃荷尔蒙葛瑞林以及诸如GLP——1、YY肽、胆囊收缩素、铃蟾肽和胰淀素等肠肽。这些短期信号作用于脑干和下丘脑的神经元,从而调节食物的摄入以及各餐的间隔。这种短效系统和长效系统(瘦素)之间通常保持互动。
食物摄入与体重是由一个反馈回路控制。以上短效系统和长效系统是由脂肪和肠道在内的许多组织构成,从这些组织发出的信号汇聚到大脑集成中心并在那儿解码。然后,神经传导通路会控制食物的摄入以及一些外围组织的新陈代谢。目前,人们在认识控制食物摄入的神经传导通路方面取得了实质性进展;但是,对于调节能量消耗、脂肪和葡萄糖新陈代谢的环路仍然停留在肤浅的认识层面。
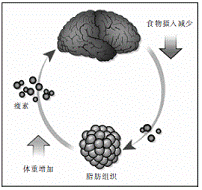
一旦体重增加,脂肪组织就会分泌更高水平的瘦素,此时,荷尔蒙进入大脑,并与瘦素受体结合,使人产生饱腹感,减少食物的摄入。反之,如果体重减轻,瘦素分泌水平就会减少,因而食物摄入就会增加。体重就这样维持相对不变
体重的减轻有利于缓解与肥胖有关的医学并发症,哪怕只是减少5——7公斤,对健康都大有裨益。但更多的减少则很难实现,因为生物学因素在其中发挥着相应的作用。因此,对肥胖者的建议是:尽己所能促进健康。譬如摄取对心脏健康有益的饮食,进行身体锻炼,尽力减肥,但也要符合健康的要求,大可不必被迫达到“正常”体重。
减肥外科手术是一种有效治疗肥胖的方法,它通过改变胃肠道的组织结构来减少食物摄入或吸收。但手术过程中可能会引发重大疾病甚至死亡,因此,这一疗法只供那些身陷重大医学难题的病人使用。另外,即使手术过后,食物摄入量显著减少,大多数病人仍然归于肥胖(BMI值大于30)。这一事实凸显了病态肥胖者与恢复正常体重者之间的生物学差异。
解决肥胖应以健康为本
迄今为止,人们对减肥外科手术的作用机制尚不清楚。许多人认为,它之所以有帮助,与其说是机械性的限制了食物摄取,不如说是手术改变了从胃肠道进入大脑的神经信号、新陈代谢信号和荷尔蒙信号。吸脂手术也是可供选择的方法之一,但它只是短期有效,因为大量脂肪被吸出后,瘦素水平随之下降,而食物摄入就会增加,直到最终恢复原来的肥胖度。而对那些瘦素水平较低的肥胖者来说,瘦素重置法是一种可行的疗法,它能大幅度减轻体重。对于小范围发生瘦素突变的肥胖者而言,采取该疗法后可获得明显效果,并且尚未发现任何缺陷。
目前为止,有关肥胖的研究取得了两方面的进展:一是识别控制饮食的神经传导通路,二是掌握了如何通过调节神经元的活动来影响饮食行为。譬如,对光的控制,包括被称为视紫红质通道的光激活离子通道,可以用来检测激活或抑制神经元的效果;另外,人们近来开始使用功能显像来绘制人脑中饮食控制区域的图像,这些研究揭示了神经生物学与心理学之间的联系。在针对肥胖疗法的深入研究方面,现有资料显示,瘦素和胰淀素共同发出信号而导致体重的减轻。现在的目标是对以上综合疗法的安全性和长期疗效进行评估。

与行为、遗传及新陈代谢相关的信号通过外围组织汇聚到大脑集成中心,经过处理,大脑会对饮食进行调节,同时也向特定的外围组织发送指令调节新陈代谢
目前需要解决的一个至关重要的问题是,不同形式的输入是如何引发饮食反应的。我们还不清楚,控制饮食的大脑中心区是如何表达这种复杂信息的,甚至不知道这些大脑中心区的确切位置。解决了这些问题也许可以揭示,在一定的神经生物学程度上,减肥的主观愿望如何以及为什么受制于饮食驱动力。另外一个具有挑战性的问题是,我们需要明确哪些遗传变异会造成体重差异。
当前,没有了饥饿的风险,而肥胖的存在只会引发各种疾病,如此,人类的进化必然趋于抵制肥胖。在瑙鲁,随着高热量饮食成为时尚,糖尿病发病率大幅上升,但接着又呈现下降趋势。这就意味着,当糖尿病发病率达到很高的时候,人体就出现了反制糖尿病的进化选择。另有证据显示,美国的肥胖发病率也已处在一个稳定的水平。因此,在未来的十几年里,人们的体重会保持一个稳定的状态。
不管未来的趋势如何,制定有效而且安全的针对肥胖的疗法是至关重要的,也是可能的。不过,短时期内不太可能开发出能使病态肥胖者恢复正常的药物。哪怕真有此类药物,也不能确定是否完全对健康有益。我们应该集中精力制定一种疗法,使人们能够减少适量的体重并维持合理的水平,从而促进身体健康。实际上,肥胖主要归因于生物学因素,人们最好不要妄加指责,以减轻肥胖人群的压力,鼓励他们更多地改善健康。这样,才能更好地反映大家的共同心愿。
资料来源 Nature
责任编辑 绍 衡


